
Allotropi Allotropisk transformation och huvudelement

De allotropi inom kemi är det kännetecknet som vissa kemiska element har att presentera sig i flera olika former men i samma tillstånd av materiens aggregering. Elementens struktur kan variera beroende på deras molekylära arrangemang och de förhållanden under vilka de bildas, såsom tryck och temperatur..
Endast när det gäller kemiska grundämnen används ordet allotropi, vilket anger vart och ett av de sätt på vilka ett element kan hittas i samma fas som en allotrop; medan föreningar som uppvisar olika kristallstrukturer gäller det inte. i det här fallet kallas det polymorfism.
Andra fall är kända, såsom syre, där allotropi kan uppstå som en förändring av antalet atomer i ämnet. I denna mening finns det en uppfattning om två allotroper av detta element, som är bättre kända som syre (Otvå) och ozon (O3).
Artikelindex
- 1 Allotropisk transformation
- 2 Allotropiska element
- 2.1 Kol
- 2.2 Svavel
- 2.3 Fosfor
- 2.4 Syre
- 3 Referenser
Allotropisk transformation
Som tidigare nämnts är allotroper olika sätt på vilka samma element kan hittas, så denna variation i dess struktur får dessa arter att visas med olika fysiska och kemiska egenskaper..
Likaså sker den allotropa transformationen mellan ett element och ett annat genom det sätt på vilket atomerna är ordnade i molekylerna; det vill säga det sätt på vilket länken har sitt ursprung.
Denna förändring mellan en allotrop och en annan kan inträffa av olika anledningar, såsom förändringar i förhållandena för tryck, temperatur och till och med förekomsten av elektromagnetisk strålning såsom ljus..
När strukturen hos en kemisk art ändras kan den också ändra dess beteende, modifiera egenskaper såsom dess elektriska ledningsförmåga, hårdhet (i fallet med fasta ämnen), smält- eller kokpunkt och till och med fysiska egenskaper som dess färg..
Dessutom kan allotropi vara av två typer:
- Monotropisk, när en av elementstrukturerna har större stabilitet än de andra under alla förhållanden.
- Enanthropisk, när de olika strukturerna är stabila under olika förhållanden men kan förvandlas till varandra på ett reversibelt sätt vid vissa tryck och temperaturer.
Huvudsakliga allotropiska element
Även om det finns mer än hundra kända element i det periodiska systemet, har inte alla allotropa former. De mest kända allotroperna presenteras nedan.
Kol
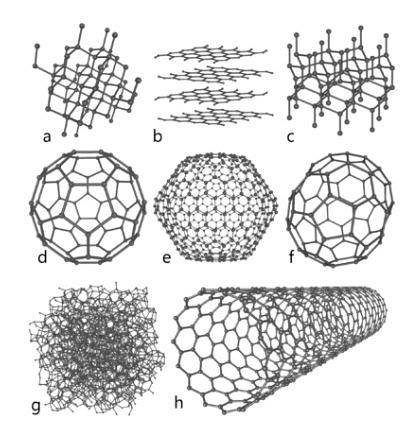
Detta element med stort överflöd i naturen representerar den grundläggande grunden för organisk kemi. Flera allotropa arter av detta är kända, bland vilka diamant, grafit och andra som kommer att exponeras nedan sticker ut..
Diamant
Diamanten visar ett molekylärt arrangemang i form av tetraedriska kristaller vars atomer är länkade med enstaka bindningar; detta innebär att de är ordnade genom hybridisering sp3.
Grafit
Grafit består av på varandra följande kolark, där dess atomer är länkade i sexkantiga strukturer med dubbelbindningar; det vill säga med hybridisering sptvå.
Carbino
Förutom de två viktiga allotroperna som nämns ovan, som är mest kända av kol, finns det andra såsom karbyne (som linjärt acetylenkol, LAC, är också känt), där dess atomer är ordnade på ett linjärt sätt genom trippelbindningar; det vill säga med hybridisering sp.
Andra
- Grafen, vars struktur är mycket lik grafit).
- Fulleren eller buckminsterfulleren, även känd som buckyball, vars struktur är sexkantig men dess atomer är ordnade i form av en ring.
- Kolnanorör, cylindriska i form.
- Amorft kol utan kristallstruktur.
Svavel
Svavel har också flera allotroper som anses vara vanliga, såsom följande (det bör noteras att alla dessa är i fast tillstånd):
Rhombiskt svavel
Som namnet antyder består dess kristallina struktur av åttkantiga romber och är också känd som α-svavel..
Monokliniskt svavel
Känd som β-svavel, har den formen av ett prisma som består av åtta svavelatomer.
Smält svavel
Det producerar prismatiska kristaller som är stabila vid vissa temperaturer och bildar nålar som saknar färg..
Plastsvavel
Även kallad svavel, den har en amorf struktur.
Flytande svavel
Den har viskositetsegenskaper som strider mot de flesta elementen, eftersom den i denna allotrop växer med ökande temperatur.
Match
Detta icke-metalliska element finns vanligtvis i naturen i kombination med andra element och har flera associerade allotropa ämnen:
Vit fosfor
Det är ett fast ämne med en tetraedrisk kristallstruktur och har tillämpningar inom militärområdet, även använt som ett kemiskt vapen..
Svart fosfor
Den har den högsta stabiliteten bland allotroperna i detta element och liknar mycket grafen.
Röd fosfor
Bildar ett amorft fast ämne med reducerande egenskaper men saknar toxicitet.
Difosfor
Som namnet antyder består den av två fosforatomer och är en gasform av detta element.
Violett fosfor
Det är ett fast ämne med en kristallin struktur med ett monokliniskt molekylärt arrangemang..
Scharlakansröd fosfor
Även fast amorf struktur.
Syre
Trots att det är ett av de vanligaste elementen i jordens atmosfär och ett av de vanligaste elementen i universum, har det få kända allotroper, bland vilka dioxygen och trioxygen sticker ut..
Dioxygen
Dioxygen är bättre känt under det enkla namnet syre, ett gasformigt ämne som är väsentligt för de biologiska processerna på denna planet..
Trioxygen
Trioxygen är bättre känt helt enkelt som ozon, en mycket reaktiv allotrop vars mest kända funktion är att skydda jordens atmosfär från externa strålningskällor..
Tetraoxygen
Bildar en solid fas av trigonal struktur med egenskaper för metastabilitet.
Andra
Det finns också sex andra fasta arter som syre bildar, med olika kristallstrukturer..
På samma sätt finns det element som selen, bor, kisel, bland andra, som presenterar olika allotroper och som har studerats med ett mindre eller större djup..
Referenser
- Wikipedia. (s.f.). Allotropi. Återställd från en.wikipedia.org
- Chang, R. (2007). Chemistry, nionde upplagan. Mexiko: McGraw-Hill.
- Britannica, E. (s.f.). Allotropi. Hämtad från britannica.com
- ThoughtCo. (s.f.). Allotropdefinition och exempel. Återställd från thoughtco.com
- Ciach, R. (1998). Avancerade ljuslegeringar och kompositer. Erhålls från books.google.co.ve




Ingen har kommenterat den här artikeln än.