
Natriumbisulfit (NaHSO3) struktur, egenskaper, användningsområden, produktion

De natriumbisulfit är en oorganisk fast substans bildad av en natriumjon Na+ och en bisulfitjon HSO3-. Dess kemiska formel är NaHSO3. Det är ett vitt kristallint fast ämne och på grund av dess antioxidativa egenskaper används det i stor utsträckning som ett konserveringsmedel (till exempel i vissa sylt).
NaHSO3 det är en reducerande kemisk förening, som är motsatsen till oxidant, och av denna anledning fungerar den som en antioxidant i många av dess tillämpningar, såsom i ätliga produkter, eftersom det förhindrar deras försämring.

Denna användning har emellertid ifrågasatts då fall av astma har rapporterats hos människor efter att de har ätit mat som innehåller natriumbisulfit. Det sägs till och med förstöra vitamin B1 i dessa.
Internationella hälsoorganisationer har begränsat användningen till mikromängder i livsmedel.
Emellertid har natriumbisulfit många andra användningsområden, såsom att erhålla jod, som ett antiinfektionsmedel, för att bleka vävnader, för nedbrytning av trä under beredning av pappersmassa, som desinfektionsmedel för öl- och vinfat osv..
Artikelindex
- 1 Kemisk struktur
- 2 Nomenklatur
- 3 fastigheter
- 3.1 Fysiskt tillstånd
- 3.2 Molekylvikt
- 3.3 Smältpunkt
- 3.4 Densitet
- 3.5 Löslighet
- 3,6 pH
- 3.7 Kemiska egenskaper
- 3.8 Risker
- 4 Skaffa
- 5 användningsområden
- 5.1 Inom massa- och pappersindustrin
- 5.2 Inom livsmedelsindustrin
- 5.3 Kontrovers över dess användning i mat
- 5.4 I jordbruksapplikationer
- 5.5 Vid erhållande av jod
- 5.6 Inom möbel- och träindustrin
- 5.7 I olika applikationer
- 6 Referenser
Kemisk struktur
Natriumbisulfit består av en natriumkatjon Na+ och en bisulfitanjon HSO3-.
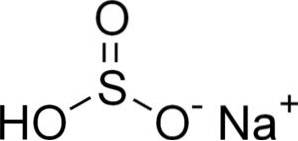
I vattenlösningar bildar bisulfit fyra arter. I utspädd lösning finns en balans mellan strukturerna som visas nedan:
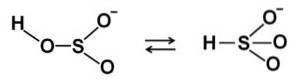
När koncentrationen ökar interagerar två bisulfitmolekyler med varandra och bildar pyrosulfitjonen StvåELLER5två-:
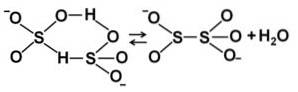
Nomenklatur
-Natriumbisulfit
-Natriumsulfit
-Natriumhydrosulfit.
Egenskaper
Fysiskt tillstånd
Fast vit kristallin.
Molekylvikt
104,06 g / mol
Smältpunkt
Det sönderfaller.
Densitet
1,48 g / cm3 vid 20 ºC.
Löslighet
Lösligt i vatten: 29 g / 100 g vatten.
pH
Dess lösningar är sura, med ett pH mellan 2,5 och 5,5.
Kemiska egenskaper
I vattenlösning natriumbisulfit NaHSO3 separeras i dess joner: natriumkatjonen Na+ och bisulfitanjonen HSO3-.
Om natriumbisulfit exponeras för luft tappar det lite SOtvå och oxideras långsamt till Na-sulfattvåSW4.
Vid uppvärmning till nedbrytning avger den rök av svaveloxider och natriummonoxid..
Det är ett reduktionsmedel som är motsatsen till oxidationsmedel. Och av den anledningen kan det fungera som en antioxidant.
Det har en lätt lukt av svavel. Det är inte brandfarligt.
Risker
NaHSO-natriumbisulfit3 det är starkt irriterande för hud och vävnader. Damm irriterar ögonen, näsan och halsen. Vid förtäring irriterar det magen. Stora doser kan orsaka våldsam kolik, diarré, depression och dödsfall..
Det är inte brännbart men vid upphettning producerar det irriterande och giftiga gaser.
Erhållande
Den framställs genom att mätta en natriumkarbonatlösning NatvåCO3 med svaveldioxid SOtvå och kristalliserar i lösning.
Applikationer
Inom massa- och pappersindustrin
NaHSO3 Det används vid matsmältningen av trä, så att det senare kan bli papper. Det fungerar också som en massa blekmedel.
Det används också för att avlägsna klor när pappersmassa har blekts med det..
I livsmedelsindustrin
Natriumbisulfit, på grund av dess reducerande egenskap, fungerar som en antioxidant.
Det används som konserveringsmedel i ett stort antal livsmedel och drycker, inklusive vin och öl, för att förhindra förstörelse och förbättra smak.
Det används för att bleka livsmedel, såsom vissa ätliga stärkelser.
Det minskar eller förhindrar matförstöring, tillåter konditionering av degen som används i bakverk och tjänar till att mjuka majskärnorna under våtmalning, bland andra användningsområden.
Förutom att kontrollera jäsning av vin och öl, fungerar det som ett antiseptiskt medel vid beredningen eftersom det fungerar som en sterilisator och fungicid i fat och kärl..

I torkade frukter finns den i koncentrationer över 100 ppm (ppm betyder "delar per miljon"), i många andra livsmedel finns den i koncentrationer mellan 10 och 100 ppm, såsom frysta och torkade potatisar, pickles, såser och sylt.

Kontrovers över dess användning i mat
Det har varit en viss oro för både de omedelbara och långvariga toxiska effekterna av natriumbisulfit i livsmedel. Det finns olika åsikter.
Det finns rapporter om biverkningar hos patienter med astma, som är en andningssjukdom, efter intag av mat med NaHSO3. Andra källor indikerar att bisulfitjonen kan förstöra vitamin B1 eller tiamin.

Men vissa forskare 1985 fann att natriumbisulfit skyddar mot strålning och kemiska medel och hämmar eller förhindrar omvandling av celler mot cancer. Låga doser är bäst.
Denna skyddande effekt har förklarats baserat på dess reducerande eller antioxidativa egenskaper och att den på detta sätt kan attackera fria radikaler.
Å andra sidan, Världshälsoorganisationen, eller WHO (för dess förkortning på engelska Världshälsoorganisationenrekommenderar som en acceptabel nivå av dagligt intag cirka 0,7 mg / kg av personens vikt.
Det betyder att det rekommenderas att inte överskrida den mängden..
United States Food and Drug Administration, eller USFDA. US Food and Drug Administration), klassificerad natriumbisulfit som "allmänt erkänd som säker".
I jordbruksapplikationer
NaHSO används i låga koncentrationer3 fungerar som en växttillväxtregulator för att förbättra fotosyntesen och främja avkastningen.
Det har testats för detta ändamål i olika typer av växter, såsom jordgubbar och teplanter..

Det är den aktiva ingrediensen i många bekämpningsmedel och biocider.
I vattenmiljöer kan det också påskynda omvandlingen av vissa herbicider till mindre giftiga produkter genom att eliminera klor..
Vid erhållande av jod
NaHSO3 är den reducerande föreningen som används för att frigöra jod från natriumjodat NaIO3. Detta är ett av sätten att få jod från källor som nitro från Chile eller något saltvatten.
Efter kristallisering av natriumnitratet från den råa Chile-nitratlösningen finns en NaIO-lösning kvar3 som behandlas med natriumbisulfit NaHSO3, genererar gratis jod.
2 NaIO3 + 5 NaHSO3 → 3 NaHSO4 + NatvåSW4 + Jagtvå
Inom möbel- och träindustrin
NaHSO3 Det har testats för att modifiera sojaproteiner och förbättra deras vidhäftningsegenskaper med trä för att limma ihop träbitar för att förbereda till exempel spånskivor, kartong eller papper, plywood, etc. Allt detta för möbler eller brädor, bland olika applikationer.

Detta görs för att ersätta traditionella formaldehydbaserade lim eftersom de både i sin tillverkningsprocess och under deras användning tenderar att frigöra formaldehyd i atmosfären, vilket är en giftig förening..
Natriumbisulfit förbättrar fastämneshalten i sojaproteinlimet och minskar dess viskositet, förbättrar dess flytbarhet så att det bättre tränger igenom träets porer, ökar sammanhållningen med det och mellan bitarna..
NaHSO-modifierat sojaproteinlim3 har god vattenbeständighet och utmärkt lagringsstabilitet på grund av antioxidantverkan av natriumbisulfit.
Detta bekräftar att NaHSO-modifierade sojaproteinlim3 är jämförbara med formaldehydbaserade lim och kan användas i möbel- och träindustrin, eftersom de är mindre förorenande.
I olika applikationer
Det har flera användningsområden, vanligtvis baserat på dess reducerande egenskaper (vilket är motsatsen till oxidationsmedel). Här är några applikationer.
-Inom fotografi.
-För lädergarvning för att ta bort hår från hudar.
-Terapeutiska användningsområden: antiinfektionsmedel. Det används som en antioxidant i vissa ögondroppar.
-Vid utvinning av naturgas genom hydraulisk sprickbildning.
-Vid färgning av fibrer används den för beredning av varma eller kalla badkar, för att solubilisera vissa färgämnen eller färgämnen..
-Som reduktionsmedel för tvätt eller blekning för att bleka ull-, siden- och vegetabiliska fibrer.
-I kemilaboratorier för att ta bort permanganatfläckar från hud och kläder. I biokemilaboratorier som konserveringsmedel för vätskor eller lösningar som kan försämras med tiden. Som ett kemiskt reagens.
-För koagulering av gummilatex.
-I den kosmetiska industrin som en antioxidant.
-Desinfektionsmedel och blekmedel.
-Vid behandling av avloppsvatten för att eliminera klor som använts i slutskedet av desinfektion och för att släppa ut redan behandlat vatten till miljön.

Referenser
- USA National Library of Medicine. (2019). Natriumbisulfit. Återställd från pubchem.ncbi.nlm.nih.gov.
- Qi, G. et al. (2013). Vidhäftning och fysikalisk-kemiska egenskaper hos sojaprotein modifierat av natriumbisulfit. J Am Oil Chem Soc (2013) 90: 1917-1926. Återställd från aocs.onlinelibrary.wiley.com.
- Borek, C. et al. (1985). Natriumbisulfit skyddar mot radiogenisk och kemiskt inducerad transformation i hamsterembryon och mus C3H / 10T-1/2-celler. Toxicol Ind Health 1985Sep; 1 (1): 69-74. Återställd från journals.sagepub.com.
- Friedler, E. et al. (2015). En kontinuerlig aktiv övervakningsstrategi för att identifiera tvärförbindelser mellan dricksvatten och avloppsdistributionssystem. Environ Monit Assess (2015) 187: 131. Återställd från link.springer.com.
- Cotton, F. Albert och Wilkinson, Geoffrey. (1980). Avancerad oorganisk kemi. Fjärde upplagan. John Wiley & Sons.
- Sunnyvale Cleanwater Program. (2019). Huvudplan för vattenföroreningskontrollanläggning. Återställd från sunnyvalecleanwater.com.
- Barros Santos, C. (2008). Tillsatser i det spanska livsmedlet och lagstiftningen som reglerar deras godkännande och användning. Vision Books. Återställd från books.google.co.ve.



Ingen har kommenterat den här artikeln än.