
Komprimerbarhet av fasta ämnen, vätskor, gaser, exempel
De kompressibilitet av ett ämne eller material är den förändring i volym som den upplever när den utsätts för en tryckförändring. I allmänhet minskar volymen när trycket appliceras på ett system eller objekt. Ibland händer emellertid motsatsen: en tryckförändring kan ge en explosion där systemet ökar i volym eller när en fasförändring äger rum..
I vissa kemiska reaktioner kan detta hända och även i gaser, eftersom när kollisionsfrekvensen ökar, uppstår de avstötande krafterna..

När du föreställer dig hur lätt eller svårt det kan vara att komprimera ett objekt, överväga de tre tillstånd som materia normalt är i: fast, flytande och gas. I var och en av dem håller molekylerna vissa avstånd från varandra. Ju starkare bindningarna som sammanfogar ämnets molekyler som utgör objektet och ju närmare de är, desto svårare blir det att orsaka en deformation.
Ett fast ämne har sina molekyler mycket nära varandra, och när man försöker föra dem närmare varandra uppstår motbjudande krafter som gör uppgiften svår. Därför sägs det att fasta ämnen inte är särskilt komprimerbara. I vätskemolekylerna finns det mer utrymme, så deras kompressibilitet är större, men ändå kräver volymförändringen vanligtvis stora krafter.
Så fasta ämnen och vätskor är knappast komprimerbara. Det skulle ta en mycket stor tryckvariation för att uppnå en märkbar volymförändring under så kallade normala tryck- och temperaturförhållanden. Å andra sidan komprimeras och dekomprimeras gaser, eftersom deras molekyler är mycket fördelade.
Artikelindex
- 1 Komprimerbarhet av fasta ämnen
- 1.1-Komprimering av ett material
- 2 Lösta övningar-exempel
- 2.1 -Löst övning 1
- 2.2 -Löst övning 2
- 2.3 -Löst övning 3
- 3 Kompressibilitet i gaser
- 3.1 -Löst övning 5
- 4 Referenser
Solid kompressibilitet
När ett objekt till exempel nedsänks i en vätska, utövar det tryck på objektet i alla riktningar. På detta sätt kan vi tro att objektets volym kommer att minska, även om detta i de flesta fall inte kommer att märkas..
Situationen kan ses i följande bild:
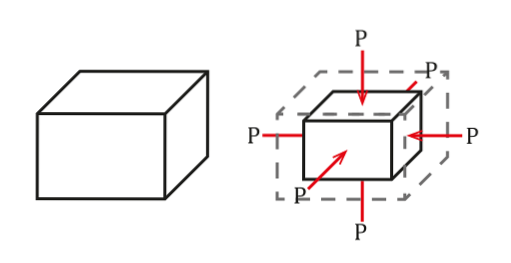
Trycket definieras som kraft per ytenhet, vilket kommer att orsaka en volymförändring AV proportionellt mot den ursprungliga volymen för objektet Veller. Denna volymförändring beror på dess egenskaper..
Hookes lag säger att den deformation som ett objekt upplever är proportionell mot den stress som appliceras på det:
Stress ∝ Stam
Den volymetriska deformationen som en kropp upplever kvantifieras med B den erforderliga proportionalitetskonstanten, som kallas materialets volymetriska modul:
B = -Stress / Strain
B = -AP / (AV / Veller)
Som AV / Veller är en måttlös kvantitet, eftersom den är kvoten mellan två volymer, har den volymetriska modulen samma tryckenheter, som i det internationella systemet är Pascal (Pa).
Det negativa tecknet anger den förväntade volymminskningen, när objektet är tillräckligt komprimerat, det vill säga trycket ökar.
-Komprimerbarhet av ett material
Det inversa eller ömsesidiga värdet av den volymetriska modulen kallas kompressibilitet och betecknas med brevet k. Därför:

Här k är det negativa av den fraktionerade volymförändringen per tryckökning. Dess enheter i det internationella systemet är inverserna av Pa, det vill säga mtvå / N.
Ekvationen för B eller för k om du föredrar, är tillämplig på både fasta ämnen och vätskor. Konceptet volymetrisk modul används sällan på gaser. En enkel modell för att kvantifiera volymminskningen som en riktig gas kan uppleva förklaras nedan..
Ljudets hastighet och kompressibilitetsmodulen
En intressant applikation är ljudets hastighet i ett medium, vilket beror på dess kompressibilitetsmodul:

Lösta övningar-exempel
-Löst övning 1
En massiv mässingsfär vars volym är 0,8 m3 den tappas i havet till ett djup där det hydrostatiska trycket är 20 M Pa större än vid ytan. Hur kommer sfärens volym att förändras? Det är känt att mässings kompressibilitetsmodul är B = 35 000 MPa,
Lösning
1 M Pa = 1 Mega pascal = 1. 10 6 Pa
Tryckvariationen i förhållande till ytan är DP = 20 x 10 6 Pa. Tillämpar ekvationen för B har vi:
B = -AP / (AV / Veller)
Därför:

AV = -5,71.10 -4 x 0,8 m3 = -4,57 x 10-4 m3
Volymskillnaden kan ha ett negativt tecken när den slutliga volymen är mindre än den ursprungliga volymen, därför överensstämmer detta resultat med alla antaganden vi hittills har gjort.
Den mycket höga kompressibilitetsmodulen indikerar att en stor tryckförändring krävs för objektet för att uppleva en märkbar volymminskning..
-Övning löst 2
Genom att sätta örat mot järnvägsspåren kan du se när ett av dessa fordon närmar sig på avstånd. Hur lång tid tar ljudet när man reser på stålskenor om tåget ligger 1 km bort?
Data
Ståldensitet = 7,8 x 10 3 kg / m3
Stålkompressibilitetsmodul = 2,0 x 10 elva Pa.
Lösning

Den ovan beräknade kompressibilitetsmodulen B gäller även vätskor, även om det vanligtvis krävs en stor ansträngning för att producera en märkbar volymminskning. Men vätskor kan expandera eller dra ihop sig när de värms upp eller svalnar, och lika om de är trycklösa eller trycksatta..
För vatten under standardtryck och temperatur (0 ° C och en atmosfärstryck ungefär eller 100 kPa) är den volymetriska modulen 2100 MPa. Det vill säga cirka 21 000 gånger atmosfärstrycket.
Av de anledningarna anses vätskor i de flesta applikationer vanligtvis vara komprimerbara. Detta kan kontrolleras omedelbart med numerisk tillämpning.
-Övning löst 3
Hitta den fraktionerade minskningen av vattenvolymen när den utsätts för ett tryck på 15 MPa.
Lösning

Kompressibilitet i gaser
Gaser, som förklarats ovan, fungerar lite annorlunda.
Att veta vilken volym de har n mol av en viss gas när den hålls begränsad vid ett tryck P och vid en temperatur T, tillståndsekvationen används. I tillståndsekvationen för en idealgas, där intermolekylära krafter inte beaktas, säger den enklaste modellen att:
P.Videalisk = n. R. T
Där R är den ideala gaskonstanten.
Förändringar i gasvolym kan utföras vid konstant tryck eller konstant temperatur. Till exempel, genom att hålla temperaturen konstant, är den isotermiska kompressibiliteten ΚT det är:

I stället för symbolen "delta" som användes tidigare när man definierade konceptet för fasta ämnen, för en gas beskrivs det med ett derivat, i detta fall partiellt derivat med avseende på P, vilket håller T konstant.
Därför BT den isotermiska kompressibilitetsmodulen är:

Och den adiabatiska kompressibilitetsmodulen B är också viktig.adiabatisk, för vilka det inte finns något inkommande eller utgående värmeflöde.
Badiabatisk = γp
Där γ är den adiabatiska koefficienten. Med denna koefficient kan ljudhastigheten i luft beräknas:

Använd ovanstående ekvation och hitta ljudets hastighet i luften.
Data
Den adiabatiska kompressibilitetsmodulen för luft är 1,42 × 105 Pa
Luftens densitet är 1225 kg / m3 (vid atmosfärstryck och 15 ºC)
Lösning

Istället för att arbeta med kompressibilitetsmodulen, som en enhetsförändring i volym per tryckförändring, kompressibilitetsfaktor för en riktig gas, ett annorlunda men illustrativt koncept för hur verklig gas jämförs med idealgas:
P. Vverklig = Z. R. T
Där Z är kompressibilitetskoefficienten för gasen, som beror på de förhållanden under vilka den finns, i allmänhet en funktion av både trycket P och temperaturen T, och kan uttryckas som:
Z = f (P, T)
Vid idealgas Z = 1. För riktiga gaser ökar Z-värdet nästan alltid med tryck och minskar med temperaturen.
När trycket ökar kolliderar de gasformiga molekylerna oftare och de avstötande krafterna mellan dem ökar. Detta kan leda till en ökning av volymen i den verkliga gasen, varigenom Z> 1.
Däremot är molekylerna fria att röra sig vid lägre tryck och attraktiva krafter dominerar. I ett sådant fall, Z < 1.
För det enkla fallet med 1 mol gas n = 1, om samma tryck- och temperaturförhållanden upprätthålls, genom att dela de föregående ekvationerna med term, får vi:

Vverklig = Z Videalisk
-Övning löst 5
Det finns en verklig gas vid 250 ºK och 15 atm tryck, som har en molär volym 12% mindre än den som beräknas med den ideala gasekvationen för tillståndet. Om tryck och temperatur hålls konstanta, hitta:
a) Kompressibilitetsfaktorn.
b) Molvolymen för den verkliga gasen.
c) Vilken typ av krafter dominerar: attraktiv eller motbjudande?
Lösning
a) Om den verkliga volymen är 12% mindre än idealet betyder det att:
Vverklig = 0,88 Videalisk
För 1 mol gas är kompressibilitetsfaktorn därför:
Z = 0,88
b) Välja den ideala gaskonstanten med lämpliga enheter för de angivna uppgifterna:
R = 0,082 L.atm / mol.K
Molvolymen beräknas genom att lösa och ersätta värden:
c) Attraktionskrafter dominerar, eftersom Z är mindre än 1.
Referenser
- Atkins, P. 2008. Fysisk kemi. Ledare Médica Panamericana. 10 - 15.
- Giancoli, D. 2006. Fysik: principer med tillämpningar. 6th. Ed Prentice Hall. 242 - 243 och 314-15
- Mott, R. 2006. Fluid Mechanics. Pearson Education 13-14.
- Rex, A. 2011. Grundläggande fysik. Pearson Education. 242-243.
- Tipler, P. (2006) Fysik för vetenskap och teknik. 5: e utgåvan Volym 1. Redaktionellt Reverté. 542.



Ingen har kommenterat den här artikeln än.