
Dimetylanilinstruktur, egenskaper, syntes, användningar

De dimetylanilin eller dimetylfenylamin är en organisk förening som bildas av en bensenring med en aminogrupp substituerad med två metylgrupper. Dess kemiska formel är C8HelvaN.
Det är också känt som N, N-dimetylanilin, eftersom det är ett derivat av anilin i vilket väteatomerna i aminogruppen ersätts av två metylgrupper. Detta gör det till en tertiär amin.
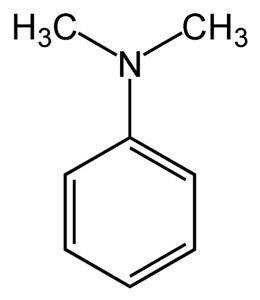
N, N-dimetylanilin är en ljusgul till brun oljig vätska med den karakteristiska lukten av aminer. Det är en basisk förening och reagerar med salpetersyra för att bilda en nitrosoförening. När den utsätts för luft blir den brun.
Det används vid tillverkning av färgämnen för färger. Den används också som en aktivator för polymerisationskatalysatorer och i blandningar som används för bildinspelning. I sin tur har den använts vid syntes av antibakteriella eller antibiotiska föreningar, såsom vissa penicillin-härledda cefalosporiner. N, N-dimetylanilin är också en bas för att erhålla andra kemiska föreningar.
Det är en brännbar vätska och vid uppvärmning till sönderdelning avger den giftiga ångor. Akut exponering av människor för N, N-dimetylanilin kan leda till negativa effekter som huvudvärk, yrsel, minskat syre i blodet och blåaktig missfärgning av huden, bland andra symtom..
Artikelindex
- 1 Struktur
- 2 Nomenklatur
- 3 fastigheter
- 3.1 Fysiskt tillstånd
- 3.2 Molekylvikt
- 3.3 Smältpunkt
- 3.4 Kokpunkt
- 3.5 Flampunkt
- 3.6 Ångtryck
- 3.7 Självantändningstemperatur
- 3.8 Densitet
- 3.9 Brytningsindex
- 3.10 Löslighet
- 3.11 Grundläggande konstant
- 3.12 Kemiska egenskaper
- 3.13 Risker
- 4 Syntes
- 5 användningsområden
- 5.1 Inom färgämnesindustrin
- 5.2 Vid tillverkning av ljushärdbara blandningar
- 5.3 Inom glasfibertillverkning
- 5.4 I syntesen av antibiotika
- 5.5 Vid katalys av kemiska reaktioner
- 5.6 I olika applikationer
- 6 Referenser
Strukturera
Följande figur visar den rumsliga strukturen för N, N-dimetylanilin:
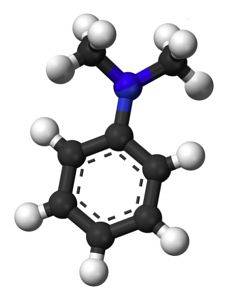
Nomenklatur
- N, N-dimetylanilin
- Dimetylanilin
- Dimetylfenylamin
- N, N-dimetylbensenamin
N, N placeras i namnet för att indikera att de två metylgrupperna (-CH3är fästa till kväve (N) och inte till bensenringen.
Egenskaper
Fysiskt tillstånd
Ljusgul till brun vätska.
Molekylvikt
121,18 g / mol.
Smältpunkt
3 ºC.
Kokpunkt
194 ºC.
Flampunkt
63 ºC (sluten koppmetod). Det är den lägsta temperatur vid vilken det avger ångor som kan antändas om en flamma passerar över den..
Ångtryck
0,70 mm Hg vid 25 ºC.
Självantändningstemperatur
371 ° C Det är den lägsta temperatur vid vilken den brinner spontant vid atmosfärstryck, utan en extern värmekälla eller flamma..
Densitet
0,9537 g / cm3 vid 20 ºC.
Brytningsindex
1,5582 vid 20 ºC.
Löslighet
I vatten är det mycket lättlösligt: 1 454 mg / L vid 25 ºC.
Fritt löslig i alkohol, kloroform och eter. Lösligt i aceton, bensen och syrehaltiga och klorerade lösningsmedel.
Grundläggande konstant
Kb 11.7, vilket anger hur lätt denna förening accepterar en vätejon från vatten.
Kemiska egenskaper
N, N-dimetylanilin är en basisk förening. Reagerar med ättiksyra för att ge N, N-dimetylaniliniumacetat.
Gruppen -N (CH3)två av N, N-dimetylanilin är en kraftfull aktivator för aromatisk substitution vid positionen för att av bensenringen.
Reagerar med natriumnitrit (NaNOtvåi närvaro av saltsyra (HCl) som bildar p-nitroso-N, N-dimetylanilin. Även med salpetersyra genererar den samma kväveförening i position för att.
När N, N-dimetylanilin reagerar med bensenediazoniumklorid, i ett milt surt medium, produceras en azoförening av typen Ar-N = N-Ar ', där Ar är en aromatisk grupp. Molekyler med azogrupper är starkt färgade föreningar.
Risker
Vid uppvärmning till sönderdelning avger den mycket giftiga anilinångor och kväveoxider NOx.
Det är en brännbar vätska.
Det sönderdelas långsamt i vatten som utsätts för solljus. Nedbryts inte.
Det flyktar från våt mark och vattenytor. Den avdunstar inte från torr mark och rör sig genom den. Ackumuleras inte i fisk.
Det kan absorberas genom huden. Det absorberas också snabbt genom inandning. Mänsklig exponering för N, N-dimetylanilin kan minska syreinnehållet i blodet och resultera i en blåaktig färg på huden..
Akut inandning av denna förening kan leda till negativa effekter på centrala nervsystemet och cirkulationssystemet, med huvudvärk, cyanos och yrsel..
Syntes
Den kan produceras på flera sätt:
- Från anilin och metanol under tryck i närvaro av syrakatalysatorer, såsom HtvåSW4. Sulfat erhålls som omvandlas till basen genom tillsats av natriumhydroxid.
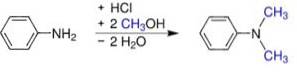
- För en anilinånga och dimetyleter över aktiverad aluminiumoxid.
- Uppvärmning av en blandning av anilin, aniliniumklorid och metanol under tryck och destillering.
Applikationer
I färgämnesindustrin
På grund av egenskapen att reagera med bensenediazoniumklorid för att bilda azoföreningar används N, N-dimetylanilin som mellanprodukt vid tillverkning av färgämnen..
Det är ett råmaterial i syntesen av färgämnena i metylviolettfamiljen.
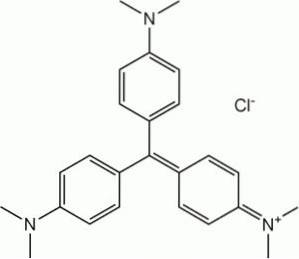
Vid tillverkning av fotohärdbara blandningar
N, N-dimetylanilin är en del av en fotohärdbar blandning som genomgår härdningsreaktionen som ett resultat av hög känslighet för synligt eller nära infrarött ljus, så att den kan användas för bildinspelning eller fotoresistmaterial..
N, N-dimetylanilin är en av komponenterna i blandningen som orsakar sensibilisering för våglängder, på ett sådant sätt att kompositionen härdas med ljus med lågenergivåglängder.
Det uppskattas att rollen för N, N-dimetylanilin sannolikt kommer att undertrycka radikalpolymerisationsavslutningsreaktionen orsakad av syre..
Inom glasfibertillverkning
N, N-dimetylanilin används som en katalytisk härdare i vissa glasfiberhartser.
I syntesen av antibiotika
N, N-dimetylanilin deltar i syntesen av cefalosporiner med utgångspunkt från penicilliner.
Penicillinsulfoxider omvandlas till cefemderivat vid upphettning i närvaro av basiska katalysatorer såsom N, N-dimetylanilin.
Dessa cefalosporiner uppvisar antibakteriell aktivitet mot grampositiva och gramnegativa organismer, liksom mot penicillinresistenta stafylokocker..
Det bör emellertid noteras att N, N-dimetylanilin kvarstår i dessa antibiotika som en orenhet..
Vid katalys av kemiska reaktioner
N, N-dimetylanilin används vid aktivering av olefinpolymerisationskatalysatorer.
Det används tillsammans med pentafluorfenol (C6F5OH) med vilken den bildar den joniska föreningen [HNPhMetvå]+[H (OC6F5)två]-. Denna jonförening har en eller två aktiva protoner som aktiverar katalysatorn baserat på en övergångsmetall.
Dessutom har N, N-dimetylanilin vid tillverkningen av hartser använts som en polymerisationsaccelerator eller promotor för bildandet av polyesterhartser. Dess verkan genererar en snabb härdning av hartset.
I olika applikationer
Det används vid syntes av andra kemiska föreningar, till exempel vanillin, och som en mellanprodukt för farmaceutiska läkemedel.
Det används också som ett lösningsmedel, som ett alkyleringsmedel, som ett stabiliseringsmedel och för att tillverka färger och beläggningar..
Referenser
- S. National Library of Medicine. (2019). N, N-dimetylanilin. Återställd från: pubchem.ncbi.nlm.nih.gov
- Morrison, R.T. och Boyd, R.N. (2002). Organisk kemi. 6: e upplagan. Prentice-Hall.
- (2000). N, N-dimetylanilin. Sammanfattning. Återställd från epa.gov
- Zanaboni, P. (1966). Omättad polyesterhartskomposition med hög stabilitet och snabb härdning vid låga temperaturer med användning av en blandning av dimetylanilin, trietanolamin och difenylamin. USA Patent nr 3 236 915. 22 februari 1966.
- Nudelman, A. och McCaully, R.J. (1977). Förfarande för omläggning av penicilliner till cefalosporiner och mellanliggande sammansättningar därav. USA Patent nr 4 010 156. 1 mars 1977.
- Kouji Inaishi (2001). Fotokörbar komposition. USA Patent nr 6 171 759 Bl. 9 januari 2001.
- Luo, L. et al. (2012). Jonbronsyra. USA Patent nr 8 088 952 B2. 3 januari 2012.


Ingen har kommenterat den här artikeln än.