
Glykosidbindningsegenskaper, typer och nomenklatur
De glykosidbindningar De är de kovalenta bindningarna som uppstår mellan sockerarter (kolhydrater) och andra molekyler, vilka kan vara andra monosackarider eller andra molekyler av olika natur. Dessa länkar möjliggör existensen av flera grundläggande komponenter för livet, inte bara i bildandet av reservbränslen och strukturella element, utan också av informationsbärande molekyler som är nödvändiga för cellulär kommunikation..
Bildandet av polysackarider beror i grunden på etableringen av glykosidbindningar mellan de fria alkohol- eller hydroxylgrupperna i de enskilda monosackaridenheterna..
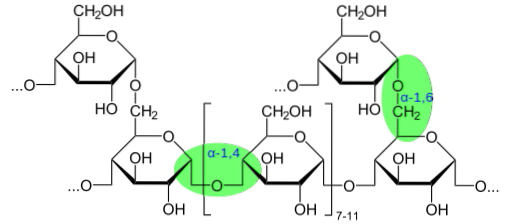
Vissa komplexa polysackarider innehåller emellertid modifierade sockerarter som är bundna till små molekyler eller grupper såsom amino, sulfat och acetyl genom glukosidbindningar, och som inte nödvändigtvis innebär frisättning av en vattenmolekyl genom en kondensationsreaktion. Dessa modifieringar är mycket vanliga i glykanerna som finns i den extracellulära matrisen eller glykokalyxen..
Glykosidbindningar förekommer i flera cellulära sammanhang, inklusive föreningen av den polära huvudgruppen av vissa sfingolipider, väsentliga beståndsdelar i cellmembranen i många organismer och bildandet av glykoproteiner och proteoglykaner..
Viktiga polysackarider såsom cellulosa, kitin, agar, glykogen och stärkelse skulle inte vara möjliga utan glykosidbindningar. På samma sätt är proteinglykosylering, som förekommer i det endoplasmiska retikulumet och i Golgi-komplexet, av yttersta vikt för aktiviteten hos många proteiner..
Många oligo- och polysackarider fungerar som glukosreservoarer, som strukturella komponenter eller som lim för cellfästning i vävnader..
Förhållandet mellan glykosidbindningar i oligosackarider är analogt med det för peptidbindningar i polypeptider och fosfodiesterbindningar i polynukleotider, med skillnaden att det finns större mångfald i glykosidbindningar.
Artikelindex
- 1 Funktioner
- 1.1 Bildning av glykosidbindningen
- 1.2 Hydrolys av glykosidbindningen
- 1.3 Mångfald
- 2 typer
- 2.1 O-glukosidbindningar
- 2.2 N-glukosidbindningar
- 2.3 Andra typer av glykosidbindningar
- 3 Nomenklatur
- 4 Referenser
Egenskaper
Glykosidbindningar är mycket mer varierade än deras analoger i proteiner och nukleinsyror, eftersom i princip två sockermolekyler kan förena varandra på många sätt, eftersom de har flera -OH-grupper som kan delta i bildandet av länken.
Vidare ger isomererna av monosackarider, det vill säga en av de två riktningarna som hydroxylgruppen kan ha i den cykliska strukturen relativt det anomera kolet, en ytterligare nivå av mångfald..
Isomerer har olika tredimensionella strukturer, liksom olika biologiska aktiviteter. Cellulosa och glykogen består av upprepade D-glukosenheter men skiljer sig åt i typen av glykosidbindning (α1-4 för glykogen och β1-4 för cellulosa) och har därför olika egenskaper och funktioner..
Precis som polypeptider har en polaritet med en N- och en C-ände, och polynukleotider har 5 'och 3' ändar, har oligo- eller polysackarider en polaritet definierad av de reducerande och icke-reducerande ändarna.
Den reducerande änden har ett fritt anomert centrum som inte bildar en glykosidbindning med en annan molekyl, vilket bibehåller aldehydens kemiska reaktivitet.
Den glykosidiska bindningen är den mest flexibla regionen i en oligo- eller polysackariddel, eftersom den strukturella sadelkonformationen för enskilda monosackarider är relativt stel..
Bildning av glykosidbindningen
Den glykosidiska bindningen kan förena två monosackaridmolekyler genom det anomera kolet i den ena och hydroxylgruppen i den andra. Det vill säga hemiacetalgruppen i ett socker reagerar med alkoholens grupp i ett annat för att bilda en acetal.
Generellt sker bildandet av dessa bindningar genom kondensationsreaktioner, där en vattenmolekyl frigörs med varje bindning som bildas..
I vissa reaktioner lämnar syre emellertid inte sockermolekylen som vatten utan som en del av difosfatgruppen i en uridindifosfatnukleotid..
Reaktionerna som ger upphov till glykosidbindningarna katalyseras av en klass av enzymer som kallas glykosyltransferaser. De bildas mellan ett kovalent modifierat socker genom tillsats av en fosfatgrupp eller en nukleotid (glukos 6-fosfat, UDP-galaktos, till exempel) som binder till den växande polymerkedjan.
Hydrolys av glykosidbindningen
Glykosidbindningar kan lätt hydrolyseras i svagt sura miljöer, men de är ganska resistenta mot alkaliska miljöer..
Den enzymatiska hydrolysen av glykosidbindningarna förmedlas av enzymer som kallas glykosidas. Många däggdjur har inte dessa enzymer för nedbrytning av cellulosa, så de kan inte extrahera energi från denna polysackarid, trots att de är en väsentlig fiberkälla.
Ruminanter som kor, till exempel, har bakterier associerade med tarmarna som producerar enzymer som kan bryta ner cellulosan de intar, vilket gör dem kapabla att dra nytta av den energi som bevaras i växtvävnader..
Enzymet lysozym, producerat i tårarna i ögat och av vissa bakterievirus, kan förstöra bakterier tack vare dess hydrolytiska aktivitet, som bryter glykosidbindningen mellan N-acetylglukosamin och N-acetylmuraminsyra i cellväggen av bakterier..
Mångfald
Oligosackarider, polysackarider eller glykaner är mycket olika molekyler och detta beror på de många sätt som monosackarider kan binda ihop för att bilda strukturer av högre ordning.
Denna mångfald baseras på det faktum, som nämnts ovan, att sockerarter har hydroxylgrupper som tillåter olika bindningsregioner, och att bindningar kan uppstå mellan de två möjliga stereoisomererna med avseende på det anomera kolet i sockret (α eller β)..
Glykosidbindningar kan bildas mellan ett socker och vilken hydroxiförening som helst, såsom alkoholer eller aminosyror.
Dessutom kan en monosackarid bilda två glykosidbindningar, så att den kan fungera som en förgreningspunkt, vilket introducerar potentiell komplexitet i strukturen av glykaner eller polysackarider i celler..
Typer
När det gäller typer av glykosidbindningar kan två kategorier differentieras: glykosidbindningarna mellan monosackarider som utgör oligo- och polysackarider och de glykosidbindningar som förekommer i glykoproteiner eller glykolipider, som är proteiner eller lipider med delar av kolhydrater.
O-glukosidbindningar
O-glykosidbindningar uppträder mellan monosackarider, de bildas genom reaktionen mellan hydroxylgruppen i en sockermolekyl och det anomera kolet i en annan.
Disackarider är en av de vanligaste oligosackariderna. Polysackarider har mer än 20 monosackaridenheter kopplade ihop linjärt och har ibland flera grenar..
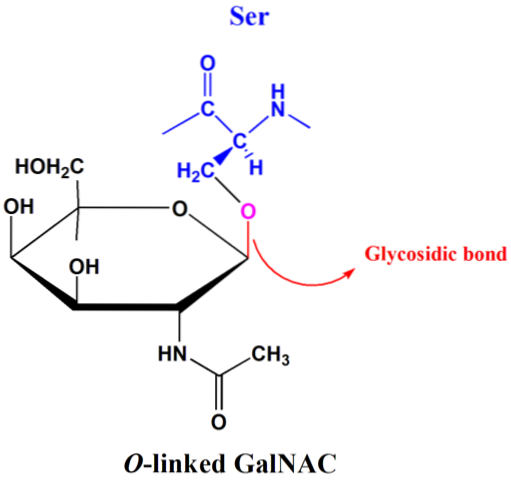
I disackarider såsom maltos, laktos och sackaros är den vanligaste glykosidbindningen den O-glukosidiska typen. Dessa bindningar kan förekomma mellan kol och -OH i a- eller β-isomera former..
Bildningen av glukosidbindningarna i oligo- och polysackarider beror på den stereokemiska beskaffenheten hos sockerarterna som förenas, liksom på deras antal kolatomer. I allmänhet förekommer linjära bindningar mellan kol 1 och 4 eller 1 och 6 för sockerarter med 6 kolatomer.
Det finns två huvudtyper av O-glykosider som, beroende på nomenklaturen, definieras som a och P eller 1,2-cis och 1.2-trans-glykosider.
Rester 1,2-cis glykosylerade, a-glykosider för D-glukos, D-galaktos, L-fukos, D-xylos eller P-glykosider för D-mannos, L-arabinos; liksom 1,2-trans (β-glykosider för D-glukos, D-galaktos och α-glykosider för D-mannos, etc.), är av stor betydelse för många naturliga komponenter.
O-glykosylering
En av de vanligaste modifieringarna efter translation är glykosylering, som består av tillsatsen av en kolhydratdel till en växande peptid eller protein. Slemhinnor, sekretoriska proteiner, kan innehålla stora mängder oligosackaridkedjor kopplade till O-glukosidbindningar..
O-glykosyleringsprocessen sker i Golgi-komplexet av eukaryoter och består av bindningen av proteiner till kolhydratdelen genom en glykosidbindning mellan -OH-gruppen i en aminosyrarest av serin eller treonin och det anomera kolet av socker..
Bildningen av dessa bindningar mellan kolhydrater och hydroxiprolin och hydroxylisinrester och med fenolgruppen av tyrosinrester har också observerats..
N-glykosidbindningar
N-glykosidbindningar är de vanligaste bland glykosylerade proteiner. N-glykosylering förekommer huvudsakligen i det endoplasmatiska retikulumet av eukaryoter, med efterföljande modifieringar som kan förekomma i Golgi-komplexet.
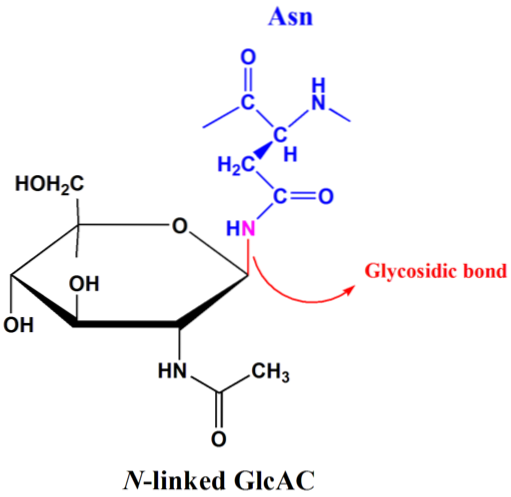
N-glykosylering beror på närvaron av konsensus-sekvensen Asn-Xxx-Ser / Thr. Den glykosidiska bindningen uppträder mellan amidkvävet i sidokedjan av asparaginresterna och det anomera kolet i sockret som binder till peptidkedjan..
Bildningen av dessa bindningar under glykosylering beror på ett enzym som kallas oligosakaryltransferas, vilket överför oligosackariderna från ett dolikolfosfat till amidkvävet i asparaginresterna..
Andra typer av glykosidbindningar
S-glukosidbindningar
De förekommer också mellan proteiner och kolhydrater, de har observerats mellan peptider med N-terminala cysteiner och oligosackarider. Peptider med denna typ av bindning isolerades initialt från proteiner i human urin och erytrocyter bundna till glukosoligosackarider..
C-glukosidbindningar
De observerades för första gången som en post-translationell modifiering (glykosylering) i en tryptofanrest i RNas 2 närvarande i human urin och i RNas 2 av erytrocyter. En mannos binder till kolet vid position 2 i indolkärnan i aminosyran genom en C-glukosidbindning.
Nomenklatur
Uttrycket glykosid används för att beskriva vilket socker vars anomera grupp ersätts med en grupp -OR (O-glykosider), -SR (tioglykosider), -SeR (selenoglykosider), -NR (N-glykosider eller glukosaminer) eller till och med -CR (C-glukosider).
De kan namnges på tre olika sätt:
(1) ersättning av terminalen "-o" för namnet på motsvarande cykliska form av monosackariden med "-ido" och innan man skriver, som ett annat ord, namnet på den substituerande R-gruppen.
(2) användning av termen "glykosyloxi" som ett prefix av monosackaridnamnet.
(3) använder termen ELLER-glykosyl, N-glykosyl, S-glykosyl eller C-glykosyl som ett prefix för namnet på hydroxiföreningen.
Referenser
- Bertozzi, C. R. och Rabuka, D. (2009). Strukturell grund för glykamångfald. I A. Varki, R. Cummings och J. Esko (red.), Essentials of Glycobiology (2: a upplagan). New York: Cold Spring Harbor Laboratory Press. Hämtad från www.ncbi.nlm.nih.gov
- Biermann, C. (1988). Hydrolys och andra klyvningar av glykosidbindningar i polysackarider. Framsteg inom kolhydratkemi och biokemi, 46, 251-261.
- Demchenko, A. V. (2008). Handbok för kemisk glykosylering: framsteg i stereoselektivitet och terapeutisk relevans. Wiley-VCH.
- Lodish, H., Berk, A., Kaiser, C. A., Krieger, M., Bretscher, A., Ploegh, H.,… Martin, K. (2003). Molekylär cellbiologi (5: e upplagan). Freeman, W. H. & Company.
- Nelson, D. L., & Cox, M. M. (2009). Lehninger Principer för biokemi. Omega-utgåvor (5: e upplagan).
- Nomenklatur för kolhydrater (rekommendationer 1996). (nitton nittiosex). Hämtad från www.qmul.ac.uk
- Soderberg, T. (2010). Organisk kemi med biologisk betoning, volym I. Kemisk fakultet (Vol. 1). Minnesota: University of Minnesota Morris Digital Well. Hämtad från www.digitalcommons.morris.umn.edu
- Taylor, C. M. (1998). Glykopeptider och glykoproteiner: Fokusera på glykosidbindningen. Tetraeder, 54, 11317-11362.



Ingen har kommenterat den här artikeln än.