
Kvävefixering biotiska och abiotiska processer

De Fixering av kväve Det är en uppsättning biologiska och icke-biologiska processer som producerar kemiska former av kväve som är tillgängliga för levande varelser. Kväve tillgänglighet kontrollerar på ett viktigt sätt hur ekosystem och global biogeokemi fungerar, eftersom kväve är en faktor som begränsar den primära nettoproduktiviteten i mark- och vattenlevande ekosystem..
I vävnaderna hos levande organismer är kväve en del av aminosyror, enheter av strukturella och funktionella proteiner som enzymer. Det är också ett viktigt kemiskt element i sammansättningen av nukleinsyror och klorofyll..
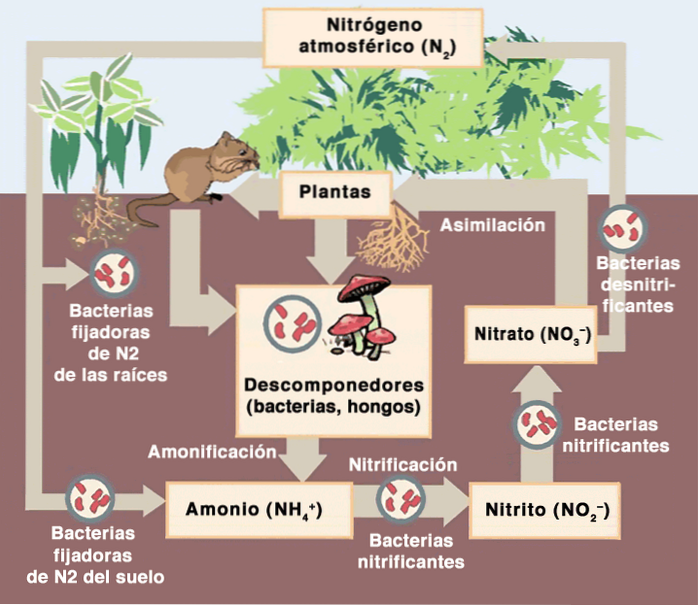
Dessutom inträffar de biogeokemiska reaktionerna av kolreduktion (fotosyntes) och koloxidation (andning) genom förmedling av kväveinnehållande enzymer, eftersom de är proteiner.
I de kemiska reaktionerna i den biogeokemiska cykeln av kväve ändrar detta element dess oxidationstillstånd från noll till Ntvå, en 3- i NH3, 3+ i NOtvå - och NH4+ , och 5+ i NO3 -.
Flera mikroorganismer utnyttjar den energi som genereras i dessa kväveoxidreduktionsreaktioner och använder den i sina metaboliska processer. Det är dessa mikrobiella reaktioner som tillsammans driver den globala kvävecykeln..
Den vanligaste kemiska kväveformen på planeten är gasformigt molekylärt diatomiskt kväve Ntvå, vilket utgör 79% av jordens atmosfär.
Det är också den minst reaktiva kemiska typen av kväve, praktiskt taget inert, mycket stabil, på grund av den tredubbla bindningen som förenar båda atomerna. Av denna anledning är kvävet som är så rikligt i atmosfären inte tillgängligt för de allra flesta levande varelser..
Kväve i kemiska former som är tillgängliga för levande varelser erhålls genom "kvävefixering". Kvävefixering kan ske på två huvudsakliga sätt: abiotiska former av fixering och biotiska former av fixering..
Artikelindex
- 1 Abiotiska former av kvävefixering
- 1.1 Elektriska stormar
- 1.2 Bränner fossila bränslen
- 1.3 Biomassaförbränning
- 1.4 Kväveutsläpp från jorderosion och bergsvittring
- 2 Biotiska former av kvävefixering
- 2.1 Fritt levande eller symbiotiska mikroorganismer
- 2.2 Mekanismer för att hålla kvävesystemet aktivt
- 2.3 Biotisk kvävefixering med fritt levande mikroorganismer
- 2.4 Energi som krävs under N2-fixeringsreaktionen
- 2.5 Enzymkvävekomplexet och syre
- 2.6 Biotisk kvävefixering av mikroorganismer i symbiotiskt liv med växter
- 3 Referenser
Abiotiska former av kvävefixering
Elektriska stormar

Blixtarna eller "blixtarna" som produceras under stormar är inte bara buller och ljus; de är en kraftfull kemisk reaktor. På grund av blixtens verkan produceras kväveoxider NO och NO under stormar.två, generiskt kallad NEJx.
Dessa elektriska urladdningar, observerade som blixtnedslag, genererar förhållanden med höga temperaturer (30 000ellerC) och höga tryck, som främjar den kemiska kombinationen av syre Otvå och kväve Ntvå från atmosfären och producerar kväveoxider NOx.
Denna mekanism har ett mycket lågt bidrag till den totala kvävefixeringshastigheten, men den är den viktigaste bland abiotiska former..
Bränner fossila bränslen
Det finns ett antropogent bidrag till produktionen av kväveoxider. Vi har redan sagt att den starka trippelbindningen av kvävemolekylen Ntvå, kan bara bryta under extrema förhållanden.
Förbränningen av fossila bränslen som härrör från petroleum (inom industrier och kommersiella och privata transporter, sjöfart, luft och land) ger enorma mängder NO-utsläpp.x till atmosfären.
NtvåEller släpps ut vid förbränning av fossila bränslen, det är en kraftfull växthusgas som bidrar till den globala uppvärmningen av planeten..
Biomassa brinner
Det finns också ett bidrag av kväveoxider NOx genom att bränna biomassa i området med högsta temperaturen i flamman, till exempel i skogsbränder, användning av ved för uppvärmning och matlagning, förbränning av organiskt avfall och all användning av biomassa som källa till värmeenergi.
Kväveoxider NOx som släpps ut i atmosfären genom antropogena vägar, orsakar allvarliga miljöföroreningsproblem, såsom fotokemisk smog i stads- och industrimiljöer, och viktiga bidrag till surt regn.
Kväveutsläpp från jorderosion och bergsvittring
Jorderosion och kvävrik berggrundsförvitring utsätter mineraler för elementen som kan frigöra kväveoxider. Bergsvittring uppstår på grund av exponering för miljöfaktorer, orsakade av fysiska och kemiska mekanismer som verkar tillsammans..
Tektoniska rörelser kan fysiskt utsätta kväverika bergarter för elementen. Därefter orsakar utfällningen av surt regn genom kemiska metoder kemiska reaktioner som frigör NOx, både från denna typ av stenar och från marken.
Det finns ny forskning som tilldelar 26% av planetens totala biotillgängliga kväve till dessa mekanismer för jorderosion och bergsvittring..
Biotiska former av kvävefixering
Vissa bakteriemikroorganismer har mekanismer som kan bryta trippelbindningen av Ntvå och producera NH-ammoniak3, som lätt omvandlas till ammoniumjon, NH4+ metaboliserbar.
Fritt levande eller symbiotiska mikroorganismer
Formerna av kvävefixering med mikroorganismer kan förekomma genom fritt levande organismer eller genom organismer som lever i symbiotiska föreningar med växter..
Även om det finns stora morfologiska och fysiologiska skillnader mellan kvävefixerande mikroorganismer, är fixeringsprocessen och kvävenasenzymsystemet som används av alla dessa mycket lika..
Kvantitativt är biotisk kvävefixering genom dessa två mekanismer (fritt liv och symbios) det viktigaste globalt..
Mekanismer för att hålla kvävesystemet aktivt
Kvävebindande mikroorganismer har strategiska mekanismer för att hålla deras kvävegenas enzymatiska system aktivt..
Dessa mekanismer inkluderar andningsskydd, konformationskemiskt skydd, reversibel hämning av enzymaktivitet, ytterligare syntes av ett alternativt kvägenas med vanadin och järn som kofaktorer, skapande av diffusionsbarriärer för syre och rumslig separation av kvävegen.
Vissa har mikroaerofilitet, såsom kemotrofa bakterier i släktet Azospirilium, Aquaspirillum, Azotobacter, Beijerinkia, Azomonas, Derxia, Crynebacterium, Rhizobium, Agrobacterium, Thiobacillus och fototrofer av genrerna Gleocapsa, Anabaena, Spirulina, Nostoc, Oscillatoria, Calothrix, Lingbya.
Andra presenterar fakultativ anaerobios, såsom de kemostrofiska släktena: Klebsiella, Citrobacter, Erwinia, Bacillus, Propionibacterium och fototrofer av genrerna Rhodospirillum, Rhodopsuedomonas.
Biotisk kvävefixering med fritt levande mikroorganismer
Kvävebindande mikroorganismer som lever i jorden i fri (asymbiotisk) form är i grunden arkebakterier och bakterier.
Det finns flera typer av bakterier och cyanobakterier som kan omvandla atmosfäriskt kväve, Ntvå, i ammoniak, NH3. Enligt den kemiska reaktionen:
Ntvå+8H++8e-+16 ATP → 2 NH3+Htvå+16 ADP + 16Pi
Denna reaktion kräver förmedling av kvävenasenzymsystemet och en kofaktor, vitamin B12. Dessutom förbrukar denna kvävefixeringsmekanism mycket energi, är endoterm och kräver 226 Kcal / mol Ntvå; det innebär att det har en hög metabolisk kostnad, varför det måste kopplas till ett system som producerar energi.
Energi som krävs under N-fixeringsreaktionentvå
Energin för denna process erhålls från ATP, som kommer från oxidativ fosforylering kopplad till elektrontransportkedjan (som använder syre som den slutliga elektronacceptorn)..
Processen att reducera molekylärt kväve till ammoniak minskar också väte i protonformen H+ till molekylärt väte Htvå.
Många kvävesensystem har kopplat ett väteåtervinningssystem förmedlat av hydrogenasenzymet. Kvävebindande cyanobakterier kopplar fotosyntes till kvävefixering.
Enzymnitrogenas-komplexet och syre
Nitrogenasenzymkomplexet har två komponenter, komponent I, dinitrogenas med molybden och järn som kofaktorer (som vi kommer att kalla Mo-Fe-protein), och komponent II, dinitrogenasreduktas med järn som kofaktor (Fe-protein).
Elektronerna som är involverade i reaktionen doneras först till komponent II och senare till komponent I, där kvävereduktionen sker..
För att överföringen av elektroner från II till I ska ske måste Fe-proteinet bindas till ett Mg-ATP vid två aktiva ställen. Denna förening genererar en konformationsförändring i Fe-proteinet. Ett överskott av syre kan ge en annan konformationsförändring i Fe-proteinet ogynnsamt, eftersom det avbryter sin elektronmottagande kapacitet.
Detta är anledningen till att kvävegenzymkomplexet är mycket mottagligt för närvaron av syre över tolerabla koncentrationer och att vissa bakterier utvecklar mikroaerofila livsformer eller fakultativ anaerobios.
Bland de fritt levande kvävebindande bakterierna kan nämnas kemotroferna som tillhör släktena Clostridium, Desulfovibrio, Desulfotomaculum, Methanosarcina, och genrenas fototrofer Chromatium, Thiopedia, Ectothiordospira, bland annat.
Biotisk kvävefixering av mikroorganismer i symbiotiskt liv med växter
Det finns andra kvävebindande mikroorganismer som kan skapa symbiotiska föreningar med växter, särskilt med baljväxter och gräs, antingen i form av ektosymbios (där mikroorganismen ligger utanför växten) eller endosymbios (där mikroorganismen lever i celler eller växtens intercellulära utrymmen).
Det mesta av kvävet som fixeras i markbundna ekosystem kommer från de symbiotiska föreningarna av släktbakterier Rhizobium, Bradyrhizobium, Sinorhizobium, Azorhizobium, Allorhizoium Y Mesorhizobium, med baljväxter.
Det finns tre intressanta typer av kvävefixerande symbioser: associerande rhizocenoser, system med cyanobakterier som symbionter och mutualistiska endorizobioser..
Rhizocenosis
I associerande rhizocenosliknande symbioser bildas inga specialiserade strukturer i växternas rötter.
Exempel på denna typ av symbios upprättas mellan majsplantor (Zea majs) och sockerrör (Saccharum officinarum) med Gluconacetobacter, Azoarcus, Azospirillum Y Herbaspirillum.
I rhizocenos använder de kvävebindande bakterierna växts rotutsöndring som näringsmedium och koloniserar rotcortexens intercellulära utrymmen..
Cyanobakterier symbionter
I system där cyanobakterier deltar har dessa mikroorganismer utvecklat speciella mekanismer för samexistens av anoxisk kvävefixering och deras syresatta fotosyntes..
Till exempel i Gleothece Y Synechococcus, de är tillfälligt separerade: de utför fotosyntes dagtid och kvävefixering på natten.
I andra fall finns det rumslig separation av båda processerna: kväve fixeras i grupper av differentierade celler (heterocyster), där fotosyntes inte utförs.
Kvävebindande symbiotiska föreningar av släktets cyanobakterier Nostoc med icke-vaskulära växter (antóceras), som i håligheter i Nothocerus endiviaefolius, med liverworts Gakstroemia magellanica och Chyloscyphus obvolutus i ektosymbios separat, med bryophytes (bildar lavar i mossarizoider) och med högre angiospermväxter, till exempel med de 65 fleråriga örterna i släktet Gunnnera.
Till exempel har den kvävebindande symbiotiska föreningen av cyanobakterier observerats Anabaena med en bryophyte, icke-vaskulär växt, på löv av den lilla ormbunken Azolla anabaenae.
Endorizobios
Som exempel på endorhizobios kan vi nämna föreningen kallad actinorhiza som upprättas mellan Frankia och några träiga växter som casuarina (Casuarina cunninghamiana) Y alAlnus glutinosa) och föreningen Rhizobium-baljväxter.
De flesta arter i familjen Leguminosae, bilda symbiotiska föreningar med bakterie Rhizobium och denna mikroorganismhar evolutionär specialisering i att överföra kväve till växten.
I rötterna av växter associerade med Rhizobium, de så kallade radikala nodulerna dyker upp, den plats där kvävefixering äger rum.
I baljväxter Sesbania Y Aechynomene, dessutom bildas knölar på stjälkarna.
- Kemiska signaler
Det finns ett utbyte av kemiska signaler mellan symbioten och värden. Växter har befunnits utstråla vissa typer av flavonoider som inducerar uttryck av nodgener i Rhizobium, som producerar noduleringsfaktorer.
Nodulationsfaktorer genererar modifieringar i rothåren, bildande av en infektionskanal och celldelning i rotbarken, vilket främjar bildandet av nodulen.
Några exempel på kvävebindande symbios mellan högre växter och mikroorganismer visas i följande tabell..
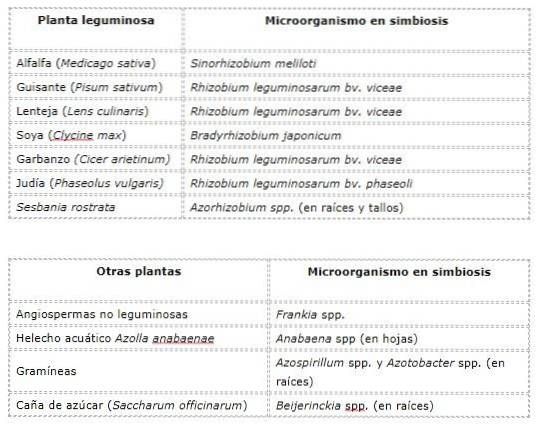
Mykorrhizobios
Dessutom finns det i de flesta ekosystem kvävebindande mycorrhizal svampar som tillhör phyla Glomeromycota, Basidiomycota och Ascomycota.
Mycorrhizal svampar kan leva i ektosymbios, bilda en hyphal mantel runt de fina rötterna hos vissa växter och sprida ytterligare hyfer i jorden. Även i många tropiska områden är växter värd för mycorrhizae i endosymbios, vars hyfer tränger in i rotceller.
Det är möjligt att en svamp bildar mycorrhizae med flera växter samtidigt, i vilket fall inbördes relationer upprättas mellan dem; eller att den mykorrhizala svampen parasiteras av en växt som inte fotosyntetiserar, mycoheterotrofisk, såsom de i släktet Monotrope. Flera svampar kan också skapa symbios med en enda växt samtidigt.
Referenser
- Inomura, K., Bragg, J. och Follows, M. (2017). En kvantitativ analys av de direkta och indirekta kostnaderna för kvävefixering. ISME Journal. 11: 166-175.
- Masson-Bovin, C. och Sachs, J. (2018). Symbiotisk kvävefixering genom rhizobia - rötterna till en framgångshistoria. Växtbiologi. 44: 7-15. doi: 10.1016 / j.pbi.2017.12.001
- Menge, D.N.L., Levin, S.A. och Hedin, L.O. (2009). Fakultativ mot obligatorisk kvävefixeringsstrategi och deras ekosystemkonsekvenser. Den amerikanska naturforskaren. 174 (4) doi: 10.1086 / 605377
- Newton, W.E. (2000). Kvävefixering i perspektiv. I: Pedrosa, F.O. Redaktör. Kvävefixering från molekyler till grödans produktivitet. Nederländerna: Kluwer Academic Publishers. 3-8.
- Pankievicz; V.C.S., gör Amaral; F.P., Santos, K.D.N., Agtuca, B., Xu, Y., Schultes, M.J. (2015). Robust biologisk kvävefixering i en modellgräs-bakteriell förening. Plant Journal. 81: 907-919. doi: 10.1111 / tpj.12777.
- Wieder, W.R., Cleveland, C.C., Lawrence, D. och Bonau, G.B. (2015). Effekter av modellens strukturella osäkerhet på koldioxidcykelprojektioner: biologisk kvävefixering som en studie. Miljöforskningsbrev. 10 (4): 1-9. doi: 10.1088 / 1748-9326 / 10/4/044016



Ingen har kommenterat den här artikeln än.