
Glutationegenskaper, struktur, funktioner, biosyntes
De glutation (GSH) är en liten tripeptidmolekyl (med endast tre aminosyrarester) icke-protein som deltar i många biologiska fenomen, såsom enzymatisk mekanik, makromolekylsbiosyntes, mellanliggande metabolism, syretoxicitet, intracellulär transport etc..
Denna lilla peptid, närvarande i djur, växter och vissa bakterier, anses vara en "buffert" oxido-reducerande, eftersom det är en av de viktigaste föreningarna med låg molekylvikt som innehåller svavel och saknar toxicitet associerad med cysteinrester.
Vissa sjukdomar hos människor har associerats med bristen på specifika enzymer av glutationmetabolism, och detta beror på dess många funktioner för att upprätthålla kroppshomeostas.
Undernäring, oxidativ stress och andra patologier som lider av människor kan bevisas som en drastisk minskning av glutation, vilket är anledningen till att det ibland är en bra indikator på kroppssystemens hälsa..
För växter är glutation på samma sätt en viktig faktor för deras tillväxt och utveckling, eftersom den också utför funktioner i flera biosyntetiska vägar och är nödvändig för cellulär avgiftning och intern homeostas, där den fungerar som en kraftfull antioxidant..
Artikelindex
- 1 Funktioner
- 2 Struktur
- 3 funktioner
- 3.1 Koenzym
- 3.2 Lagring av cystein
- 3.3 Proteinvikning
- 3.4 Funktion i erytrocyter
- 3.5 Xenobiotisk metabolism
- 3.6 Oxidativt tillstånd hos celler
- 4 Biosyntes
- 4.1 Reducerad glutation (GSH)
- 4.2 Oxiderad glutation (GSSG)
- 5 Fördelar med intaget
- 5.1 Cancer
- 5.2 HIV
- 5.3 Muskelaktivitet
- 5.4 Leverpatologier
- 5.5 Antioxidant
- 5.6 "Absorption"
- 6 Biverkningar
- 7 Referenser
Egenskaper
De första studierna som gjordes i relation till glutationens subcellulära läge visade att det finns i mitokondrierna. Senare observerades det också i regionen som motsvarar kärnmatrisen och i peroxisomer.
För närvarande är det känt att det fack där koncentrationen är mest rikligt finns i cytosolen, eftersom det produceras aktivt där och transporteras till andra cellulära fack såsom mitokondrierna..
I däggdjursceller ligger glutationskoncentrationen i millimolområdet, medan dess reducerade form (GSH) i blodplasma finns i mikromolära koncentrationer..
Denna intracellulära koncentration liknar koncentrationen av glukos, kalium och kolesterol, viktiga element för cellulär struktur, funktion och metabolism..
Vissa organismer har analoga eller olika glutationmolekyler. Protozoan parasiter som påverkar däggdjur har en form som kallas "trypanothion" och i vissa bakterier ersätts denna förening med andra svavelmolekyler såsom tiosulfat och glutamylcystein..
Vissa växtarter har, förutom glutation, homologa molekyler som har andra rester än glycin vid den C-terminala änden (homoglutation) och som kännetecknas av att de har funktioner som liknar de i tripeptiden i fråga..
Trots förekomsten av andra föreningar som liknar glutation i olika organismer är detta en av de "tioler" som finns i den högsta koncentrationen intracellulärt..
Det höga förhållandet som normalt finns mellan den reducerade formen (GSH) och den oxiderade formen (GSSG) av glutation är ett annat kännetecken för denna molekyl..
Strukturera
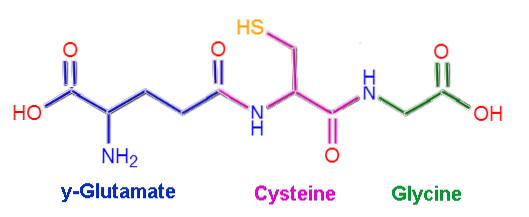
Glutation eller L-γ-glutamyl-L-cysteinyl-glycin, som namnet antyder, består av tre aminosyrarester: L-glutamat, L-cystein och glycin. Cystein- och glycinrester är sammankopplade genom vanliga peptidbindningar, det vill säga mellan a-karboxylgruppen i en aminosyra och a-aminogruppen i den andra..
Bindningen som uppstår mellan glutamat och cystein är emellertid inte typisk för proteiner, eftersom den uppträder mellan y-karboxyldelen av R-gruppen av glutamat och a-aminogruppen i cystein. Kallas y-bindning..
Denna lilla molekyl har en molmassa på drygt 300 g / mol och närvaron av y-bindningen verkar vara avgörande för denna peptids immunitet mot verkan av många aminopeptidasenzymer..
Funktioner
Som nämnts är glutation ett protein som deltar i många cellulära processer hos djur, växter och vissa prokaryoter. I denna mening är dess allmänna deltagande i:
-Processerna för proteinsyntes och nedbrytning
-Bildandet av DNA-ribonukleotidprekursorer
-Reglering av aktiviteten hos vissa enzymer
-Skydd av celler i närvaro av reaktiva syrearter (ROS) och andra fria radikaler
-Signaltransduktion
-Genetiskt uttryck och i
-Apoptos eller programmerad celldöd
Koenzym
Glutation har också bestämts att fungera som ett koenzym i många enzymatiska reaktioner, och den delen av dess betydelse är relaterad till dess förmåga att transportera aminosyror i form av y-glutamylaminosyror intracellulärt..
Glutation som kan lämna cellen (vilket den gör i sin reducerade form) kan delta i oxidationsreduktionsreaktioner i närheten av plasmamembranet och den omgivande cellmiljön, vilket skyddar celler från skador mot olika klasser av oxidationsmedel.
Förvaring av cystein
Denna tripeptid fungerar också som en källa för cysteinlagring och bidrar till upprätthållandet av det reducerade tillståndet för sulfhydrylgrupperna i proteinerna inuti cellen och ferrotillståndet för hemgruppen av proteinerna som innehåller nämnda kofaktor..
Proteinvikning
När det deltar i proteinvikning verkar det ha en viktig funktion som ett reduktionsmedel för disulfidbryggor som har bildats felaktigt i proteinstrukturer, vilket vanligtvis beror på exponering för oxidationsmedel såsom syre, väteperoxid, peroxynitrit och vissa superoxider.
Erytrocytfunktion
I erytrocyter bidrar reducerad glutation (GSH) producerad av enzymet glutationreduktas, som använder NADPH producerad av pentosfosfatvägen, till avlägsnande av väteperoxid genom reaktionen katalyserad av ett annat enzym: glutationperoxidas, som producerar vatten och oxiderat glutation (GSSG).
Nedbrytningen av väteperoxid och därmed förhindrandet av dess ansamling i erytrocyterna förlänger livscykeln för dessa celler, eftersom det undviker oxidationsskador som kan uppstå i cellmembranet och som kan sluta i hemolys..
Xenobiotisk metabolism
Glutation är också en viktig spelare i ämnesomsättningen av xenobiotika tack vare effekten av glutation-S-transferasenzymer som genererar glutationkonjugat som sedan kan metaboliseras intracellulärt..
Det är klokt att komma ihåg att termen "främlingsfientligt" används för att hänvisa till läkemedel, miljöföroreningar och kemiska cancerframkallande ämnen som en organism utsätts för..
Oxidativt tillstånd hos celler
Eftersom glutation finns i två former, en reducerad och en oxiderad, bestämmer förhållandet mellan de två molekylerna cellernas redoxtillstånd. Om förhållandet GSH / GSSG är större än 100 anses cellerna friska, men om det är nära 1 eller 10 kan det vara en indikator på att cellerna är i ett tillstånd av oxidativ stress.
Biosyntes
Glutationstripeptiden syntetiseras inuti celler, både i växter och djur, genom inverkan av två enzymer: (1) γ-glutamylcysteinsyntas och (2) glutation-syntetas (GSH-syntetas), medan dess nedbrytning eller "sönderdelning" beror på verkan av enzymet y-glutamyltranspeptidas.
I växtorganismer kodas var och en av enzymerna av en enda gen och defekter i något av proteinerna eller deras kodande gener kan orsaka dödlighet i embryon.
Hos människor, som hos andra däggdjur, är levern den huvudsakliga platsen för glutation-syntes och export, särskilt i leverceller (hepatocyter) som omger de venösa kanalerna som transporterar blod och andra ämnen till och från organet i fråga..
Syntes de novo glutation, dess regenerering eller återvinning, kräver energi från ATP för att uppstå.
Reducerat glutation (GSH)
Reducerat glutation härrör från aminosyrorna glycin, glutamat och cystein, som redan nämnts, och dess syntes börjar med aktiveringen (med användning av ATP) av y-karboxylgruppen av glutamat (av R-gruppen) för att bilda en mellanliggande acylfosfat, som attackeras av a-aminogruppen i cystein.
Denna första två aminosyrakondensationsreaktion katalyseras av y-glutamylcysteinsyntetas och påverkas vanligtvis av den intracellulära tillgängligheten av aminosyrorna glutamat och cystein..
Den sålunda bildade dipeptiden kondenseras därefter med en glycinmolekyl tack vare GSH-syntetas verkan. Under denna reaktion sker en aktivering med ATP av a-karboxylgruppen i cystein också för att bilda ett acylfosfat och sålunda gynna reaktionen med glycinresten..
Oxiderad glutation (GSSG)
När reducerat glutation deltar i oxidationsreduktionsreaktioner består den oxiderade formen faktiskt av två glutationmolekyler kopplade ihop genom disulfidbroar; det är av denna anledning som den oxiderade formen förkortas med initialerna "GSSG".
Bildningen av den oxiderade typen av glutation beror på ett enzym som kallas glutationperoxidas eller GSH-peroxidas, vilket är ett peroxidas som innehåller en selenocystein (en cysteinrest som istället för att ha en svavelatom har en selenatom) på plats aktiv.
Omvandlingen mellan de oxiderade och reducerade formerna sker tack vare deltagandet av ett GSSG-reduktas eller glutationreduktas, som använder NAPDH för att katalysera reduktionen av GSSG i närvaro av syre, med samtidig bildning av väteperoxid.
Fördelar med intaget
Glutation kan administreras oralt, topiskt, intravenöst, intranasalt eller nebuliserat för att öka dess systemiska koncentration hos patienter som lider av oxidativ stress, till exempel.
Cancer
Forskning om oral administrering av glutation antyder att dess intag kan minska riskerna för oral cancer och att det, när det ges tillsammans med oxidativ kemoterapi, minskar de negativa effekterna av behandlingen hos cancerpatienter..
HIV
I allmänhet har patienter som är infekterade med det förvärvade immunbristviruset (HIV) intracellulära glutationbrister i både röda blodkroppar och T-celler och monocyter, vilket avgör deras korrekta funktion.
I en studie av Morris et al., Visades det att leverera glutation till makrofager från HIV-positiva patienter förbättrade funktionen hos dessa celler avsevärt, särskilt mot infektioner med opportunistiska patogener såsom M. tuberculosis.
Muskelaktivitet
Andra studier har att göra med förbättring av muskelkontraktil aktivitet, antioxidativt försvar och oxidativ skada orsakad som svar på ischemi / reperfusionsskador efter oral administrering av GSH under fysisk motståndsträning..
Leverpatologier
Det har i sin tur ansetts att dess intag eller intravenös administrering har funktioner för att förhindra utvecklingen av vissa typer av cancer och för att minska cellskador som uppstår till följd av vissa leverpatologier..
Antioxidant
Även om inte alla rapporterade studier har utförts på humana patienter, men vanligtvis är test i djurmodeller (i allmänhet murina), bekräftar resultaten som erhållits i vissa kliniska prövningar effektiviteten av exogent glutation som en antioxidant..
Av denna anledning används den för behandling av grå starr och glaukom, som en "anti-aging" -produkt, för behandling av hepatit, många hjärtsjukdomar, minnesförlust och för att stärka immunförsvaret och för Clearance efter tungmetall och läkemedelsförgiftning.
"Absorption"
Exogent administrerad glutation kan inte komma in i celler om den inte hydrolyseras till dess ingående aminosyror. Därför är den direkta effekten av administreringen (oral eller intravenös) av denna förening ökningen av den intracellulära koncentrationen av GSH tack vare bidraget från aminosyrorna som är nödvändiga för dess syntes, som effektivt kan transporteras till cytosolen..
Bieffekter
Även om intaget av glutation anses vara "säkert" eller ofarligt har inte tillräckligt många studier gjorts på dess biverkningar..
Men från de få rapporterade studierna är det känt att det kan ha negativa effekter som härrör från interaktionen med andra läkemedel och som kan vara skadliga för hälsan i olika fysiologiska sammanhang..
Om det tas långsiktigt verkar det som om de verkar för att sänka zinknivån för mycket och dessutom kan de, om de inhaleras, ge allvarliga astmaattacker hos astmatiska patienter..
Referenser
- Allen, J., & Bradley, R. (2011). Effekter av oral glutationstillskott på systemiska oxidativa stressbiomarkörer hos mänskliga volontärer. Journal of Alternative and Complementary Medicine, 17(9), 827-833.
- Conklin, K. A. (2009). Antioxidanter i kosten under cancerchemoterapi: inverkan på kemoterapeutisk effektivitet och utveckling av biverkningar. Näring och cancer, 37(1), 1-18.
- Meister, A. (1988). Glutationmetabolism och dess selektiva modifiering. Journal of Biological Chemistry, 263(33), 17205-17208.
- Meister, A., & Anderson, M. E. (1983). Glutation. Ann. Rev Biochem., 52, 711-760.
- Morris, D., Guerra, C., Khurasany, M., Guilford, F., & Saviola, B. (2013). Glutationstillskott förbättrar makrofagfunktioner vid HIV. Journal of Interferon & Cytokine Research, elva.
- Murray, R., Bender, D., Botham, K., Kennelly, P., Rodwell, V., & Weil, P. (2009). Harpers illustrerade biokemi (28: e upplagan). McGraw-Hill Medical.
- Nelson, D. L., & Cox, M. M. (2009). Lehninger Principer för biokemi. Omega-utgåvor (5: e upplagan). https://doi.org/10.1007/s13398-014-0173-7.2
- Noctor, G., Mhamdi, A., Chaouch, S., Han, Y. I., Neukermans, J., Marquez-garcia, B., ... Foyer, C. H. (2012). Glutation i växter: en integrerad översikt. Växt, cell och miljö, 35, 454-484.
- Pizzorno, J. (2014). Glutation! Undersökande medicin, 13(1), 8-12.
- Qanungo, S., Starke, D. W., Pai, H. V, Mieyal, J. J., & Nieminen, A. (2007). Glutationstillskott potentierar hypoxisk apoptos genom S-glutationylering av p65-NFkB. Journal of Biological Chemistry, 282(25), 18427-18436.
- Ramires, P. R., & Ji, L. L. (2001). Glutationstillskott och träning ökar hjärtmotstånd mot ischemi-reperfusion in vivo. Ann. J. Physiol. Hjärta Circ. Physiol., 281, 679-688.
- Sies, H. (2000). Glutation och dess roll i cellulära funktioner. Gratis radikal biologi och medicin R, 27(99), 916-921.
- Wu, G., Fang, Y., Yang, S., Lupton, J. R., & Turner, N. D. (2004). Glutationmetabolism och dess konsekvenser för hälsan. American Society for Nutritional Sciences, 489-492.



Ingen har kommenterat den här artikeln än.