
Den andra lagen om termodynamikformler, ekvationer, exempel
De Termodynamikens andra lag den har olika uttrycksformer. En av dem säger att ingen värmemotor kan omvandla all energi som den absorberar till användbart arbete (Kelvin-Planck-formulering). Ett annat sätt att säga det är att säga att verkliga processer sker i en sådan mening att energikvaliteten är lägre eftersom entropi tenderar att öka.
Denna lag, även känd som termodynamikens andra princip, har uttryckt sig på olika sätt över tiden, från tidigt 1800-tal till nutid, även om dess ursprung härrör från skapandet av de första ångmaskinerna i England., I början av 1700-talet.

Men även om det uttrycks på många sätt, tenderar tanken att materia blir oordning och att ingen process är 100% effektiv, eftersom förluster alltid kommer att finnas..
Alla termodynamiska system följer denna princip och börjar med universum i sig själv till morgonkoppen kaffe som väntar tyst på bordet och utbyter värme med miljön..
Kaffet svalnar när tiden går, tills det är i termisk jämvikt med miljön, så det skulle vara mycket förvånande om en dag skulle motsatsen hända och miljön svalnade medan kaffet värmte upp sig själv. Det är osannolikt att det kommer att hända, vissa kommer att säga omöjligt, men föreställ dig bara att det får en uppfattning om den mening där saker händer spontant.
I ett annat exempel, om vi skjuter en bok på ytan på ett bord, kommer den så småningom att sluta, eftersom dess kinetiska energi kommer att gå förlorad som värme på grund av friktion..
Termodynamikens första och andra lagstiftning upprättades omkring 1850 tack vare forskare som Lord Kelvin - skaparen av termen "termodynamik" -, William Rankine - författare till den första formella texten om termodynamik - och Rudolph Clausius..
Artikelindex
- 1 Formler och ekvationer
- 1.1 Reversibla och irreversibla processer
- 2 applikationer
- 2.1 Carnot-motor
- 2.2 Mänsklig metabolism
- 3 Exempel
- 4 Lösta övningar
- 4.1 Övning 1
- 4.2 Övning 2
- 4.3 Övning 3
- 5 Referenser
Formler och ekvationer
Entropi - nämndes i början - hjälper oss att fastställa den mening som saker händer i. Låt oss gå tillbaka till exemplet på kroppar i termisk kontakt.
När två objekt vid olika temperaturer kommer i kontakt och slutligen efter ett tag når termisk jämvikt, drivs de till det av det faktum att entropin når sitt maximala, när båda temperaturerna är desamma.
Betecknar entropi som S, förändringen i entropi AS av ett system ges av:

Förändringen av entropi AS indikerar graden av störning i ett system, men det finns en begränsning i användningen av denna ekvation: den är endast tillämplig på reversibla processer, det vill säga de där systemet kan återgå till sitt ursprungliga tillstånd utan att lämna ett spår av vad som hände-.
I irreversibla processer verkar termodynamikens andra lag så här:

Vändbara och irreversibla processer
Kaffekoppen blir alltid kall och är ett bra exempel på en oåterkallelig process, eftersom den alltid bara sker i en riktning. Om du lägger till grädde i kaffet och skakar får du en mycket trevlig kombination, men oavsett hur mycket du skakar igen kommer du inte att ha kaffe och grädde separat, eftersom omrörning är oåterkallelig..

Även om de flesta av de dagliga processerna är irreversibla, är det vissa nästan reversibel. Vändbarhet är en idealisering. För att detta ska kunna ske måste systemet förändras mycket långsamt på ett sådant sätt att det vid varje punkt alltid är i jämvikt. På detta sätt är det möjligt att återföra det till ett tidigare tillstånd utan att lämna spår i omgivningen..
Processer som ligger nära detta ideal är mer effektiva eftersom de levererar mer arbete med mindre energiförbrukning..
Friktionskraften är ansvarig för mycket av irreversibiliteten, eftersom värmen som genereras av den inte är den typ av energi som eftersträvas. I boken som glider över bordet är friktionsvärme energi som inte återvinns.
Även om boken återgår till sin ursprungliga position har bordet varit varmt som ett spår av att komma och gå på den.
Titta nu på en glödlampa: det mesta av arbetet som gjorts av strömmen genom glödtråden slösas bort i värme av Joule-effekten. Endast en liten andel används för att avge ljus. I båda processerna (bok och glödlampa) har systemets entropi ökat.
Applikationer
En idealisk motor är en som är byggd med reversibla processer och saknar friktion som orsakar energiförluster, omvandling nästan all värmeenergi i användbart arbete.
Vi betonar ordet nästan, för även den idealiska motorn, som är Carnots, är inte 100% effektiv. Den andra lagen om termodynamik säkerställer att så inte är fallet.
Carnot-motor
Carnot-motorn är den mest effektiva motorn som kan utvecklas. Den fungerar mellan två temperaturtankar i två isotermiska processer - vid konstant temperatur - och två adiabatiska processer - utan överföring av termisk energi-.
Diagrammen kallade PV-tryck-volymdiagram - klargör situationen med en överblick:
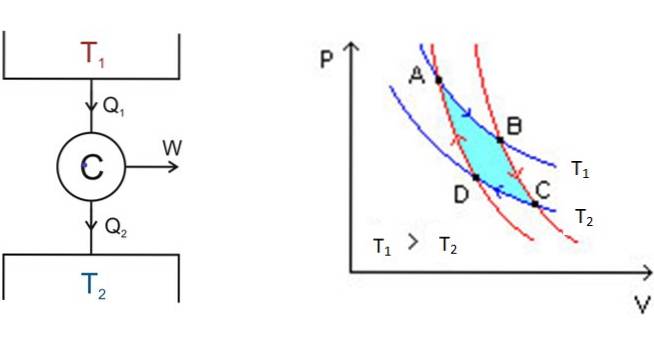
Till vänster, i figur 3 är diagrammet för Carnot-motorn C, som tar värme Q1 av tanken som är vid temperatur T1, omvandlar värmen till arbete W och ger avfallet Qtvå till den kallaste tanken, som ligger vid temperaturen Ttvå.
Från och med A expanderar systemet tills det når B och absorberar värme vid den fasta temperaturen T1. I B börjar systemet en adiabatisk expansion där ingen värme vinner eller förloras för att nå C.
I C börjar en annan isotermisk process: att överföra värme till den andra kallare termiska avsättningen som är vid Ttvå. När detta händer komprimeras systemet och når punkt D. Det börjar en andra adiabatisk process för att återgå till startpunkten A. På detta sätt avslutas en cykel.
Effektiviteten hos Carnot-motorn beror på temperaturen i kelvin i de två termiska behållarna:
Maximal effektivitet = (Qinträde - Futgång) / Qinträde = 1 - (Ttvå/ T1)
Carnots sats säger att detta är den mest effektiva värmemotorn där ute, men var inte för snabb att köpa den. Kommer du ihåg vad vi sa om reversibilitet i processen? De måste hända väldigt, mycket långsamt, så maskinens effekt är praktiskt taget noll..
Mänsklig metabolism
Människor behöver energi för att hålla alla sina system i drift, därför beter de sig som termiska maskiner som tar emot energi och omvandlar den till mekanisk energi för att till exempel flytta.
Effektivitet och av människokroppen när man utför arbete kan definieras som kvoten mellan den mekaniska kraften som den kan ge och den totala energiinmatningen, som kommer med mat.
Som medelkraft Pm är arbete W utfört i ett tidsintervall At, kan uttryckas som:
Pm = W / At
Ja UU / Δt är den hastighet med vilken energi tillsätts, kroppens effektivitet är som:
Genom ett flertal tester med volontärer har man uppnått effektivitet på upp till 17%, vilket ger cirka 100 watt effekt under flera timmar.
Naturligtvis beror det i stor utsträckning på den uppgift som utförs. Att trampa en cykel är något mer effektivt, cirka 19%, medan repetitiva uppgifter som inkluderar spader, plockar och hack är så låga som cirka 3%..
Exempel
Den andra lagen om termodynamik är implicit i alla processer som sker i universum. Entropi ökar alltid, även om det i vissa system verkar minska. För att detta ska hända har det varit tvungen att öka någon annanstans, så att det i den totala balansen är positivt.
- I lärandet finns entropi. Det finns människor som lär sig saker bra och snabbt, förutom att de lätt kommer ihåg dem senare. Det sägs att de är människor med låg entropilärande, men de är säkert mindre många än de med hög entropi: de som har svårare att komma ihåg de saker de studerar.
- Ett företag med oorganiserade arbetstagare har mer entropi än ett där arbetare utför uppgifter på ett ordnat sätt. Det är uppenbart att det senare kommer att vara effektivare än det förra.
- Friktionskrafter genererar mindre effektivitet vid drift av maskiner, eftersom de ökar mängden försvunnen energi som inte kan användas effektivt.
- Att kasta tärningar har en högre entropi än att vända ett mynt. Att slänga ett mynt har trots allt bara två möjliga resultat, medan att kasta matrisen har 6. Ju fler händelser som är troliga, desto mer entropi finns det..
Lösta övningar
Övning 1
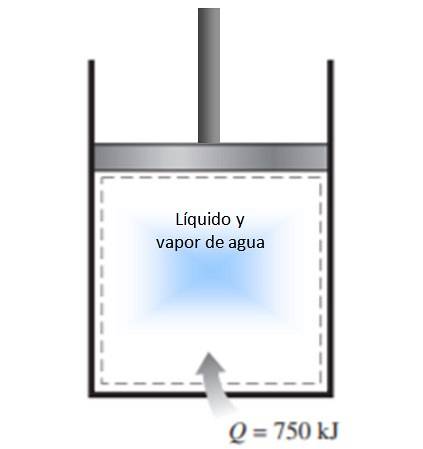
En kolvcylinder fylls med en blandning av vätska och vattenånga vid 300 K och 750 kJ värme överförs till vattnet genom en konstant tryckprocess. Som ett resultat förångas vätskan inuti cylindern. Beräkna förändringen i entropi i processen.

Lösning
Processen som beskrivs i uttalandet utförs vid konstant tryck i ett slutet system, som inte genomgår massutbyte.
Eftersom det är en förångning, under vilken temperaturen inte ändras heller (under fasförändringar är temperaturen konstant), kan definitionen av entropiändring som anges ovan tillämpas och temperaturen kan gå utanför integralen:
AS = 750.000 J / 300 K = 2500 J / K.
Eftersom värme kommer in i systemet är förändringen i entropi positiv.
Övning 2
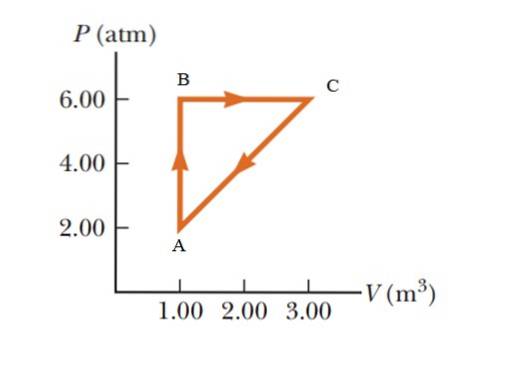
En gas genomgår en tryckökning från 2,00 till 6,00 atmosfärer (atm) och bibehåller en konstant volym på 1,00 m3, och expandera sedan vid konstant tryck tills den når en volym på 3,00 m3. Slutligen återgår det till sitt ursprungliga tillstånd. Beräkna hur mycket arbete som utförs i en cykel.

Lösning
Det är en cyklisk process där den inre energivariationen är noll, enligt termodynamikens första lag, därför Q = W. I ett PV-diagram (tryck-volym) motsvarar arbetet under en cyklisk process det område som omges av kurvan. För att ge resultaten i det internationella systemet är det nödvändigt att göra en enhetsändring av trycket med följande omvandlingsfaktor:
1 atm = 101,325 kPa = 101,325 Pa.
Området som omges av diagrammet motsvarar en triangel vars bas (3 - 1 m3) = 2 m3 och vars höjd är (6 - 2 atm) = 4 atm = 405,300 Pa
WABCA = ½ (2 m3 x 405300 Pa) = 405300 J = 405,3 kJ.
Övning 3
En av de mest effektiva maskinerna som någonsin byggts sägs vara en koleldad ångturbin vid floden Ohio, som används för att driva en elektrisk generator som arbetar mellan 1870 och 430 ° C..
Beräkna: a) Den maximala teoretiska verkningsgraden, b) Den mekaniska effekten som levereras av maskinen om den absorberar 1,40 x 105 J energi varje sekund från den heta tanken. Den verkliga effektiviteten är känd för att vara 42,0%.
Lösning
a) Den maximala effektiviteten beräknas med ekvationen ovan:
Maximal effektivitet = (Qinträde - F utgång) / Qinträde = 1 - (Ttvå/ T1)
För att ändra grader Celsius till kelvin, lägg bara till 273,15 till Celsius temperaturen:

Att multiplicera med 100% ger maximal procentuell effektivitet, vilket är 67,2%
c) Om den verkliga effektiviteten är 42%, är det en maximal effektivitet på 0,42.
Den mekaniska effekten som levereras är: P = 0,42 x 1,40 x 10 5 J / s = 58800 W.
Referenser
- Bauer, W. 2011. Fysik för teknik och vetenskap. Volym 1. Mc Graw Hill.
- Cengel, Y. 2012. Termodynamik. 7mamma Utgåva. Mcgraw hill.
- Figueroa, D. (2005). Serie: Fysik för vetenskap och teknik. Volym 4. Vätskor och termodynamik. Redigerad av Douglas Figueroa (USB).
- Knight, R. 2017. Physics for Scientists and Engineering: a Strategy Approach.
- López, C. Den första lagen om termodynamik. Återställd från: culturacientifica.com.
- Serway, R. 2011. Fundamentals of Physics. 9na Cengage Learning.
- Sevilla universitet. Termiska maskiner. Återställd från: laplace.us.es


Ingen har kommenterat den här artikeln än.