
Atomvolym Hur det varierar i det periodiska systemet och exempel
De atomvolym är ett relativt värde som indikerar förhållandet mellan elementets molära massa och dess densitet. Så denna volym beror på elementets densitet, och densiteten beror i sin tur på fasen och hur atomerna är ordnade i den..
Så atomvolymen för ett element Z är inte densamma i en annan fas än den den uppvisar vid rumstemperatur (flytande, fast eller gasformig), eller när den är en del av vissa föreningar. Således skiljer sig atomvolymen av Z i förening ZA från den för Z i förening ZB.

Varför? För att förstå det är det nödvändigt att jämföra atomer med till exempel kulor. Kulorna, som de blåaktiga på bilden ovan, har en väldefinierad materialgräns, som kan ses tack vare sin blanka yta. Däremot är atomernas gräns diffus, även om de kan betraktas som fjärrfäriska.
Således, vad som bestämmer en punkt bortom atomgränsen är noll sannolikheten för att hitta en elektron, och denna punkt kan vara längre eller närmare kärnan beroende på hur många angränsande atomer interagerar runt atomen under övervägande..
Artikelindex
- 1 Atomvolym och radie
- 2 Ytterligare formel
- 3 Hur varierar atomvolymen i det periodiska systemet?
- 3.1 Atomvolymer av övergångsmetaller
- 4 Exempel
- 4.1 Exempel 1
- 4.2 Exempel 2
- 5 Referenser
Atomvolym och radie
Genom att interagera med två H-atomer i H-molekylentvå, positionerna för deras kärnor definieras såväl som avstånden mellan dem (kärnkraftsavstånd). Om båda atomerna är sfäriska är radien avståndet mellan kärnan och den otydliga gränsen:
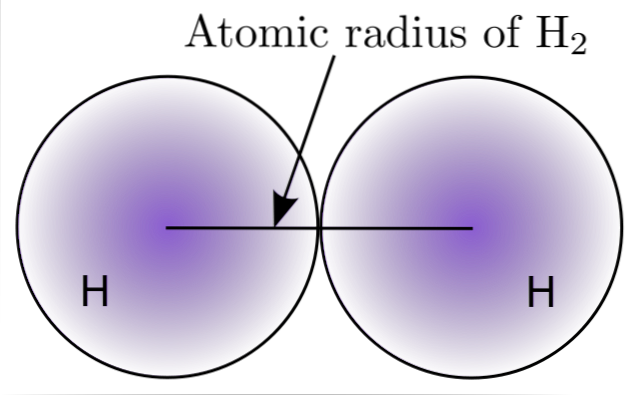
I bilden ovan kan du se hur sannolikheten för att hitta en elektron minskar när den rör sig bort från kärnan. Då man delar det kärnkraftiga avståndet med två erhålls atomradien. Därefter antar vi en sfärisk geometri för atomerna, och formeln används för att beräkna sfärens volym:
V = (4/3) (Pi) r3
I detta uttryck är r den atomära radien bestämd för H-molekylentvå. Värdet på V beräknat med denna oprecisa metod kan förändras om till exempel H beaktastvå i flytande eller metalliskt tillstånd. Denna metod är dock mycket felaktig eftersom atomernas former är mycket långt ifrån den ideala sfären i deras interaktioner..
För att bestämma atomvolymerna i fasta ämnen beaktas många variabler som rör arrangemanget och som erhålls genom röntgendiffraktionsstudier..
Ytterligare formel
Molmassa uttrycker mängden materia som har ett mol atomer av ett kemiskt element.
Dess enheter är g / mol. Å andra sidan är densitet den volym som ett gram av elementet upptar: g / ml. Eftersom enheterna med atomvolym är ml / mol måste du spela med variablerna för att nå de önskade enheterna:
(g / mol) (ml / g) = ml / mol
Eller vad är detsamma:
(Molmassa) (1 / D) = V.
(Molmassa / D) = V.
Således kan volymen av en mol atomer i ett element lätt beräknas; medan med formeln för den sfäriska volymen beräknas volymen för en enskild atom. För att komma fram till detta värde från första började en omvandling genom Avogadros nummer (6.02 · 10-2. 3).
Hur varierar atomvolymen i det periodiska systemet?
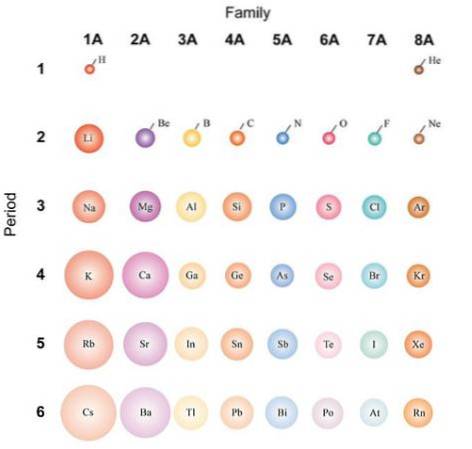
Om atomerna anses sfäriska, kommer deras variation att vara densamma som den som observerats i atomradier. I bilden ovan, som visar representativa element, illustreras att atomerna blir från höger till vänster; istället blir de mer omfattande från topp till botten.
Detta beror på att kärnan under samma period innehåller protoner när den rör sig åt höger. Dessa protoner utövar en attraktiv kraft på de externa elektronerna, som känner en effektiv kärnladdning Zef, mindre än den faktiska kärnkraftsladdningen Z.
Elektronerna i de inre skalen stöter bort de yttre skalens, vilket minskar kärnans effekt på dem; detta kallas skärmeffekt. Under samma period kan skärmeffekten inte motverka ökningen av antalet protoner, så elektronerna i det inre skalet hindrar inte atomerna från att komma ihop..
Men att gå ner i en grupp möjliggör nya energinivåer, som gör att elektroner kan kretsa längre från kärnan. På samma sätt ökar antalet elektroner i det inre skalet, vars skärmningseffekter börjar minskas om kärnan lägger till protoner igen..
Av dessa skäl inses det att grupp 1A har de mest voluminösa atomerna, till skillnad från de små atomerna i grupp 8A (eller 18), de hos ädelgaserna..
Atomvolymer av övergångsmetaller
Övergångsmetallatomer innehåller elektroner i inre d-orbitaler. Denna ökning av skärmeffekten och, liksom i den verkliga kärnkraftsladdningen Z, avbryts nästan lika, så att deras atomer behåller samma storlek under samma period..
Med andra ord: under en period uppvisar övergångsmetaller liknande atomvolymer. Dessa små skillnader är emellertid enormt signifikanta när man definierar metalliska kristaller (som om de var metalliska kulor).
Exempel
Två matematiska formler är tillgängliga för att beräkna atomens volym för ett element, var och en med motsvarande exempel.
Exempel 1
Med tanke på atomradien för väte -37 pm (1 pikometer = 10-12m) - och cesium -265 pm-, beräkna deras atomvolymer.
Med hjälp av den sfäriska volymformeln har vi då:
VH= (4/3) (3.14) (37 pm)3= 212.07 pm3
VCs= (4/3) (3.14) (265 pm)3= 77912297,67 pm3
Dessa volymer uttryckta i pikometrar är emellertid orimliga, så de omvandlas till enheter av ångström och multiplicerar dem med omvandlingsfaktorn (1Å / 100pm)3:
(212.07 pm3) (1Å / 100 pm)3= 2.1207 × 10-4 TILL3
(77912297.67 pm3) (1Å / 100pm)3= 77,912 Å3
Således visas skillnaderna i storlek mellan den lilla H-atomen och den skrymmande Cs-atomen numeriskt. Man måste komma ihåg att dessa beräkningar endast är approximationer under påståendet att en atom är helt sfärisk, som vandrar framför verkligheten.
Exempel 2

Densiteten av rent guld är 19,32 g / ml och dess molära massa är 196,97 g / mol. Följande M / D-formel för att beräkna volymen av en mol guldatomer erhålls följande:
VAu= (196,97 g / mol) / (19,32 g / ml) = 10,19 ml / mol
Det vill säga 1 mol guldatomer upptar 10,19 ml, men vilken volym upptar en guldatom specifikt? Och hur man uttrycker det i enheter av pm3? För detta, använd bara följande omvandlingsfaktorer:
(10,19 ml / mol) · (mol / 6,02 · 10-2. 3 atomer) · (1 m / 100 cm)3(13.00 / 10-12m)3= 16,92 · 106 p.m3
Å andra sidan är atomradien av guld 166 pm. Om båda volymerna jämförs - den som erhållits med den tidigare metoden och den som beräknas med den sfäriska volymformeln - kommer det att konstateras att de inte har samma värde:
VAu= (4/3) (3.14) (166 pm)3= 19.15 · 106 p.m3
Vilken av de två är närmast det accepterade värdet? Den som är närmast de experimentella resultaten som erhållits genom röntgendiffraktion av kristallstrukturen av guld.
Referenser
- Helmenstine, Anne Marie, Ph.D. (09 december 2017). Atomisk volymdefinition. Hämtad den 6 juni 2018 från: thoughtco.com
- Mayfair, Andrew. (13 mars 2018). Hur man beräknar en atoms volym. Sciencing. Hämtad den 6 juni 2018 från: sciencing.com
- Wiki Kids Ltd. (2018). Lothar Meyer Atomic Volymkurvor. Hämtad den 6 juni 2018 från: wonderwhizkids.com
- Lumen. Periodiska trender: Atomic Radius. Hämtad den 6 juni 2018 från: courses.lumenlearning.com
- Camilo J. Derpich. Atomvolym och densitet. Hämtad den 6 juni 2018 från: es-puraquimica.weebly.com
- Whitten, Davis, Peck & Stanley. Kemi. (8: e upplagan). CENGAGE Learning, s 222-224.
- CK-12 Foundation. (22 februari 2010). Jämförande atomstorlekar. [Figur]. Hämtad den 6 juni 2018 från: commons.wikimedia.org
- CK-12 Foundation. Utgåva (22 februari 2010). Atomradie av Htvå. [Figur]. Hämtad den 6 juni 2018 från: commons.wikimedia.org



Ingen har kommenterat den här artikeln än.