
Kaliumbensoatstruktur, egenskaper, produktion, användningsområden

De kaliumbensoat är en organisk förening bildad av en kalium K-jon+ och en bensoatjon C6H5KUTTRA-. Dess kemiska formel är C6H5COOK eller kondenserad formel C7H5KOtvå. Det är ett vitt kristallint fast ämne. Det är hygroskopiskt, vilket innebär att det absorberar vatten från luften.
Vattenhaltiga kaliumbensoatlösningar är lätt alkaliska. I ett surt medium är bensoatjonen (C6H5KUTTRA-tenderar att ta en proton och förvandlas till bensoesyra (C6H5COOH).

Kaliumbensoat används som konserveringsmedel, särskilt när det är önskvärt att dessa är fria från natrium (Na). Förhindrar matförstöring på grund av mikroorganismer.
Det används bland annat i pålägg, bearbetade läskedrycker och bageriprodukter. Dess konserverande verkan beror troligen på bensoesyra (C6H5COOH) som bildas vid lågt pH, vilket förhindrar reproduktion av svampar och bakterier.
Även om kaliumbensoat är godkänt av hälsoorganisationer, är det lämpligt att inte missbruka dess användning, eftersom det har visat sig att det kan påverka foster hos möss.
Artikelindex
- 1 Struktur
- 2 Nomenklatur
- 3 fastigheter
- 3.1 Fysiskt tillstånd
- 3.2 Molekylvikt
- 3.3 Löslighet
- 3,4 pH
- 3.5 Kemiska egenskaper
- 4 Skaffa
- 5 användningsområden
- 5.1 I den bearbetade livsmedelsindustrin
- 5.2 Mot svampar
- 5.3 Mot bakterier
- 5.4 I olika applikationer
- 5.5 Negativa effekter av intag av mat med kaliumbensoat
- 6 Referenser
Strukturera
Kaliumbensoat är ett organiskt salt, det vill säga ett salt av en karboxylsyra, eftersom det är kaliumsaltet av bensoesyra. Den består av en K + kaliumkatjon och en C-bensoatanjon6H5KUTTRA-.
Bensoatanjon C6H5KUTTRA- består av en bensenring C6H5- och en karboxylatgrupp -COO-.
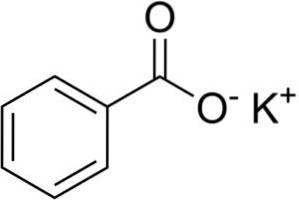
Bindningen mellan dessa två joner är en stark elektrostatisk bindning som håller dem i kristallgitteret..
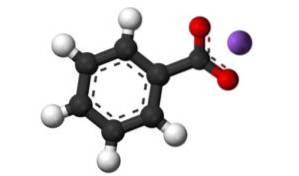
Nomenklatur
- Kaliumbensoat
- Kaliumsalt av bensoesyra
Egenskaper
Fysiskt tillstånd
Fast vit kristallin.
Molekylvikt
160,212 g / mol
Löslighet
Lösligt i vatten.
pH
Vattenlösningar av kaliumbensoat är något basiska.
Kemiska egenskaper
Det är hygroskopiskt, det vill säga det är ett fast ämne som lätt absorberar vatten från miljön.
Föreningen mellan kaliumjonen K+ och bensoatjonen C6H5KUTTRA- som i de flesta jonföreningar kan den endast övervinnas genom hög temperatur eller genom ett mycket polärt lösningsmedel såsom vatten.
Bensoatanjon C6H5KUTTRA- det är måttligt grundläggande, med en märkbar tendens att kombinera med protoner. Reagerar med vatten genom att ta en proton H+ för att bilda bensoesyra (C6H5COOH) och detta leder till en ökning av koncentrationen av OH-joner-.
C6H5KUTTRA- + HtvåO ⇔ C6H5COOH + OH-
Av denna anledning är vattenlösningar av kaliumbensoat lätt alkaliska..
Erhållande
För att bereda kaliumbensoat, bensoesyra (C6H5COOH) med kaliumkarbonat (KtvåCO3i en minsta volym vatten för att erhålla en klar lösning från vilken saltet kristalliserar.
2 C6H5COOH + KtvåCO3 → 2 C6H5KUTTRA-K+ + HtvåO + COtvå↑
Sedan tvättas det kristalliserade kaliumbensoatsaltet flera gånger med eter och torkas.
Applikationer
I den bearbetade livsmedelsindustrin
Kaliumbensoat används ofta som ett antimikrobiellt medel för konservering av drycker, fruktderivat, bageriprodukter och andra livsmedel.

Det är ett livsmedelskonserveringsmedel som kan hämma, sakta ner eller sakta ner fermenterings-, försurnings- eller försämringsprocessen av mat på grund av vissa svampar och bakterier..
Enligt Environmental Protection Agency eller EPA Naturvårdsverket) kaliumbensoat har verifierats som en förening som inte påverkar människors hälsa.
Mot svampar
Det är ett svampmedel, eftersom det kan förstöra dem genom att undertrycka deras förmåga att växa eller reproducera. Det är inte en fungicid för vävnader från djur eller människor, utan en hämmare som saktar eller bromsar spridningen av svampar i mat eller dryck.
Vissa typer av mögel producerar ämnen som kallas aflatoxiner, som är ett hot för både människor och djur eftersom de är giftiga, kan orsaka cancer och mutationer.
De flesta formar inhiberas i koncentrationer av 0,05-0,10% kaliumbensoat. Prestandan för detta beror på pH, eftersom det vid ett lägre pH är mer effektivt som en antisvamp.

Detta beror på att den antifungala effekten faktiskt finns i bensoesyra C6H5COOH, som är den konjugerade syran av kaliumbensoat. Denna syra bildas vid lågt pH, det vill säga i närvaro av en stor mängd vätejoner H+:
Kaliumbensoat + vätejoner → bensoesyra + kaliumjoner
C6H5COOK + H+ → C6H5COOH + K+
Enligt vissa forskare beror dess effektivitet delvis på lösligheten av bensoesyra i mikroorganismens cellmembran. Denna typ av syra ökar flödet av protoner genom membranet..
Detta orsakar störning eller desorganisering av vissa funktioner i svampcellen..
Mot bakterier
Det är ett medel som fungerar mot vissa bakterier. Det läggs till livsmedel som bearbetade korvar, bearbetade skinkor (färdiga att äta) och vissa drycker.
Det har testats mot Listeria monocytogenes, en bakterie som kan döda människor som äter mat som är förorenad med den. Det producerar feber, kräkningar och diarré, bland andra symtom.
Livsmedel behandlade med kaliumbensoat och kontaminerade med kaliumbensoat har visat sig Listeria måste hållas vid temperaturer under -2,2 ° C så att bakterierna inte reproducerar sig.

Å andra sidan har användningen av elektronstrålning försökt för att intensifiera effekten av kaliumbensoat mot bakterier, men det har fastställts att bensen C produceras.6H6 som är en giftig förening.
Därför, även om livsmedel innehåller kaliumbensoat, rekommenderas det att de helst kokas vid höga temperaturer innan de konsumeras, för att eliminera alla typer av faror som härrör från närvaron av patogena bakterier..
I olika applikationer
Enligt konsulterade källor används kaliumbensoat också i lim och bindemedel för en mängd olika användningsområden. Det tillsätts till cigaretter och tobak eller är relaterat till tillverkningen av dessa.
Det används i personligvårdsprodukter som kosmetika, schampo, parfymer, tvålar, lotioner etc. Också en del av färger och beläggningar.
Negativa effekter av intag av mat med kaliumbensoat
Vissa forskare fann att kaliumbensoat gav skadliga effekter på mössfoster.
Även om inga effekter observerades hos vuxna möss som exponerades för kaliumbensoat, sågs missbildningar i fostrets ögon och en markant minskning i vikt och längd hos de små kropparna hos musfostren..
Detta innebär att foster är känsligare för kaliumbensoat än vuxna möss..
Referenser
- Mandal, P.K. et al. (1978). Viskositetsbeteende för bensoesyra och bensoatjon i vattenlösning. Journal of Solution Chemistry, Vol. 7, nr 1, 1978. Återställd från link.springer.com.
- Rusul, G. och Marth, E.H. (1987). Tillväxt och aflatoxinproduktion av Aspergillus parasiticus NRRL 2999 i närvaron av kaliumbenzoat eller kaliumsorbat och vid olika initiala pH-värden. J Food Prot. 1987; 50 (10): 820-825. Återställd från ncbi.nlm.nih.gov.
- Lu, Z. et al. (2005). Hämmande effekter av organiska syrasalter för kontroll av Listeria monocytogenes på Frankfurters. J Food Prot.2005; 68 (3): 499-506. Återställd från ncbi.nlm.nih.gov.
- Zhu, M.J. et al. (2005). Inverkan av antimikrobiella ingredienser och bestrålning på överlevnaden av Listeria monocytogenes och kvaliteten på färdig att äta kalkonskinka. Poult Sci.2005; 84 (4): 613-20. Återställd från ncbi.nlm.nih.gov.
- USA National Library of Medicine. (2019). Kaliumbensoat. Återställd från pubchem.ncbi.nlm.nih.gov.
- Afshar, M. et al. (2013). Teratogena effekter av långvarig konsumtion av kaliumbensoat på ögonutveckling i balb / c fostermöss. Iran J Basic Med Sci. 2013; 16 (4): 584-589. Återställd från ncbi.nlm.nih.gov.
- Lide, D.R. (redaktör) (2003). CRC Handbook of Chemistry and Physics. 85th CRC Press.
- Morrison, R.T. och Boyd, R.N. (2002). Organisk kemi. 6: e upplagan. Prentice-Hall.



Ingen har kommenterat den här artikeln än.