
Bensinstruktur, egenskaper, användningsområden och risker
De bensoin eller benso Det är ett vitt kristallint fast ämne med en kamferlukt som består av en organisk förening. Det är en aceton, speciellt en acetofenon med intilliggande hydroxi- och fenylkol. Den produceras genom katalytisk kondensation av bensaldehyd, med kaliumcyanid som katalysator.
Det rapporterades första gången 1828 av Julius Von Liebig och Friedrich Woehler under deras undersökningar av en bitter mandelolja, som bestod av bensaldehyd och hydrocyansyra. Den katalytiska syntesen av bensoin förbättrades senare av Nikolai Zinin.
Bensin är praktiskt taget olösligt i vatten, men det är lösligt i het alkohol och andra organiska lösningsmedel, såsom koldisulfid och aceton..
Detta namn används också för att hänvisa till bensinharts, erhållet från trädet Styrax bensoin. Hartset innehåller bensoesyra, fenylpropionsyra, bensaldehyd, kanelsyra, bensylbensoat och vanillin, vilket ger det en vaniljlukt..
Denna eteriska olja bör inte förväxlas med föreningen bensin, som har en annan sammansättning och ursprung..
Artikelindex
- 1 Struktur av bensoin
- 2 fastigheter
- 2.1 Namn
- 2.2 Molekylformel
- 2.3 Molmassa
- 2.4 Fysisk beskrivning
- 2.5 Smak
- 2.6 Kokpunkt
- 2.7 Smältpunkt
- 2.8 Flampunkt
- 2.9 Löslighet i vatten
- 2.10 Löslighet i organiska lösningsmedel
- 2,11 pH
- 2.12 Stabilitet
- 2.13 En annan experimentell egenskap
- 3 Syntes
- 4 användningsområden
- 4.1 Förmedlande medel
- 4.2 I livsmedel
- 4.3 Mänsklig och veterinärmedicin
- 4.4 Personlig vård
- 4.5 Användning av eterisk bensinolja
- 5 Toxicitet
- 6 Referenser
Struktur av bensoin
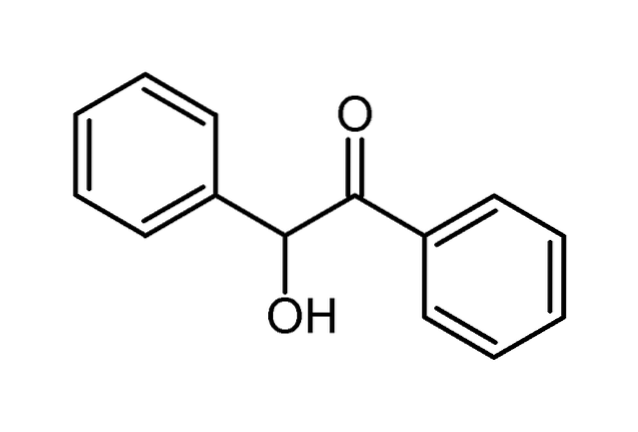
I bilden ovan visades bensoins molekylstruktur med en sfär och stavmodell. Man kan se att den har två aromatiska ringar åtskilda av två syrebärande kol; från vänster till höger, CHOH och CO. Observera också att ringarna har olika riktningar i rymden..
Den hydrofoba delen dominerar i sin struktur, medan oxygener bidrar något till dess dipolmoment; eftersom båda aromatiska ringarna lockar elektrontätheten mot dem, sprider laddningen mer homogent.
Resultatet är att bensinmolekylen inte är för polär; vilket motiverar att det är dåligt lösligt i vatten.
Genom att fokusera på båda syreatomerna kommer det att ses att OH-gruppen kan bilda en intramolekylär vätebindning med den intilliggande karbonylgruppen; det vill säga, de skulle inte binda två bensinmolekyler, utan snarare skulle en specifik rumslig konformation förstärkas, vilket förhindrade H (OH) C-CO-bindningen från att rotera för mycket.
Även om bensin inte betraktas som en molekyl med hög polaritet, ger dess molekylvikt den tillräcklig sammanhållningskraft för att definiera en monoklinisk vit kristall, som smälter runt 138 ° C; beroende på föroreningsnivån kan den ha en lägre eller högre temperatur.
Egenskaper
Namn
Några av dess många ytterligare namn är:
- 2-hydroxi-1,2-difenyletanon.
- bensoylfenylkarbanol.
- 2-hydroxi-2-fenylacetofenon.
- 2-hydroxi-1,2-difenyletan-1-on.
Molekylär formel
C14H12ELLERtvå eller C6H5COCH (OH) C6H5.
Molmassa
212,248 g / mol.
Fysisk beskrivning
Benzoin är ett vitt till benvitt kristallint fast ämne med kamferlukt. När de är trasiga är färska ytor mjölkvita. Det kan också visas som ett torrt pulver eller vita eller gula kristaller.
Smak
Inte beskrivet. Något skarpt.
Kokpunkt
344 ºC.
Smältpunkt
137 ºC.
Antändningspunkt
181 ºC.
Vattenlöslighet
Praktiskt taget olöslig.
Löslighet i organiska lösningsmedel
Löslig i het alkohol och koldisulfid.
pH
I alkoholhaltig lösning är den sur, bestäms av lakmusspapper.
Stabilitet
I stall. Det är en brännbar förening och oförenlig med starka oxidationsmedel.
En annan experimentell egenskap
Minska Fehlings lösning.
Syntes
Den nedre bilden visar kondensationsreaktionen av bensaldehyd för att ge upphov till bensin. Denna reaktion gynnas i närvaro av kaliumcyanid i etylalkohollösning..
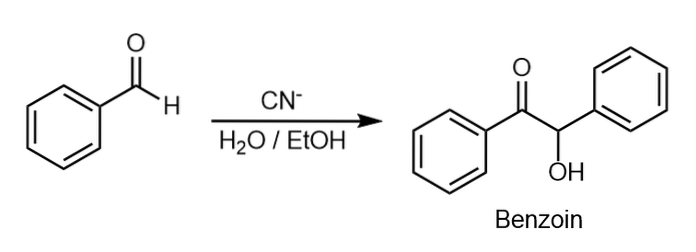
Två bensaldehydmolekyler är kovalent kopplade genom att frigöra en vattenmolekyl.
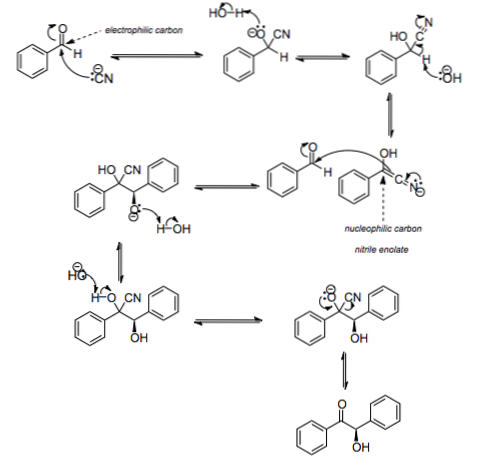
Hur händer detta? Genom mekanismen som illustreras ovan. CN-anjon- den fungerar som en nukleofil genom att attackera kolet i karbonylgruppen i bensaldehyd. Genom att göra detta och med deltagande av vatten blir C = O C = N; men nu ersätts H med en OH och bensaldehyden blir nitrilenolat (bildens andra rad).
Den negativa laddningen av kväve avlägsnas mellan den och kolet -C-CN; detta kol sägs då vara nukleofilt (det ser efter positiva laddningar). Så mycket att den attackerar karbonylgruppen i en annan bensaldehydmolekyl.
Återigen ingriper en vattenmolekyl för att producera en OH- och deprotonera en OH-grupp; som senare bildar en dubbelbindning med kol för att ge upphov till en C = O-grupp, medan CN-gruppen migrerar som en cyanidanjon. Således har CN- katalyserar reaktionen utan att konsumeras.
Applikationer
Förmedlande agent
Benzoin är involverad i syntesen av organiska föreningar genom katalytisk polymerisation. Det är en mellanprodukt för syntesen av a-bensoinoxim, ett analytiskt reagens för metaller. Det är ett föregångare för bensyl, som fungerar som en fotoinitiator.
Syntesen av bensyl fortsätter genom organisk oxidation med koppar (III), salpetersyra eller ozon. Benzoin används vid beredning av farmaceutiska läkemedel såsom oxaprozin, ditazol och fenytoin.
I mat
Benzoin används som ett livsmedelssmakämne.
Mänsklig och veterinärmedicin
I veterinärmedicin används det som ett antiseptiskt medel för topisk applicering, används vid behandling av hudsår för att producera deras läkning.
Det används också i medicin i formuleringar för beredning av inhalationsmedel för behandling av bronkit och slemlösande medel för oral användning..
Personlig vård
Benzoin används vid tillverkning av deodoranter.
Benzoin eterisk olja använder
Denna eteriska olja har rapporterats stimulera cirkulationen. En fördelaktig effekt på nervsystemet har också rapporterats, vilket manifesteras av en lindring av ångest och stress. På samma sätt har det antecknats att det har en antiseptisk verkan på öppna sår..
Vissa föreningar som finns i bensoin eterisk olja, såsom bensaldehyd, bensoesyra och bensylbensoat, är bakteriedödande och svampdödande ämnen som förhindrar sepsis..
Det har visats att den har antiflatulent och karminativ verkan, en effekt som tillskrivs dess avslappnande verkan på magmusklerna. På samma sätt tillskrivs det en diuretisk verkan som bidrar till att eliminera giftiga ämnen för kroppen.
Denna eteriska olja används som ett slemlösande medel som lindrar trängsel i luftvägarna. På samma sätt har de använts för att lindra artrit genom topisk applicering som möjliggör absorption av medicinska komponenter genom huden..
Giftighet
Benzoin vid kontakt orsakar rodnad och irritation i hud och ögon. Vid inandning av sammansatt damm uppträder irritation i luftvägarna, som manifesteras av hosta. Men i allmänhet är det inte en mycket giftig förening..
Till tinkturen av bensin, ett alkoholiskt extrakt av trädets harts Stirax bensoin, En uppsättning giftiga åtgärder har påpekats för honom. Kanske för att tinkturen är en blandning av föreningar; inklusive bensoesyra, bensaldehyd, etc..
Kontakt med huden orsakar inte signifikant irritation. Men kontakt med ögonen kan orsaka irritation, vilket manifesteras av rodnad, smärta, sönderrivning och suddig syn..
Inandning av ångor från bensintinktur kan orsaka irritation i luftvägarna, hosta, nysningar, rinnande näsa, heshet och halsont..
Slutligen kan intag av tinkturen orsaka irritation i mag-tarmkanalen, manifesterad av buksmärta, illamående, kräkningar och diarré..
Referenser
- Wikipedia. (2019). Bensin (organisk förening). Återställd från: en.wikipedia.org
- Nationellt centrum för bioteknikinformation. (2019). Benzoin. PubChem-databas. CID = 8400. Återställd från: pubchem.ncbi.nlm.nih.gov
- Donald L. Robertson. (2012). Flerstegssyntes-koenzymkatalyserad syntes av bensoin och derivat. Återställd från: home.miracosta.edu
- Tim Soderberg. (2014, 29 augusti). Vitamin B1. Kemi LibreTexts. Återställd från: chem.libretexts.org
- Haisa, S. Kashino och M. Morimoto. (1980). Strukturen av bensoin. Acta Cryst. B36, 2832-2834. doi.org/10.1107/S0567740880010217
- Meenakshi Nagdeve. (21 maj 2019). 11 fantastiska fördelar med eterisk bensinolja. Organiska fakta. Återställd från: organicfacts.net
- Bre. (2019). Benzoin eterisk olja älskad av Ancient Royalty. Återställd från: monq.com


Ingen har kommenterat den här artikeln än.