
Kalorimetri vilka studier och tillämpningar
De kalorimetri är en teknik som bestämmer förändringarna i kaloriinnehållet i ett system associerat med en kemisk eller fysisk process. Den är baserad på mätning av temperaturförändringar när ett system absorberar eller avger värme. Kalorimetern är den utrustning som används i reaktioner där ett värmeväxling är involverat.
Vad som kallas en "kaffekopp" är den enklaste formen av denna typ av apparat. Genom dess användning mäts mängden värme som är involverad i reaktioner som utförs vid konstant tryck i en vattenlösning. En kalorimeter för kaffekopp består av en polystyrenbehållare som placeras i en bägare..

Vattnet placeras i polystyrenbehållaren, försedd med ett lock av samma material som ger en viss grad av värmeisolering. Dessutom har behållaren en termometer och en mekanisk omrörare..
Denna kalorimeter mäter mängden värme som absorberas eller släpps ut, beroende på om reaktionen är endoterm eller exoterm, när en reaktion äger rum i en vattenlösning. Systemet som ska studeras består av reaktanterna och produkterna.
Artikelindex
- 1 Vad studerar kalorimetri?
- 2 Värmekapacitet för en kalorimeter
- 2.1 Exempel på användning av kalorimetern för att beräkna specifik värme
- 3 Kalorimetrisk pump
- 4 typer av kalorimeter
- 4.1 Isotermisk titreringskalorimeter (CTI)
- 4.2 Differentialsökningskalorimeter
- 5 applikationer
- 5.1 Användning av isotermisk titreringskalorimetri
- 5.2 Användning av differentiell skanningskalorimetri
- 6 Referenser
Vad studerar kalorimetri?
Kalorimetri studerar förhållandet mellan värmeenergin associerad med en kemisk reaktion och hur den används för att bestämma dess variabler. Deras tillämpningar inom forskningsområden motiverar omfattningen av dessa metoder.
Kalorimeters kalorikapacitet
Denna kapacitet beräknas genom att dividera mängden värme som absorberas av kalorimetern med temperaturförändringen. Denna variation är produkten av värmen som avges i en exoterm reaktion, vilken är lika med:
Mängden värme som absorberas av kalorimetern + mängden värme som absorberas av lösningen
Variationen kan bestämmas genom att tillsätta en känd mängd värme genom att mäta temperaturförändringen. För denna bestämning av kalorikapaciteten används vanligen bensoesyra, eftersom dess förbränningsvärme är känd (3,227 kJ / mol).
Kalorikapaciteten kan också bestämmas genom att tillsätta värme med hjälp av en elektrisk ström.
Exempel att använda kalorimetern för att beräkna specifik värme
En bar på 95 g av en metall upphettas till 400 ° C och tar den omedelbart till en kalorimeter med 500 g vatten, initialt vid 20 ° C. Systemets slutliga temperatur är 24 ºC. Beräkna metallens specifika värme.
Aq = m x ce x At
I detta uttryck:
Δq = belastningsvariation.
m = massa.
ce = specifik värme.
Δt = temperaturvariation.
Värmen som erhålls av vattnet är lika med värmen som avges från metallstången.
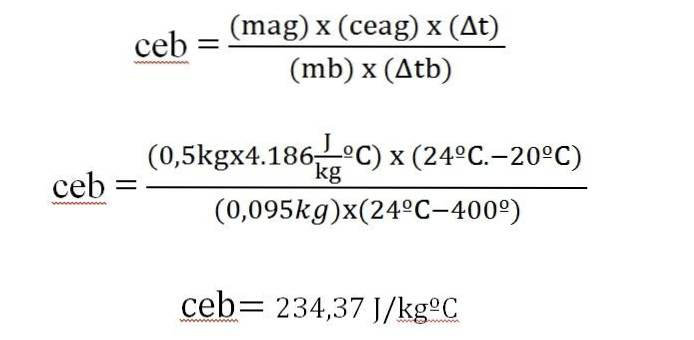
Detta värde liknar det som visas i en tabell över den specifika värmen för silver (234 J / kg ºC).
Så, en av tillämpningarna av kalorimetri är samarbetet för identifiering av material.
Kalorimetrisk pump
Den består av en stålbehållare, känd som pumpen, som är motståndskraftig mot de höga tryck som kan uppstå under reaktionerna i denna behållare. denna behållare är ansluten till en tändkrets för att starta reaktionerna.
Pumpen är nedsänkt i en stor behållare med vatten, vars funktion är att absorbera värmen som genereras i pumpen under reaktionerna, vilket gör temperaturvariationen liten. Vattenbehållaren är utrustad med en termometer och en mekanisk omrörare.
Energiförändringar mäts med praktiskt taget konstant volym och temperatur, så inget arbete görs med de reaktioner som uppstår i pumpen.
AE = q
ΔE är variationen av den inre energin i reaktionen och q värmen som genereras i denna.
Typer av kalorimeter
Isotermisk titreringskalorimeter (CTI)
Kalorimetern har två celler: i en placeras provet och i den andra, referensen, vanligtvis placeras vatten.
Temperaturskillnaden som genereras mellan cellerna - på grund av reaktionen som sker i provcellen - avbryts av ett återkopplingssystem som injicerar värme för att utjämna temperaturerna i cellerna..
Denna typ av kalorimeter gör det möjligt att följa interaktionen mellan makromolekyler och deras ligander..
Differentialskanningskalorimeter
Denna kalorimeter har två celler, som CTI, men har en anordning som gör det möjligt att bestämma temperaturen och värmeflödena associerade med förändringar i ett material som en funktion av tiden.
Denna teknik ger information om vikningen av proteiner och nukleinsyror, såväl som deras stabilisering..
Applikationer

-Kalorimetri gör det möjligt att bestämma det värmeväxling som sker vid en kemisk reaktion, vilket möjliggör en tydligare förståelse av mekanismen för denna.
-Genom att bestämma materialets specifika värme ger kalorimetri data som hjälper till att identifiera det.
-Eftersom det finns en direkt proportionalitet mellan värmeförändringen av en reaktion och koncentrationen av reaktanterna, kombinerat med det faktum att kalorimetri inte kräver tydliga prover, kan denna teknik användas för att bestämma koncentrationen av ämnen som finns i komplexa matriser..
-Inom kemiteknik används kalorimetri i säkerhetsprocessen såväl som i olika områden av optimeringsprocessen, kemisk reaktion och i manöverenheten..
Användning av isotermisk titreringskalorimetri
-Det samarbetar i upprättandet av enzymverkningsmekanismen, liksom i dess kinetik. Denna teknik kan mäta reaktioner mellan molekyler, bestämma bindningsaffinitet, stökiometri, entalpi och entropi i lösning utan behov av markörer..
-Bedömer interaktionen mellan nanopartiklar och proteiner och är tillsammans med andra analysmetoder ett viktigt verktyg för att registrera konformationsförändringar i proteiner.
-Den har tillämpning vid bevarande av mat och grödor.
-När det gäller konservering av mat kan du bestämma dess försämring och hållbarhet (mikrobiologisk aktivitet). Den kan jämföra effektiviteten hos olika metoder för konservering av livsmedel och kan bestämma den optimala dosen konserveringsmedel samt nedbrytningen i förpackningskontrollen.
-När det gäller grönsaksgrödor kan du studera fröets spiring. När de befinner sig i vatten och i närvaro av syre släpper de ut värme som kan mätas med en isotermisk kalorimeter. Undersök åldern och felaktig lagring av fröna och studera deras tillväxthastighet inför variationer i temperatur, pH eller olika kemikalier.
-Slutligen kan du mäta jordens biologiska aktivitet. Dessutom kan det upptäcka sjukdomar.
Användning av kalorimetri för differentiell skanning
-Tillsammans med isotermisk kalorimetri har det gjort det möjligt att studera interaktionen mellan proteiner och deras ligander, den allosteriska interaktionen, vikningen av proteiner och mekanismen för deras stabilisering..
-Värmen som frigörs eller absorberas under en molekylär bindningshändelse kan mätas direkt.
-Differentialskanningskalorimetri är ett termodynamiskt verktyg för direkt etablering av upptagningen av värmeenergi som förekommer i ett prov. Detta gör det möjligt att analysera de faktorer som är involverade i proteinmolekylens stabilitet..
-Han studerar också termodynamiken för nukleinsyrans vikande övergång. Tekniken möjliggör bestämning av den oxidativa stabiliteten hos linolsyra som är isolerad och kopplad till andra lipider.
-Tekniken tillämpas vid kvantifiering av nanosolider för farmaceutisk användning och vid termisk karakterisering av nanostrukturerade lipidtransportörer..
Referenser
- Whitten, K., Davis, R., Peck, M. och Stanley, G. Kemi. (2008). 8: e upplagan Cengage Learning Redigera.
- Rehak, N. N. och Young, D. S. (1978). Potentiella tillämpningar av kalorimetri i det kliniska laboratoriet. Clin. Chem. 24 (8): 1414-1419.
- Stossel, F. (1997). Tillämpningar av reaktionskalorimetri inom kemiteknik. J. Therm. Anal. 49 (3): 1677-1688.
- Weber, P. C. och Salemme, F. R. (2003). Tillämpningar av kalorimetriska metoder för läkemedelsupptäckt och studier av proteininteraktioner. Curr. Opin. Struct. Biol. 13 (1): 115-121.
- Gill, P., Moghadem, T. och Ranjbar, B. (2010). Differentiell scanning kalorimetriska tekniker: tillämpningar inom biologi och nanovetenskap. J. Biol. Tech. 21 (4): 167-193.
- Omanovic-Miklicanin, E., Manfield, I. och Wilkins, T. (2017). Tillämpningar av isotermisk titreringskalorimetri vid utvärdering av protein-nanopartikelinteraktioner. J. Therm. Anal. 127: 605-613.
- Community College Consortium for Bioscience Credentials. (7 juli 2014). Kaffekopp kalorimeter. [Figur]. Hämtad den 7 juni 2018 från: commons.wikimedia.org



Ingen har kommenterat den här artikeln än.