
Dihydroxiacetonfosfat (DHAP) egenskaper och tillämpningar
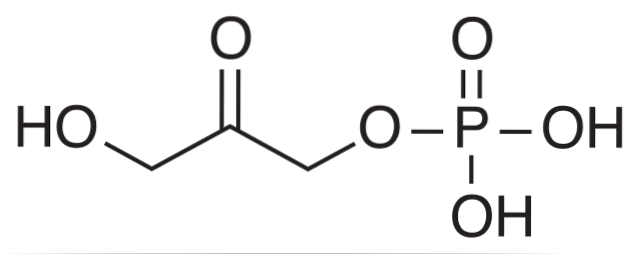
De dihydroxiacetonfosfat Det är en kemisk förening förkortad under akronymen DHAP. Det är en mellanhand i vissa metaboliska vägar för levande organismer, såsom glykolytisk nedbrytning eller glykolys, såväl som i Calvin-cykeln i växter.
Biokemiskt är DHAP produkten av effekten av ett aldolaseenzym på fruktos-1,6-bisfosfat (FBP), vilket orsakar en aldolytisk nedbrytning vilket resulterar i två trekolföreningar: DHAP och glyceraldehyd 3-fosfat (GAP).
I Calvin-cykeln utför aldolas den omvända reaktionen och kondenserar DHAP-molekyler med GAP-molekyler för att bilda en hexos..
Artikelindex
- 1 Funktioner
- 2 DHAP i glykolys
- 2.1 Aldolasereaktion
- 2.2 Reaktion av TIM
- 3 DHAP i Calvin-cykeln
- 4 DHAP i glukoneogenes
- 5 Referenser
Egenskaper
DHAP klassificeras inom de molekyler som kallas ketotrioser. Dessa är monosackarider som består av en kedja av tre kol (trioser) med karbonylgruppen på det centrala kolet (C2).
GAP och DAHP är funktionella isomerer och utgör de enklaste kolhydraterna inom biologiskt aktiva organiska molekyler.
Även om den kemiska strukturen hos många vanliga kolhydrater såsom GAP och DHAP är aldehyder och ketoner, ges de termen kolhydrat, med hänvisning till direkta derivat av sackarider.
DHAP i glykolys
I glykolys försämrar en serie reaktioner glukos till pyruvat. Denna nedbrytning sker successivt i 10 på varandra följande steg, där olika enzymer ingriper och en mängd mellanprodukter produceras, som alla fosforyleras..
DHAP uppträder i glykolys i den fjärde reaktionen av denna process, som består av nedbrytningen av FBP i två kolhydrater av tre kol (trioser), varav endast GAP fortsätter glykolyssekvensen, medan DHAP behöver omvandlas till GAP för att följa denna väg.
Denna reaktion katalyseras av ett aldolas (fruktosbisfosfat aldolas), som utför en aldol-klyvning mellan C3- och C4-kolerna i FBP.
Denna reaktion inträffar endast om hexosen som ska delas upp har en karbonylgrupp vid C2 och en hydroxyl vid C4. Av denna anledning inträffade isomerisering av glukos-6-fosfat (G6P) till fruktos-6-fosfat (F6P) tidigare..
DHAP är också inblandat i den femte glykolysreaktionen, det vill säga dess isomerisering till GAP av enzymet triosfosfatisomeras eller TIM. Med denna reaktion är den första fasen av glukosnedbrytning slutförd..
Aldolasereaktion
I aldolnedbrytningen produceras två mellanprodukter, där DHAP utgör 90% av blandningen i jämvikt.
Det finns två typer av aldolaser: a) aldolas av typ I finns i djur- och växtceller och kännetecknas av bildandet av en Schiff-bas mellan det enzymatiska aktiva stället och karbonylen i FBP. b) Typ II aldolas finns i vissa bakterier och svampar, den har en metall i det aktiva stället (vanligtvis Zn).
Aldolklyvningen börjar med vidhäftningen av substratet till det aktiva stället och avlägsnandet av en proton från β-hydroxylgruppen och bildar den protonerade Schiff-basen (iminiumkatjon). Nedbrytningen av C3- och C4-kolet ger frisättning av GAP och bildandet av en mellanprodukt som kallas enamin..
Enaminen stabiliseras därefter, så en iminiumkatjon bildas som hydrolyseras, med vilken DHAP slutligen frigörs och det fria enzymet regenereras sålunda.
I celler med aldolas av typ II sker inte bildandet av Schiff-basen, utan är en tvåvärd metallisk katjon, i allmänhet Zntvå+, den som stabiliserar den mellanliggande enaminen för att frigöra DHAP.
TIM-reaktion
Som nämnts är jämviktskoncentrationen av DHAP högre än för GAP, så att DHAP-molekyler transformeras till GAP eftersom den senare används i följande glykolysreaktion..
Denna omvandling sker tack vare TIM-enzymet. Detta är den femte reaktionen av den glykolytiska nedbrytningsprocessen och i den blir C1- och C6-kolerna av glukos C3-kolerna i GAP, medan C2- och C5-kolerna blir C2 och C3 och C4 för glukos blir de C1 av GAP.
TIM-enzymet anses vara det "perfekta enzymet" eftersom diffusion styr reaktionshastigheten, vilket innebär att produkten bildas lika snabbt som enzymets aktiva plats och dess substrat kommer ihop..
I reaktionen av transformation av DHAP till GAP bildas en mellanprodukt som kallas enediol. Denna förening kan ge upp protonerna från hydroxylgrupperna till en rest av det aktiva stället för TIM-enzymet..
DHAP i Calvin-cykeln
Calvin-cykeln är den fotosyntetiska kolreduktionscykeln (PCR) som utgör den mörka fasen av fotosyntesprocessen i växter. I detta steg används produkterna (ATP och NADPH) som erhålls i processens lätta fas för att framställa kolhydrater..
I denna cykel bildas sex GAP-molekyler, varav två transformeras till DHAP genom isomerisering, tack vare TIM-enzymets verkan, i en omvänd reaktion mot den som sker vid nedbrytningen av glykolys. Denna reaktion är reversibel, även om jämvikten, i fallet med denna cykel och till skillnad från glykolys, förskjuts mot omvandlingen av GAP till DHAP.
Dessa DHAP-molekyler kan sedan följa två vägar, en är en aldolkondensation katalyserad av ett aldolas, i vilken den kondenserar med en GAP-molekyl för att bilda FBP.
Den andra reaktionen som en av DHAP: erna kan ta är en fosfathydrolys katalyserad av ett sedoheptulosbisfosfatas. I den här sista vägen reagerar den med en erytros för att bilda sedoheptulos 1,7-bisfosfat.
DHAP i glukoneogenes
Vid glukoneogenes omvandlas vissa icke-glukidföreningar såsom pyruvat, laktat och vissa aminosyror till glukos. I denna process uppträder DHAP igen genom isomerisering av en GAP-molekyl genom TIM-verkan och sedan genom en aldolkondensation blir den FBP.
Referenser
- Bailey, P. S. och Bailey, C. A. (1998). Organisk kemi: begrepp och tillämpningar. Ed Pearson Education.
- Devlin, T. M. (1992). Lärobok för biokemi: med kliniska korrelationer. John Wiley & Sons, Inc..
- Garrett, R. H., & Grisham, C. M. (2008). Biokemi. Ed. Thomson Brooks / Cole.
- Nelson, D. L., & Cox, M. M. (2006). Lehninger Principles of Biochemistry 4: e upplagan. Ed Omega. Barcelona.
- Rawn, J. D. (1989). Biokemi (Nr 577.1 RAW). Ed. Interamericana-McGraw-Hill
- Voet, D., & Voet, J. G. (2006). Biokemi. Panamerican Medical Ed..



Ingen har kommenterat den här artikeln än.