
Crystal Structure Structure, Typer och exempel
De kristallstruktur Det är ett av de fasta tillstånden som atomer, joner eller molekyler kan anta i naturen, vilket kännetecknas av att ha en hög rumslig ordning. Med andra ord är detta ett bevis på den "korpuskulära arkitekturen" som definierar många kroppar med glasiga och glänsande utseende..
Vad främjar eller vilken kraft är ansvarig för denna symmetri? Partiklarna är inte ensamma, men de interagerar med varandra. Dessa interaktioner förbrukar energi och påverkar stabiliteten hos de fasta ämnena, så att partiklarna försöker anpassa sig själva för att minimera denna energiförlust..

Så deras inneboende natur leder dem till att placera sig i det mest stabila rumsliga arrangemanget. Till exempel kan detta vara den där avstötningarna mellan joner med samma laddningar är minimala, eller där vissa atomer - såsom metalliska - också upptar största möjliga volym i sina förpackningar..
Ordet "kristall" har en kemisk betydelse som kan förklaras felaktigt för andra kroppar. Kemiskt hänvisar det till en ordnad struktur (mikroskopiskt) som till exempel kan bestå av DNA-molekyler (en DNA-kristall).
Det används dock populärt för att hänvisa till glasartade föremål eller ytor, såsom speglar eller flaskor. Till skillnad från äkta kristaller består glas av en amorf struktur (oordning) av silikater och många andra tillsatser..
Artikelindex
- 1 Struktur
- 1.1 Enhetscell
- 2 typer
- 2.1 Enligt dess kristallina system
- 2.2 Enligt dess kemiska natur
- 3 Exempel
- 3.1 K2Cr2O7 (trikliniksystem)
- 3.2 NaCl (kubiskt system)
- 3.3 ZnS (wurtzit, sexkantigt system)
- 3.4 CuO (monokliniskt system)
- 4 Referenser
Strukturera
I bilden ovan illustreras några smaragdpärlor. Precis som dessa uppvisar många andra mineraler, salter, metaller, legeringar och diamanter en kristallstruktur; men vilket förhållande har dess ordning med symmetrin?
Om en kristall, vars partiklar kan observeras med blotta ögat, appliceras symmetrioperationer (invertera den, rotera den i olika vinklar, reflektera den i ett plan, etc.), kommer det att konstateras att den förblir intakt i alla dimensioner av rymden..
Motsatsen inträffar för en amorf fast substans, från vilken olika ordningar erhålls genom att den utsätts för en symmetrioperation. Dessutom saknar den strukturella repetitionsmönster, vilket visar slumpmässigheten i fördelningen av dess partiklar..
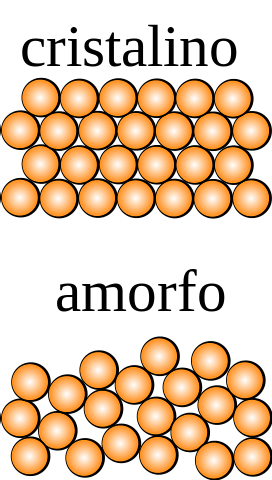
Vad är den minsta enhet som utgör strukturmönstret? I den övre bilden är det kristallina fasta ämnet symmetriskt i rymden, medan det amorfa inte är det..
Om rutor ritades som slutna orange sfärer och symmetrioperationer applicerades på dem, skulle det konstateras att de genererar andra delar av kristallen.
Ovanstående upprepas med mindre och mindre rutor tills det finns en som är asymmetrisk; den som föregår den i storlek är per definition enhetscellen.
Enhetscell
Enhetscellen är det minsta strukturella uttrycket som möjliggör fullständig reproduktion av det kristallina fasta ämnet. Från detta är det möjligt att montera glaset och flytta det i alla rymdriktningar.
Det kan betraktas som en liten låda (bagageutrymme, skopa, behållare etc.) där partiklarna, representerade av sfärer, placeras enligt ett fyllningsmönster. Dimensionerna och geometrin för denna ruta beror på längderna på dess axlar (a, b och c) samt vinklarna mellan dem (α, β och γ).
Den enklaste av alla enhetsceller är den med den enkla kubiska strukturen (övre bild (1)). I detta upptar sfärernas centrum hörnen på kuben, fyra vid basen och fyra i taket..
I detta arrangemang upptar sfärerna bara 52% av kubens totala volym, och eftersom naturen avskyr ett vakuum, antar inte många föreningar eller element denna struktur..
Men om sfärerna är ordnade i samma kub på ett sådant sätt att man upptar mitten (kubiskt centrerad i kroppen, bcc), blir det en mer kompakt och effektiv packning (2). Nu upptar sfärerna 68% av den totala volymen.
Å andra sidan, i (3) upptar ingen sfär mitten av kuben, utan centrum av dess ansikten, och de upptar alla upp till 74% av den totala volymen (ansiktscentrerad kubik, cc).
Således kan man se att för samma kub kan andra arrangemang erhållas, varierande på vilket sfärerna packas (joner, molekyler, atomer, etc.).
Typer
Kristallstrukturer kan klassificeras enligt deras kristallsystem eller partiklarnas kemiska natur..
Till exempel är det kubiska systemet det vanligaste av alla och många kristallina fasta ämnen styrs av det; Emellertid gäller samma system för både joniska och metalliska kristaller..
Enligt dess kristallina system
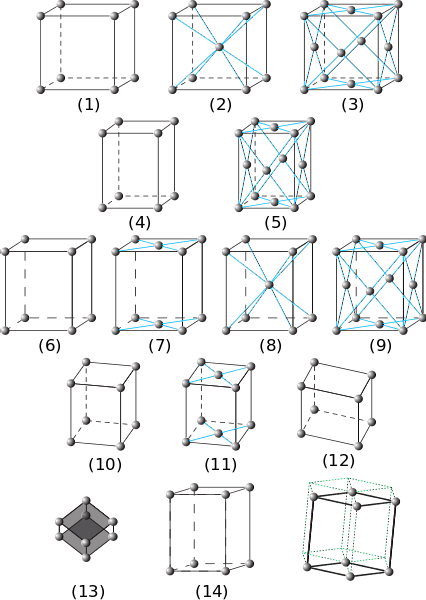
I den föregående bilden representeras de sju huvudkristallsystemen. Det kan noteras att det faktiskt finns fjorton av dessa, som är produkten av andra former av förpackningar för samma system och utgör Bravais-nätverk.
Från (1) till (3) finns kristaller med kubiska kristallsystem. I (2) observeras (av de blå ränderna) att sfären i mitten och hörnen samverkar med åtta grannar, så sfärerna har ett koordinationsnummer på 8. Och i (3) är koordinationsnumret 12 ( för att se det måste du duplicera kuben i vilken riktning som helst).
Elementen (4) och (5) motsvarar enkla och ansiktscentrerade tetragonala system. Till skillnad från kubik är dess c-axel längre än a- och b-axlarna.
Från (6) till (9) finns de ortorombiska systemen: från enkla och centrerade på baserna (7), till de som är centrerade på kroppen och ansiktena. I dessa α är β och γ 90º, men alla sidor har olika längd.
Figurerna (10) och (11) är de monokliniska kristallerna och (12) är den trikliniska, den sista uppvisar ojämlikheter i alla dess vinklar och axlar..
Element (13) är det rombohedrala systemet, analogt med det kubiska men med en vinkel γ som skiljer sig från 90 °. Slutligen finns de sexkantiga kristallerna
Förskjutningarna av elementen (14) härrör från det sexkantiga prisma som spåras av de gröna prickade linjerna.
Enligt dess kemiska natur
- Om kristallerna består av joner är de joniska kristaller som finns i salter (NaCl, CaSO4, CuCltvå, KBr, etc.)
- Molekyler som glukos bildar (närhelst de kan) molekylära kristaller; i detta fall de berömda sockerkristallerna.
- Atomer vars bindningar i huvudsak är kovalenta bildar kovalenta kristaller. Så är fallet med diamant eller kiselkarbid.
- Metaller som guld bildar också kompakta kubiska strukturer som utgör metalliska kristaller..
Exempel
KtvåCrtvåELLER7 (trikliniksystem)
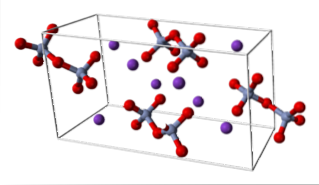
NaCl (kubiskt system)
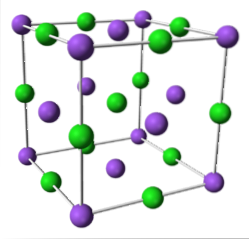
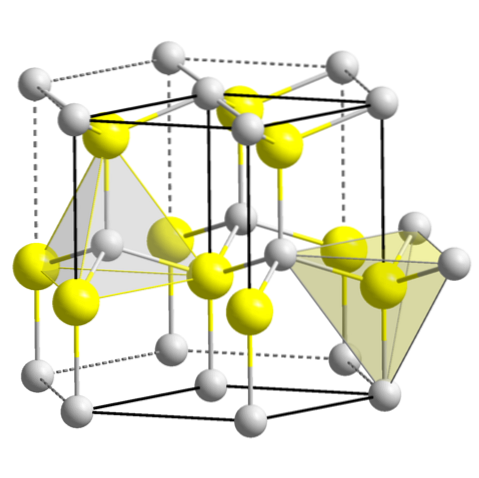
ZnS (wurtit, sexkantigt system)
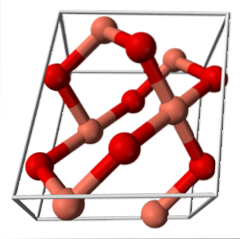
CuO (monokliniskt system)
Referenser
- Quimitube. (2015). Varför "kristaller" inte är kristaller. Hämtad den 24 maj 2018 från: quimitube.com
- Pressböcker. 10.6 Gitterstrukturer i kristallina fasta ämnen. Hämtad den 26 maj 2018 från: opentextbc.ca
- Academic Resource Center för Crystal Structures. [PDF]. Hämtad den 24 maj 2018 från: web.iit.edu
- Ming. (30 juni 2015). Typer kristallstrukturer. Hämtad den 26 maj 2018 från: crystalvisions-film.com
- Helmenstine, Anne Marie, Ph.D. (31 januari 2018). Typer av kristaller. Hämtad den 26 maj 2018 från: thoughtco.com
- KHI. (2007). Kristallina strukturer. Hämtad den 26 maj 2018 från: folk.ntnu.no
- Paweł Maliszczak. (25 april 2016). Grova smaragdkristaller från Panjshir Valley Afghanistan. [Figur]. Hämtad den 24 maj 2018 från: commons.wikimedia.org
- Napy1kenobi. (26 april 2008). Bravais-galler. [Figur]. Hämtad den 26 maj 2018 från: commons.wikimedia.org
- Användare: Sbyrnes321. (21 november 2011). Kristallint eller amorft. [Figur]. Hämtad den 26 maj 2018 från: commons.wikimedia.org



Ingen har kommenterat den här artikeln än.