
Vad är diatomiska element? (Exempel)
De diatomiska element, Även kallade homonukleära diatomiska molekyler, de består av bara två atomer av samma kemiska element. Vissa element kan inte existera på egen hand, även om de är isolerade från någon annan typ av atom.
Element av denna typ kommer att kombineras med atomer av samma element för att vara stabila. Med andra ord kan väte, ett diatomiskt element, inte vara av sig självt. Det kan inte bara existera H.
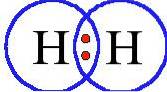
Väte är så reaktivt att när det isoleras från allt utom väte, kommer det att kombineras till en diatomisk (två-atom) molekyl. Därför finns vätgas, som ibland används som bränsle, som Htvå.
Diatomiska molekyler
Diatomiska molekyler innehåller två atomer som är kemiskt bundna. Om de två atomerna är identiska, såsom syremolekylen (Otvå), utgör en homonukleär diatomisk molekyl, medan om atomerna är olika, som i kolmonoxid (CO) -molekylen, bildar den en heteronukleär diatomisk molekyl.
Molekyler som innehåller mer än två atomer kallas polyatomiska molekyler, till exempel koldioxid (COtvå) och vatten (HtvåELLER). Polymermolekyler kan innehålla tusentals komponentatomer.
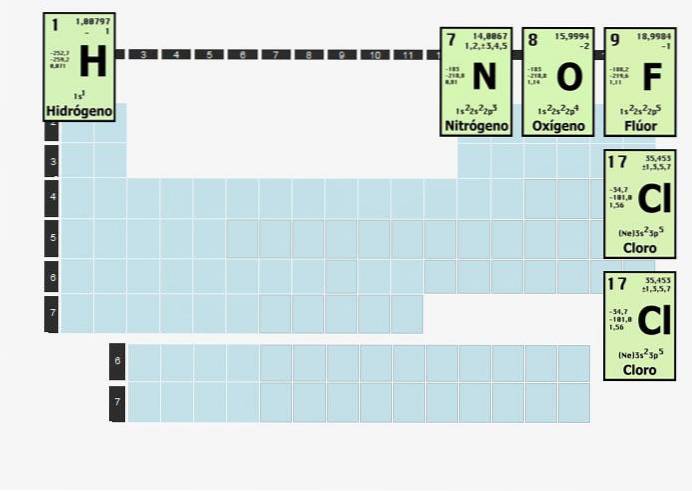
Det finns sju element som utgör diatomiska molekyler. Följande 5 elementgaser finns som diatomiska molekyler vid rumstemperatur och tryck:
-Väte - Htvå
-Kväve - Ntvå
-Syre - Otvå
-Fluor - Ftvå
-Klor - Cltvå
Brom och jod förekommer vanligen i flytande form, men också som diatomiska gaser vid något högre temperaturer, vilket gör totalt 7 diatomiska element..
-Brom - Brtvå
-Jod - jagtvå
Diatomiska element är halogener (fluor, klor, brom, jod) och grundämnen med en -gen-slutning (väte, syre, kväve). Astatin är en annan halogen, men dess beteende är okänt..
Egenskaper hos diatomiska element
Alla diatomiska molekyler är linjära, vilket är det enklaste rumsliga arrangemanget av atomer.
Det är bekvämt och vanligt att representera en diatomisk molekyl som två punktsmassor (de två atomerna) förbundna med en masslös fjäder..
Energierna som är involverade i molekylens rörelser kan delas in i tre kategorier:
- Translationsenergierna (molekylen som rör sig från punkt A till punkt B)
- Rotationsenergier (molekylen roterar runt sin axel)
- Vibrationsenergier (molekyler som vibrerar på olika sätt)
Alla diatomiska element är gaser vid rumstemperatur med undantag av brom och jod som är flytande (jod kan till och med vara i fast tillstånd), och alla med undantag av syre och kväve är kopplade genom en enda bindning..
Syremolekylen har sina två atomer förenade med en dubbelbindning och kvävemolekylen med en trippelbindning.
Några diatomiska element
Väte
Väte (Htvå), med atomnummer 1, är en färglös gas som inte formellt upptäcktes som ett element av Henry Cavendish förrän 1766, men hittades av misstag ungefär hundra år tidigare av Robert Boyle.
Det är en färglös, luktfri, giftfri gas som finns naturligt i vårt universum. Att vara det första elementet i det periodiska systemet, är väte det lättaste och mest rikliga av alla kemiska element i universum eftersom det utgör 75% av dess massa..
Kväve
Kväve (Ntvå) har ett atomnummer på sju och utgör cirka 78,05% av jordens atmosfär i volym.
Det är en luktfri, färglös och mestadels inert gas, och den förblir färglös och luktfri i flytande tillstånd..

Syre
Syre (Otvå) har ett atomnummer på åtta. Denna färglösa, luktfria gas har åtta protoner i kärnan och är ljusblå i sina flytande och fasta tillstånd..
En femtedel av jordens atmosfär består av syre och det är det tredje rikaste elementet i universum i massa..
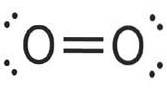
Syre är det vanligaste masselementet i jordens biosfär. Den höga syrekoncentrationen i atmosfären är resultatet av jordens syrgascykel, som främst drivs av fotosyntes i växter..
Fluor
Fluor (Ftvå) har ett atomnummer på nio och är det mest reaktiva och elektronegativa av alla element. Detta icke-metalliska element är en blekgul gas som ingår i halogengruppen.
George Gore var tydligen den första forskaren som isolerade fluor, men hans experiment exploderade när fluor som producerades reagerade med väte..
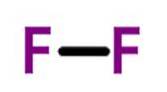
1906 tilldelades Ferdinand Frederic Henri Moissan Nobelpriset i kemi för sitt arbete med isolering av fluor 1886. Det är det mest elektronegativa elementet i det periodiska systemet..
Klor
Klor (Cltvå) är medlem i halogengruppen med ett atomnummer på sjutton. En av dess former, NaCl, har använts sedan urminnes tider.

Klor har använts i tusentals år i många andra former, men det namngavs inte förrän 1810 av Sir Humphry Davy..
Klor i sin rena form är gulgrönt, men dess vanliga föreningar är vanligtvis färglösa..
Brom
Brom (Brtvå) har ett atomnummer på trettiofem. Det är en tung mörkbrun vätska, det enda icke-metalliska elementet som är en vätska.

Brom upptäcktes av Antoine J. Balard 1826. Det användes för viktiga ändamål långt innan det formellt upptäcktes..
Jod
Jod (jagtvå) har ett atomnummer på femtiotre, med femtiotre protoner i atomens kärna. Det är en blåsvart icke-metall som spelar en mycket viktig roll i organisk kemi..
Jod upptäcktes 1811 av Barnard Courtois. Han kallade det jod från det grekiska ordet "ioder" som betyder violett. Det är en solid blå-svart.
Jod spelar en mycket viktig roll i biologin hos alla levande organismer eftersom dess brist leder till sjukdomar som hypertyreoidism och hypotyreoidism.
Referenser
- (S.F.). Homonukleära diatomiska molekyler. Återställd från boundless.com.
- Klorfakta. (S.F.). Återställd från softschools.com.
- Diatomiska element. (S.F.). Återställd från ths.talawanda.org.
- Encyclopædia Britannica. (2016, 14 september). Molekyl. Återställd från britannica.com.
- Helmenstine, A. (2014, 28 september). Diatomiska element. Återställd från sciencenotes.org.
- Helmenstine, A. M. (2017, 29 mars). Vad är de sju diatomiska elementen? Återställd från thoughtco.com.
- Syre fakta. (S.F.). Återställd från softschools.com.
- Royal Society of Chemistry. (2015). molekylär jod. Återställd från chemspider.com.



Ingen har kommenterat den här artikeln än.