
Kalciumsilikategenskaper, struktur, erhållning, användning
De kalciumsilikat är namnet på en grupp kemiska föreningar bildade av kalciumoxid (CaO) och kiseldioxid (SiOtvå). Den allmänna formeln för dessa föreningar är xCaO • ySiOtvå• Z HtvåELLER.
De är vita eller gulvita fasta ämnen. De kan vara vattenfria, det vill säga utan vatten (H.tvåO) i dess struktur, eller kan innehålla den. De är en del av flera typer av mineraler i naturen.

Kalciumsilikater är olösliga i vatten, men när de sammanfogar det bildar de hydratiserade geler (material som gelatin) som är mycket hårda, beständiga och nästan vattentäta när de härdar.
Detta har lett till att de används i byggbranschen, eftersom de används i cement, tegel och fuktisolerande paneler. De är också en del av material för att läka perforeringar i tänderna och det har även studerats att använda dem vid regenerering av ben, det vill säga som ett biomaterial.
De har föreslagits för att minska föroreningarna från vissa metallurgiska industrier. De används också som friktionsgeneratorer i fordonsbromsar och kopplingar..
Artikelindex
- 1 Struktur
- 2 Nomenklatur
- 3 fastigheter
- 3.1 Fysiskt tillstånd
- 3.2 Molekylvikt
- 3.3 Smältpunkt
- 3.4 Densitet
- 3.5 Löslighet
- 3,6 pH
- 3.7 Övriga egenskaper
- 4 Skaffa
- 5 användningsområden
- 5.1 För att få tegelstenar
- 5.2 I Portland cement
- 5.3 Att immobilisera radioaktivt avfall
- 5.4 Som isolering för byggnader
- 5.5 Att minska föroreningar i metallindustrin
- 5.6 I biomaterial
- 5.7 I biodentin
- 5.8 Andra applikationer
- 6 Referenser
Strukturera
Kalciumsilikat kan innehålla en varierande mängd kalciumoxid (CaO) och kiseldioxid (SiO)två). Dess allmänna formel är:
xCaO • ySiOtvå• Z HtvåELLER
där x, y och z är tal som kan ha olika värden.
Mängden CaO måste vara mellan 3% och 35% (i vikt på torr basis) och SiO-haltentvå Det bör vara 50-95% (i vikt på torr basis). De kan vara vattenfria (utan vatten i dess struktur, det vill säga z = 0 i formeln) eller de kan hydratiseras (med vatten är dess konformation).
Nomenklatur
- Kalciumsilikat
- Kiselsyrakalciumsalt
- Kalciumoxid och kisel
Egenskaper
Fysiskt tillstånd
Mycket fin vit eller benvit fast substans.
Molekylvikt
Kalciummetasilikat CaO • SiOtvå eller CaSiO3 = 116,16 g / mol
Smältpunkt
CaSiO kalciummetasilikat3 = 1540 ° C
Densitet
CaSiO Kalciummetasilikat3 = 2,92 g / cc
Löslighet
Olöslig i vatten och etanol.
pH
En lera framställd med 5% kalciumsilikat kan ha ett pH på 8,4-12,5.
Andra egenskaper
Kalciumsilikat kan hydratiseras (med vatten i molekylen) eller vattenfritt (utan vatten i molekylen) med olika proportioner av kalcium i form av kalciumoxid CaO och kiseldioxid i form av kiseldioxid SiOtvå.
Den har hög vattenabsorptionsförmåga. Kalciummetasilikat (CaO • SiOtvå eller CaSiO3) sticker ut för sin briljans och vithet, låg luftfuktighet, lågt flyktigt innehåll och god oljeabsorption.

Bland hydraterna av kalciumsilikat är de som bildas genom att tillsätta vatten till CatvåJa5 och till Ca3Ja5. Hydreringsprodukterna för dessa två föreningar är de vanligaste i vissa typer av cement..
Erhållande
Kalciumsilikat erhålls på olika sätt genom att reagera kiselhaltigt material (såsom kiselgur) och kalciumföreningar (såsom kalciumhydroxid (Ca (OH))två).
Kalciumsilikat kan framställas till exempel genom kalcinering av kalciumoxid (CaO) med kiseldioxid (SiOtvå) vid förhöjda temperaturer.
När reaktionen utförs med ett molförhållande 1: 1 (detta betyder att det finns samma antal CaO-molekyler som SiOtvå) resulterar i kalciummetasilikat CaSiO3 o CaO • SiOtvå:
CaO + SiOtvå + värme → CaSiO3
Applikationer
För att få tegelstenar
Med kalciumsilikat tillverkas enheter eller tegelstenar för konstruktion. De erhålls med fint kiselhaltigt material och kalk eller hydratiserad kalk. Inerta pigment kan tillsättas för att ge tegelstenen en annan färg.
Enheterna formas under tryck och härdas i en autoklav (ångugn) vid 170 ° C i 4-6 timmar. Under härdningen reagerar en del kalk med det kiselhaltiga materialet för att bilda ett kalciumsilikathydrat, som håller tegelstenen ihop..

Emellertid tenderar kalciumsilikatsten att expandera och krympa mer än lertegel, vilket ibland kan orsaka sprickbildning i murverket..
Detta har väckt uppmärksamhet och de har ansetts vara potentiellt farliga.
I Portland cement
Kalciumsilikater är en del av Portlandcement, som är ett mycket använt material inom byggindustrin.
Portlandcement är ett hydrauliskt cement som produceras av pulveriserande material som huvudsakligen bildas av hydratiserade kalciumsilikater och kalciumsulfat CaSO4 (kasta).

Det hårdnar snabbt på grund av hydratiseringsreaktionen som genererar en hydratiserad kalciumsilikatgel. Detta resulterar i ett starkt, tätt och låggenomsläppligt material (som inte släpper igenom vatten).
De silikater som den innehåller är trikalciumsilikat Ca3Ja5 o 3CaO.SiOtvå och dikalciumsilikat CatvåJa4 eller 2CaO.SiOtvå.
Att immobilisera radioaktivt sopor
Kalciumsilikater i cement kan variera i viktprocent. Portlandcementens sammansättning kan förändras beroende på vilken typ av konstruktion som den är avsedd för..
Vissa typer av detta cement används för att immobilisera radioaktivt avfall så att det inte skadar människor eller miljön..
Som isolering för byggnader
Kalciumsilikat används för att erhålla mineralskumskivor eller isolerande mineralskivor.

Dessa tjänar till att isolera väggarna från fukt. CaO och SiO blandastvå med vatten och 3-6% cellulosa tillsätts, vilket förbättrar kanternas flexibilitet och stabilitet.
Det resulterande slammet hälls i formar och upphettas sedan med ånga vid högt tryck och temperatur i en speciell ångugn som kallas en autoklav..
Resultatet är ett styvt, mycket fint porskum som skärs i ark eller brädor och behandlas med speciella tillsatser så att det kan stöta bort vatten..
Kalciumsilikatskum används inom byggsektorn, särskilt för att isolera väggar och förbättra skyddet mot fukt, vilket är användbart särskilt vid renovering av gamla byggnader.
För att minska föroreningar i metallindustrin
Dicalcium Silicate CatvåJa4 eller 2CaO.SiOtvå som finns i slagg eller avfall från stålproduktion har använts för att fälla upp lösta metaller i sura avlopp från andra metallurgiska processer.
Utfällning betyder att den upplösta metallen blir en del av en fast förening som går till botten av behållaren och kan samlas upp.

CatvåJa4 närvarande i stålslagg reagerar med vatten och producerar Ca (OH)två som har förmågan att neutralisera surheten hos sura lösningar av metaller från andra processer:
2 CatvåJa4 + 4 timmartvåO → 3CaO.2SiOtvå.3HtvåO + Ca (OH)två
Förutom att neutralisera kan kalciumsilikatföreningen adsorbera några av metalljoner Mtvå+ genom utbyte med kalciumjonen Catvå+. Här är en översikt:
≡Si-O-Ca + Mtvå+ → ≡Si-O-M + Catvå+
Den fasta föreningen innehållande metallen kan sedan användas för ett annat ändamål och kastas inte. Detta är ett exempel på industriell ekologi.
I biomaterial
Kalciumsilikatkeramik började testas som biomaterial sedan 1990. De har studerats för deras potentiella användning vid regenerering av benvävnad på grund av deras bioaktivitet överlägsen andra material..
Detta tillskrivs det faktum att de har kisel (Si), vilket spelar en viktig roll i de mekanismer som leder till bildandet av nytt ben..
Kalciumsilikatbaserade cement har förmågan att inducera bildandet av en kalciumfosfat / apatitbeläggning när de nedsänks i biologiska vätskor och främja vävnadsregenerering..
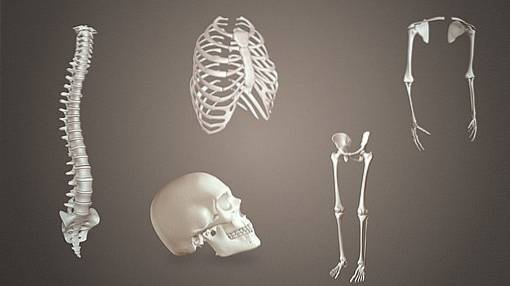
Av dessa skäl betraktas det som ett lämpligt material för benreparation..
I biodentinen
Kalciumsilikat är en del av biodentin. Detta är ett material som används för att reparera tandperforationer, benresorptioner och som fyllning för änden av tänderots rötter..
Biodentin är ett bioaktivt cement med låg porositet som har större mekanisk hållfasthet eller hårdhet än andra material och liknar dentin.
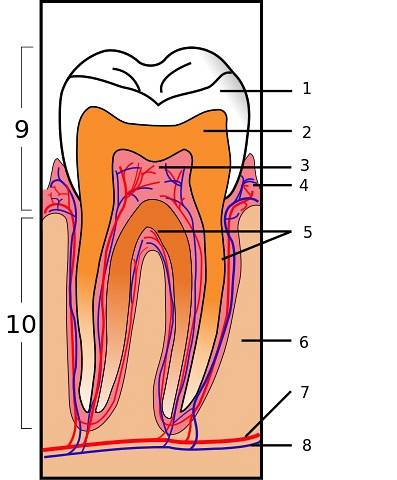
Den består av trikalciumsilikat (Ca3Ja5dikalciumsilikat (CatvåJa5), kalciumkarbonat (CaCO3) och zirkoniumoxid. När det blandas med vatten bildar kalciumsilikater en klibbig hydratiserad gel som efter ett tag stelnar och skapar en hård struktur..
Det utövar en positiv effekt på cellerna i tandmassan och accelererar bildandet av broar i dentinet, där styrkan hos dess bindningar, dess mikrohårdhet och motstånd mot kompression framhävs..
Andra appar
Kalciumsilikater används också som antiklumpmedel och filterhjälpmedel..
Kalciummetasilikat CaSiO3 används i keramik, i anordningar där friktion krävs, såsom fordonsbromsar och kopplingar, och för att erhålla metaller.
På grund av sin höga ljusstyrka och vithet, CaSiO3 Den används för att fylla färger och plast.
Referenser
- Ropp, R.C. (2013). Grupp 14 (C, Si, Ge, Sn och Pb) Alkaliska jordföreningar. Kalciumsilikater. I Encyclopedia of the Alkaline Earth Compounds. Återställd från sciencedirect.com.
- FAO (2015). Kalciumsilikat. Specifikationer som utarbetats vid 80-taletth JECFA (2015) och publicerad i FAO JECFA Monographs 17. Hämtad från fao.org.
- Harrisson, A.M. (2019). Konstitution och specifikation av Portland Cement. Kalciumsilikathydrat. I Lea's Chemistry of Cement and Concrete (femte upplagan). Återställd från sciencedirect.com.
- Gellert, R. (2010). Oorganiska mineraliska material för isolering i byggnader. Kalciumsilikatskum och mineralskum. I material för energieffektivitet och termisk komfort i byggnader. Återställd från sciencedirect.com.
- Goudouri, O-M. et al. (2016). Karakteriserar nedbrytningsbeteendet hos biokeramiska byggnadsställningar. Apatit / wollastonit byggnadsställningar. I karaktärisering och design av vävnadsställningar. Återställd från sciencedirect.com.
- Rani, P. et al. (2019). Tandmassakappning av nanokompositer. Biodentin. In Applications of Nanocomposite Materials in Dentistry. Återställd från sciencedirect.com.
- Ingham, J.P. (2013). Betongprodukter. Kalciumsilikatenheter. I geomaterial under mikroskopet. Återställd från sciencedirect.com.
- Ojovan, M.I. och Lee, W.E. (2005). Immobilisering av radioaktivt avfall i cement. Hydrauliska cement. I en introduktion till immobilisering av kärnavfall. Återställd från sciencedirect.com.
- Ramachandra Rao, S. (2006). Resursåtervinning och återvinning från metallurgiskt avfall. Kalciumsilikat som utfällningsmedel för upplösta metaller. I avfallshanteringsserien. Återställd från sciencedirect.com.
- Prati, C. och Gandolfi, M.G. (2015). Kaliumsilikatbioaktiva cement: Biologiska perspektiv och kliniska tillämpningar. Dent Mater, 2015 apr; 31 (4): 351-70. Återställd från ncbi.nlm.nih.gov.



Ingen har kommenterat den här artikeln än.