
Alkaner eller mättade kolväteegenskaper, exempel
De alkaner eller mättade kolväten de kännetecknas av att de i sin struktur endast har enkla kovalenta bindningar. Detta innebär att de kolatomer som finns i dessa arter är bundna till det maximala antalet väteatomer med vilka det är möjligt för dem att bilda bindningar, av denna anledning är de kända som mättad.
I universumet av organisk kemi anses alkaner, även kända som paraffiner, vara ganska rikliga och mycket viktiga arter, som tillhör gruppen alifatiska kolväten (som omättade kolväten)..
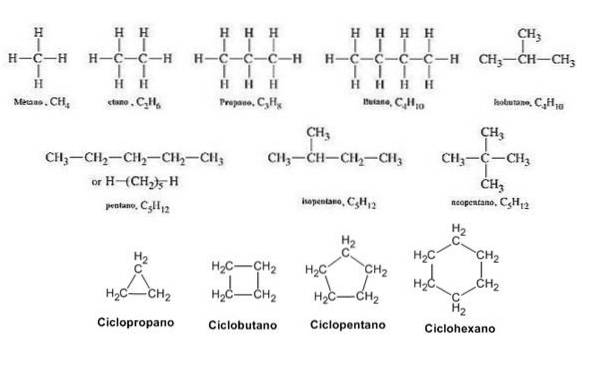
Det enklaste mättade kolvätet som kan bildas tas som ett exempel: metan, en förening som finns i gasfasen under vanliga omgivningsförhållanden (25 ° C och atm), vars formel är CH4.
Som kan ses har den enda kolatomen som finns i denna molekyl fyra enkla bindningar, en med varje väteatom..
Alkener och alkyner har viktiga kommersiella användningsområden, såsom i fallet med eten och propen; men de är också mer reaktiva föreningar än mättade kolväten, vilket gör att de har ett stort antal reaktioner som uppstår från vanliga alkener och alkyner..
Artikelindex
- 1 Nomenklatur för alkaner
- 1.1 Nomenklatur för linjära mättade kolväten
- 1.2 Nomenklatur för grenade mättade kolväten
- 1.3 Nomenklatur för cykliska mättade kolväten
- 2 fastigheter
- 2.1 Geometrisk isomerisering
- 2.2 Surhet
- 2.3 Polaritet
- 2.4 Kok- och smältpunkter
- 3 Exempel på alkaner
- 3.1 Linjära alkaner
- 3.2 Grenade alkaner
- 3.3 Cykloalkaner
- 4 Referenser
Nomenklatur för alkaner
För att korrekt namnge alkaner eller mättade kolväten är det första att komma ihåg att enligt IUPAC (International Union of Pure and Applied Chemistry) bör den systematiska nomenklaturen för de fyra enklaste alkanerna inte tillämpas..
Nomenklatur för linjära mättade kolväten
Dessa föreningar har den allmänna formeln CnH2n + 2, där värdet av n endast kan vara positiva heltal (n = 1,2, ...), och de namnges med hjälp av prefixet som motsvarar antalet kolatomer och suffixet läggs till -år.
Så de första fyra mättade molekylerna är: metan (CH4etan (CtvåH6propan (C3H8) och butan (C4H10).
Till att börja med nomenklaturen för alkanerna som har mellan fem och tio kolatomer räknas antalet av dessa atomer som finns i den längsta kedjan så länge den är kontinuerlig.
Dessutom, om en väteatom subtraheras från en alkan, blir den en substituent, det vill säga en grupp vars ändning ändras -år för -ilo. Till exempel metan (CH4) skulle bli metyl (-CH3) och på liknande sätt med de andra molekylerna.
Med hänsyn till vad som hittills har angetts och tillägget att räkningen alltid måste startas med den kolatom som har närmast substituent, anges substituentens position följt av alkanens namn..
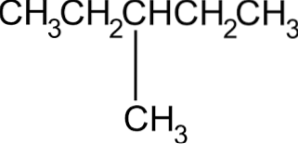
Således kallas ovanstående förening 3-metylpentan.
Grenad mättad kolvätenomenklatur
På liknande sätt har förgrenade alkaner samma allmänna formel som linjära, men med n> 2. Således, varje gång en eller flera atomer eller grupper av atomer ersätter en eller flera väteatomer, måste placeringen av dessa substituenter påpekas..
Om det finns flera grenar av grupper av samma alkyltyp, uttrycken gav-, tri- eller tetra- för att ange mängden av dessa substituenter, föregås av indikeringen av deras positioner och slutar med namnet på alkanen.
I händelse av att substituenterna är olika namnges de enligt alfabetisk ordning och kan också ha icke-kolsubstituenter, såsom klor (Cl) eller nitro (NOtvå).
För att räkna kolantalet i huvudkedjan ges i alla fall det minsta antalet kolet som är kopplat till den lägsta substituenten i alfabetisk ordning och fortsätter i den riktningen.
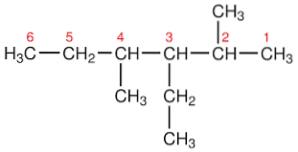
Nomenklatur för cykliska mättade kolväten
Mättade kolväten av cyklisk typ, bättre känd som cykloalkaner har den allmänna formeln CnH2n, där n = 3,4, ...
I dessa organiska molekyler är kolatomerna som utgör den ordnade på ett stängt sätt, det vill säga deras struktur bildar en ring.
För att namnge dessa arter följs riktlinjerna som beskrivs ovan för linjära och grenade alkaner, och läggs bara till prefixet cykel-. Likaså cyklopropan (C3H6) som den enklaste cykloalkanen.
På liknande sätt kan dessa molekyler innehålla mer än en ring integrerad i sin huvudkedja, med minst tre kolatomer och till och med bilda mycket komplexa strukturer..
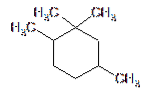
Egenskaper
Mättade kolväten har huvudegenskapen att bilda enkla bindningar mellan deras atomer, vilket gör dem till en mycket stor grupp av molekyler och ger dem ganska specifika egenskaper som beskrivs nedan:
Geometrisk isomerisering
Strukturen hos alkanmolekyler ger förändringar i deras fysiska och kemiska egenskaper på grund av konformationen av de fyra bindningarna som kol kan bilda..
Detta betyder att trots att kolet i dessa molekyler har en hybridisering av sp-typen3, vinklarna mellan deras intilliggande atomer kan variera beroende på typen av atom.
För att förklara det mer exakt har cykloalkaner vridningsvinklar som ger dem en unik egenskap som kallas stereokemi, vilket kan påverka energierna i molekylen och andra faktorer som är inneboende i den, såsom att ge den spektroskopiska och optiska egenskaper..
Aciditet
Mättade kolväten uppvisar en relativt låg reaktivitet mot joniska och andra polära arter. Samtidigt har de praktiskt taget ingen interaktion med sura och alkaliska ämnen..
Polaritet
Alkaner anses vara icke-ledande eftersom de har praktiskt taget ingen polaritet i närvaro av ett elektriskt fält. Således kan inte vätebindningar bildas för att möjliggöra dess löslighet i polära lösningsmedel..
Så de är praktiskt taget lösliga i alla icke-polära lösningsmedel, eftersom de inte kan blandas med polära lösningsmedel som vatten..
Kok- och smältpunkter
I mättade kolväten uppstår intermolekylära interaktioner på grund av van der Waals-krafter, där starkare interaktioner översätts till högre kokpunkter..
En liknande trend observeras för smältpunkter, men detta beror på molekylens förpackningskapacitet..
Eftersom dessa interaktioner är direkt relaterade till artens molekylvikt, desto större blir molekylens kok- och smältpunkter högre..
Genom att ha en styvare struktur som ger dem ett intermolekylärt kontaktplan har cykloalkaner således högre kok- och smältpunkter än deras motsvarande linjära alkaner..
Exempel på alkaner
Linjära alkaner
Metan: Det är en färglös och luktfri gas som förekommer rikligt i naturen och som en produkt av vissa mänskliga aktiviteter. Metan är den enklaste medlemmen av alkaner och är bland de mest potenta av växthusgaserna (Encyclopædia Britannica, 2017).
Etan: det är en gas som huvudsakligen finns i naturgas och används i blandningar med andra gaser för att producera bränslen.
Propan: det är en färglös gas som finns i naturgas och används som bränsle i hem och industrier. Den kemiska formeln för propan är C3H8 och den utökade formeln är CH3CHtvåCHtvå (Propanformel, S.F).
Butan: o n-butan är en av dussintals gaser som extraheras från rå naturgas och kan också produceras från råolja. N-butan är en färglös universalgas. Butan kan användas för uppvärmning, kylning och lättare bränsle.
N-pentan: är en klar färglös vätska med en petroleumliknande lukt. Pentan finns i alkoholhaltiga drycker och humleolja. Denna alkan är en del av vissa bränslen och används som ett speciallösningsmedel i laboratoriet..
N-hexan: Det är en färglös transparent vätska med en petroleumliknande lukt. Finns i citrusfrukter, används den för att extrahera ätliga oljor från frön och grönsaker, som ett speciellt lösningsmedel och som rengöringsmedel.
N-heptan: Det är en färglös transparent vätska med en petroleumliknande lukt. Det finns i kardemumma. Mindre tät än vatten och olösligt i vatten. Ångor tyngre än luft.
N-oktan: är en färglös vätska med bensinlukt. Mindre tät än vatten och olösligt i vatten. Därför flyter den på vattnet. Ger irriterande ånga.
Metylklorid: Det kallas också klormetan, det är en färglös gas. Det är den enklaste haloalkanen, som används vid tillverkning av silikonpolymerer och vid tillverkning av andra kemiska produkter.
Kloroform: det är en färglös, luktande och mycket flyktig vätska som har använts i stor utsträckning för sina bedövningsegenskaper. På grund av dessa egenskaper har det rykte för att kunna bedöva eller slå människor, även när de konsumeras i små doser (MoviesDoes Chloroform verkligen utslagna dig så snabbt som de visar i filmer?, 2016).
Koltetraklorid: även kallad tetraklormetan, en färglös, tät, mycket giftig, flyktig, icke-brandfarlig vätska som har en karakteristisk lukt och används som lösningsmedel.
Kloroetan: är en gas som kondenserar under lätt tryck. Kloroetan används främst för lokal smärtlindring inom idrottsmedicin (National Center for Biotechnology Information., 2017).
Bromoetan: även känd som etylbromid, det är en färglös flyktig vätska, något löslig och tätare än vatten. Ångorna är tyngre än luft. Används för att tillverka läkemedel och som lösningsmedel.
Grenade alkaner
Isobutan: är en färglös gas med en svag petroleumlukt. Den transporteras som en flytande gas under ångtrycket. Kontakt med vätskan kan orsaka frostskador. Tänds lätt.
IsopentanÄven kallad 2-metylbutan, det är en färglös vattenhaltig vätska med en bensinlukt. Flyter i vattnet. Producerar brandfarlig och irriterande ånga (National Center for Biotechnology Information. PubChem Compound Database;, 2017).
2-metylpentan: är en grenad alkan med molekylformeln C6H14. Det är en vattnig vätska med en bensinlukt som flyter på vatten och ger en irriterande ånga.
3, 3-dimetylhexan: finns i örter och kryddor. 3, 3-dimetylhexan är en komponent i Osmanthus fragrans (söt osmanthus) och ginsengolja.
2,3-dimetylhexan: finns i frukt. 2,3-dimetylhexan är en flyktig komponent av stärkelse.
Neopentan: det är en vätska som är mindre tät än vatten. Olösligt i vatten men lösligt i alkohol (National Center for Biotechnology Information., 2015).
2, 2, 4-trimetylpentan: o Isoktan släpps ut i miljön genom tillverkning, användning och bortskaffande av produkter associerade med petroleumsindustrin. 2,2,4-trimetylpentan trängde in i en människas hud och orsakade nekros i huden och vävnaden i handen, vilket krävde operation (National Center for Biotechnology Information., 2017).
Cykloalkaner
Cyklopropan: Det är en färglös gas med en lukt som liknar petroleum. Kontakt med vätskan kan orsaka frostskador. Kan kvävas av luftförskjutning och har en narkotisk effekt i hög koncentration.
Cyklobutan: Gas som kondenseras till en vätska vid 13 ° C. Olöslig i vatten. Löslig i alkohol, aceton och eter.
Cyklopentan: Det är en färglös transparent vätska med en petroleumliknande lukt. Mindre tät än vatten och olöslig i den. Ångorna är tyngre än luft.
Cyklohexan: finns i kålrabi. Tunnare i färgadditivblandningar för livsmedelsbruk.
Cykloheptan: det är en färglös oljig vätska, olöslig och mindre tät än vatten. Inandning av höga koncentrationer kan ha en narkotisk effekt. Används för att tillverka andra kemikalier.
Cyklooktan: är ett polycykliskt kolväte med nio kolatomer. Olöslig i vatten.
Metylcyklohexan: Det är en färglös transparent vätska med en petroleumliknande lukt. I metylcyklohexan är stolkonformationen där den stora metylgruppen är ekvatorial den mest stabila och därför den mest befolkade av alla möjliga konformationer (Carey, 2011).
Isopropylcyklohexan: det är en färglös vätska som finns i frukt. Isopropylcyklohexan finns i Carica papaya (papaya).
metylcyklopentan: det är en färglös olöslig vätska och mindre tät än vatten. Ångor kan vara narkotiska och irriterande. Metylcyklopentan isoleras från Helianthus annuus (solros).
Norborano: det är en bicyklisk alkan även kallad bicyklo [2,2,1] heptan med formeln C7H12.
Referenser
- Alkaner. (2016, 28 november). Återställd från chem.libretexts.org.
- Alkaner. (S.F.). Hämtad från hyperphysics.phy-astr.gsu.edu.
- (2014). Alkaner. Återställd från bbc.co.uk.
- Carey, F. A. (2011, 2 december). Kolväte. Återställd från britannica.
- Encyclopædia Britannica. (2017, 24 mars). Metan. Återställd från britannica.com.
- Khan akademin. (S.F.). Alkaner, cykloalkaner och funktionella grupper. Återställd från khanacademy.org.
- Slår Chloroform dig verkligen ut så snabbt som de visar i filmer? (2016). Återställd från vetenskap.
- Nationellt centrum för bioteknikinformation ... (2017, 06 maj). PubChem Compound Database; CID = 6337. Hämtad från PubChem.
- Nationellt centrum för bioteknikinformation. (2015, 6 maj). PubChem Compound Database; CID = 10041. Hämtad från PubChem.
- Nationellt centrum för bioteknikinformation. (2017, 6 maj). PubChem Compound Database; CID = 10907. Hämtad från PubChem.
- Nationellt centrum för bioteknikinformation. PubChem Compound Database;. (2017, 6 maj). PubChem Compound Database; CID = 6556,. Hämtad från PubChem.
- Propanformel. (S.F.). Återställd från softschools.com.



Ingen har kommenterat den här artikeln än.