
Isopropylalkoholstruktur, egenskaper, syntes och användningar
De isopropylalkohol eller isopropanol är en organisk förening vars kemiska formel är CH3CHOHCH3 eller (CH3)tvåCHOH. Det tillhör en av de viktigaste familjerna inom organisk kemi: alkoholer, som namnet antyder..
Det är en flytande, färglös, starkt luktande, flyktig och brandfarlig kemisk förening. Det är en svag syra och bas samtidigt, liknar vatten, beroende på pH i lösningen och / eller närvaron av en syra eller en bas som är starkare än den. Isopropylalkoholångor orsakar mycket mild irritation i näsan, halsen och ögonen..
Isopropylalkohol används som huvudingrediens i olika produkter inom läkemedels-, kemi-, handels- och hushållsindustrin. På grund av dess antimikrobiella egenskaper används den i stor utsträckning som ett antiseptiskt medel på huden och slemhinnan och som desinfektionsmedel i inerta material..
Det är mycket användbart som lösningsmedel, eftersom det har låg toxicitet och det används också som bensintillsats..
På samma sätt är det råmaterialet för syntes av andra organiska föreningar genom att ersätta den hydroxyl (OH) funktionella gruppen. På detta sätt är denna alkohol mycket användbar och mångsidig för att erhålla andra organiska föreningar; såsom alkoxider, alkylhalogenider, bland andra kemiska föreningar.
Artikelindex
- 1 Struktur av isopropylalkohol eller isopropanol
- 2 Fysikaliska och kemiska egenskaper
- 2.1 Molekylvikt
- 2.2 Fysiskt utseende
- 2.3 Lukt
- 2.4 Smältpunkt
- 2.5 Kokpunkt
- 2.6 Densitet
- 2.7 Löslighet
- 2,8 pKa
- 2.9 Konjugatbas
- 2.10 Absorbans
- 3 Nomenklatur
- 4 Syntes
- 5 användningsområden
- 5.1 Sammanfattningsvis
- 5.2 För rengöring
- 5.3 Antimikrobiell
- 5.4 Medicin
- 5.5 Lösningsmedel
- 6 Referenser
Struktur av isopropylalkohol eller isopropanol
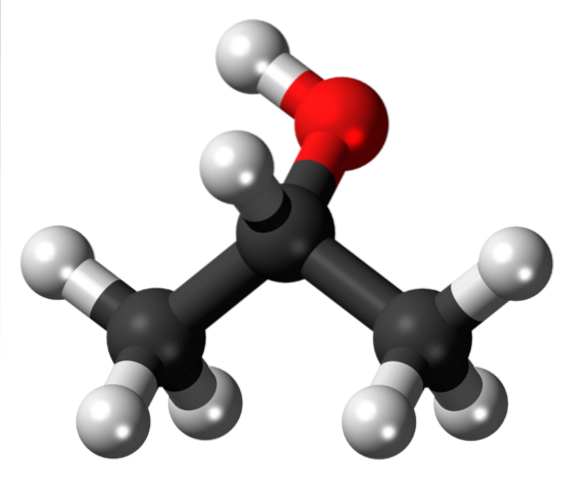
Den övre bilden visar strukturen för isopropylalkohol eller isopropanol med en modell av sfärer och staplar. De tre grå sfärerna representerar kolatomerna, som utgör isopropylgruppen, bundna till en hydroxyl (röda och vita sfärer).
Som alla alkoholer består de strukturellt av en alkan; i detta fall propan. Detta ger alkohol karaktäristiken för lipofil (förmåga att lösa upp fetter med tanke på dess affinitet för dem). Den är bunden till en hydroxylgrupp (-OH), som å andra sidan ger strukturen den hydrofila egenskapen.
Därför kan isopropylalkohol lösa upp fett eller fläckar. Observera att -OH-gruppen är bunden till det mellersta kolet (2: a, dvs fäst vid två andra kolatomer), vilket visar att denna förening är en sekundär alkohol.
Dess kokpunkt är lägre än den för vatten (82,6 ° C), vilket kan förklaras från propanskelettet, som knappast kan interagera med varandra med hjälp av Londons spridningskrafter; lägre än vätebindningar (CH3)tvåCHO-H - H-O-CH (CH3)två.
Fysiska och kemiska egenskaper
Molekylvikt
60,10 g / mol.
Fysiskt utseende
Flytande och färglös och brandfarlig.
Odör
Stark lukt
Smältpunkt
-89 ° C.
Kokpunkt
82,6 ° C.
Densitet
0,786 g / ml vid 20 ° C.
Löslighet
Det är lösligt i vatten och lösligt i organiska föreningar såsom kloroform, bensen, etanol, glycerin, eter och aceton. Det är olösligt i saltlösningar.
pKa
17
Konjugerad bas
(CH3)tvåCHO-
Absorbans
Isopropylalkohol i det synliga ultravioletta spektrumet har en maximal absorbans vid 205 nm.
Nomenklatur
I nomenklaturen för organiska föreningar finns det två system: det för vanliga namn och det internationellt standardiserade IUPAC-systemet..
Isopropylalkohol motsvarar det vanliga namnet, som slutar med suffixet -ico, föregås av ordet alkohol och med namnet på alkylgruppen. Alkylgruppen består av 3 kolatomer, två metyländar och den i mitten fäst till -OH-gruppen; dvs. isopropylgrupp.
Isopropylalkohol eller isopropanol har andra namn såsom 2-propanol, sek-propylalkohol, bland andra; men enligt IUPAC-nomenklaturen kallas det propan-2-ol.
Enligt denna nomenklatur är det först "propan" eftersom kolkedjan innehåller eller består av tre kolatomer.
För det andra indikeras OH-gruppens position i kolkedjan med hjälp av ett tal; i det här fallet är det 2.
Namnet slutar med "ol", karakteristiskt för organiska föreningar av alkoholfamiljen eftersom de innehåller hydroxylgruppen (-OH).
Namnet isopropanol anses vara felaktigt av IUPAC på grund av frånvaron av kolväteisopropan.
Syntes
Den kemiska syntesreaktionen av isopropylalkohol på industriell nivå är i grunden en vattentillsatsreaktion; det vill säga hydrering.
Utgångsprodukten för syntes eller erhållande är propen, till vilken vatten tillsätts. Propen CH3-CH = CHtvå Det är en alken, ett kolväte som härrör från petroleum. Genom hydrering ersätts ett väte (H) med en hydroxylgrupp (OH).
Vatten tillsätts till alkenpropen i närvaro av syror för att producera isopropanolalkohol..
Det finns två sätt att hydrera den: den direkta och den indirekta som utförs under polära förhållanden, vilket genererar isopropanol..
CH3-CH = CHtvå (Propen) => CH3CHOHCH3 (Isopropanol)
Vid direkt hydrering, i gas- eller vätskefasen, hydreras propen genom syrakatalys vid högt tryck.
Vid indirekt hydrering reagerar propen med svavelsyra och bildar sulfatestrar som genom hydrolys producerar isopropylalkohol.
Isopropylalkohol erhålls också genom hydrering av aceton i den flytande fasen. Dessa processer följs av destillation för att separera alkoholen från vattnet, vilket genererar vattenfri isopropylalkohol med ett utbyte av cirka 88%..
Applikationer
Isopropylalkohol har ett brett användningsområde på kemisk nivå. Det är användbart för framställning av andra kemiska föreningar. Den har många applikationer på industriell nivå, för rengöringsutrustning, på medicinsk nivå, för hushållsprodukter och för kosmetisk användning..
Denna alkohol används bland annat i parfymer, hårfärger, lacker, tvålar, som du kommer att se nedan. Dess användning är huvudsakligen och i princip extern, eftersom dess inandning eller intag är mycket giftigt för levande varelser.
Sammanfattningsvis
Från den kan alkylhalogenider erhållas genom att i allmänhet ersätta brom (Br) eller klor (Cl), den funktionella gruppen alkohol (OH).
Genom att genomföra en process för oxidation av isopropylalkohol med kromsyra kan aceton ges upphov. Det kan bilda alkoxider som ett resultat av reaktionen av isopropylalkohol med vissa metaller såsom kalium.
För rengöring
Isopropylalkohol är idealisk för rengöring och underhåll av optiska glasögon som linser och elektronisk utrustning. Denna alkohol avdunstar snabbt, lämnar inga rester eller spår och uppvisar inte toxicitet vid användning eller extern användning.
Antimikrobiell
Isopropanol har antimikrobiella egenskaper, orsakar denaturering av bakterieproteiner, löser upp lipoproteiner i cellmembranet, bland andra effekter.
Som ett antiseptiskt medel appliceras isopropylalkohol på huden och slemhinnorna och avdunstar snabbt och lämnar en svalande effekt. Det används för att utföra mindre operationer, insättning av nålar, katetrar, bland andra invasiva ingrepp. Dessutom används det som desinfektionsmedel för medicinska instrument.
Medicin
Förutom dess användning som ett antimikrobiellt medel krävs det i laboratorier för rengöring, konservering av prover och DNA-extraktion..
Denna alkohol är också mycket användbar vid framställning av farmakologiska produkter. Isopropylalkohol blandas med dofter och eteriska oljor och används i terapeutiska föreningar för att gnugga på kroppen.
Lösningsmedel
Isopropylalkohol har egenskapen att lösa upp vissa oljor, naturliga hartser, tandkött, alkaloider, etylcellulosa, bland andra kemiska föreningar.
Referenser
- Carey, F. A. (2006). Organic Chemistry Sixth Edition. Mc Graw Hill Publishing House
- Morrison, R. och Boyd, R. (1990). Organisk kemi. Femte upplagan. Ledare Addison-Wesley Iberoamericana.
- PubChem. (2019). Isopropylalkohol. Återställd från: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Isopropylalkohol. Återställd från: en.wikipedia.org
- Wade, L. (5 april 2018). Isopropylalkohol. Encyclopaedia Britannica. Återställd från: britannica.com



Ingen har kommenterat den här artikeln än.