
Sulfanilinsyras struktur, egenskaper, syntes, användningsområden

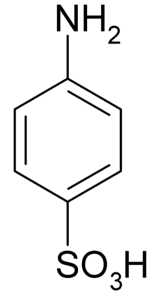
De sulfanilsyra är en kristallin förening vars molekyl bildas av en bensenring till vilken en basisk grupp (-NHtvåoch en syragrupp (-SO3H). Dess kemiska formel är NHtvåC6H4SW3H.
Det är också känt som 4-aminobensensulfonsyra. Den framställs genom sulfonering av anilin i paraposition. Dess kristaller är vita eller gråvita. Dess beteende liknar mer ett salt än en organisk förening med NH-gruppertvå Björn3H. Därför är det olösligt i de flesta organiska lösningsmedel.
En av dess huvudsakliga användningsområden är syntesen av färgämnen, eftersom den lätt bildar en diazo-förening som är en råvara för denna applikation..
Både sulfanilsyra och dess derivat har använts som antibakteriella medel. Det används vid syntes av mukolytiska föreningar, eftersom de har förmågan att minska viskositeten hos slem eller mycket viskösa biologiska vätskor..
Det används också i pappersindustrin och i formler för gravyrer eller litografier. Det är en del av hartserna som används i blandningar av betong eller murbruk för att låta dem behålla sin flytbarhet under lång tid utan att påverka den slutliga härdningstiden.
Det är en främlingsfientlig metabolit, det betyder att den inte produceras naturligt av levande varelser. Det irriterar huden, ögonen och slemhinnorna. Dessutom kan det förorena miljön.
Artikelindex
- 1 Struktur
- 2 Nomenklatur
- 3 fastigheter
- 3.1 Fysiskt tillstånd
- 3.2 Molekylvikt
- 3.3 Smältpunkt
- 3.4 Densitet
- 3.5 Löslighet
- 3.6 Kemiska egenskaper
- 3.7 Övriga egenskaper
- 4 Syntes
- 5 användningsområden
- 5.1 Inom färgämnesindustrin
- 5.2 Inom analytisk kemi
- 5.3 I medicin som ett antibakteriellt medel
- 5.4 I medicin som ett mucolytiskt medel
- 5.5 I bioanalyslaboratorier
- 5.6 I pappersindustrin
- 5.7 I tryck, gravyrer eller litografier
- 5.8 I byggmaterial
- 6 Referenser
Strukturera
Sulfanilsyra har vita kristaller bildade av ortorombiska eller monokliniska ark. Dess monohydrat kristalliserar i vatten i form av ortorombiska ark. Om kristallisationen fortgår mycket långsamt kristalliserar dihydratet. Monohydratet blir vattenfritt när det är nära 100 ºC.
Nomenklatur
- Sulfanilinsyra.
- P-aminobensensulfonsyra.
- 4-aminobensensulfonsyra.
Egenskaper
Fysiskt tillstånd
Vitt eller benvitt kristallint fast ämne.
Molekylvikt
173,19 g / mol.
Smältpunkt
Den sönderdelas vid cirka 288 ° C utan att smälta. Det rapporteras också vid> 320 ºC.
Densitet
1,49 g / cm3
Löslighet
Nästan olöslig i vatten: 10,68 g / L vid 20 ºC.
Olöslig i etanol, bensen och eter. Lätt löslig i het metanol.
Löslig i vattenlösningar av baser. Olöslig i vattenlösningar av mineralsyror. Löslig i koncentrerad saltsyra.
Kemiska egenskaper
Dess egenskaper skiljer sig från andra amino- eller sulfonerade föreningars egenskaper, eftersom de liknar saltens egenskaper. Detta beror på att dess struktur faktiskt innehåller -NH-grupperna3+ Och så3-, vilket ger det zwitterjoniska egenskaper.
Den innehåller en syragrupp och en basisk grupp vid motsatta poler av samma molekyl. Men vätejonen är bunden till kväve istället för syre på grund av -NH-gruppentvå är en starkare bas än -SO-gruppen3-.
Eftersom det är en zwitterion har den en hög smältpunkt och olöslighet i organiska lösningsmedel..
Sulfanilic syra är löslig i alkalisk lösning eftersom hydroxidjonen OH-, eftersom den är starkt basisk startar den en vätejon (H+) av den svaga basgruppen -NHtvå, bildning av p-aminobensensulfonatjonen, som är löslig i vatten.
I syralösning förändras strukturen av sulfanilsyra inte, därför förblir den olöslig.
Andra egenskaper
Vid uppvärmning till nedbrytning avger den giftiga ångor av kväveoxider och svavel.
Exponering för sulfanilsyra kan leda till symtom som irritation i hud, ögon och slemhinnor. Det är en frätande förening.
Syntes
Den framställs genom att reagera anilin med svavelsyra (HtvåSW4) vid höga temperaturer. Ursprungligen bildas syraaniliniumsulfatsaltet, som vid uppvärmning till 180-200 ° C omorganiseras för att bilda den substituerade ringen i paraposition, eftersom den är den mest stabila produkten.
För att förbereda den med en hög grad av renhet, sulfoneringen av en blandning av anilin och sulfolan med HtvåSW4 vid 180-190 ºC.
Applikationer
I färgämnesindustrin
Sulfanilinsyra används vid syntes eller beredning av olika färgämnen, såsom metylorange och tartrazin. För detta är det diazotiserad och genererar diazotiserad sulfanilsyra..
Det är viktigt att notera att tartrazin har använts som färgämne i maten. Men när det har intagits genererar det vissa metaboliter i människokroppen, inklusive sulfanilsyra, som möjligen är ansvariga för bildandet av reaktiva syrearter. Dessa kan påverka njure (njurar) eller lever (lever) vävnader..

Inom analytisk kemi
Det används som ett reagens vid bestämning av olika kemiska föreningar, inklusive nitriter..
I medicin som ett antibakteriellt medel
Sulfanilamid, härledd från sulfanilsyra, har tillämpning inom läkemedelsindustrin eftersom den har antibakteriell aktivitet.
I människokroppen förväxlar bakterier det med p-aminobensoesyra, som är en viktig metabolit. Denna ersättning innebär att bakterierna inte reproducerar och dör.
Ett annat derivat av sulfanilsyra, erhållet genom kondensation med andra föreningar, har också antibakteriella egenskaper, vilka är baserade på dess förmåga att förskjuta folsyra (en del av vitamin B-komplexet)..
Denna förening kan tas oralt, injiceras intravenöst eller appliceras externt i en salva..
I medicin som ett mucolytiskt medel
Ett derivat av sulfanilsyra som har mukolytisk aktivitet har använts. Detta är att det uppvisar flytande aktivitet av slem, för att lösa upp slem själv eller mycket viskösa biologiska vätskor.
Föreningen kan användas för att producera flytande av slem som produceras av en vävnad på grund av patologiska tillstånd. Till exempel trängsel i andningsorganen eller bland annat från vaginalvägarna.
När det gäller flytning av slem i luftvägarna administreras produkten genom inandning, droppar i näsan, dimma, aerosoler eller nebulisatorer. Det är en behandling som är tillämplig på människor eller däggdjur. Det är en mer kraftfull förening än de baserade på cystein.

Det används också i laboratoriet när det är önskvärt att minska viskositeten hos biologiska vätskor för att underlätta analytiska bestämningar..
I bioanalyslaboratorier
Diazotiserad sulfanilsyra (ett derivat framställt genom att reagera sulfanilsyra med natriumnitrit) används vid bestämning av bilirubin.
Bilirubin är ett gult pigment som finns i galla. Överskott av bilirubin i blodet är en konsekvens av leversjukdomar, hematologiska (eller blod) störningar eller störningar i gallvägarna.
För att mäta mängden bilirubin i blodet reageras den diazo som härrör från sulfanilsyra med bilirubin för att bilda azobilirubinkomplexet, vars intensitet mäts med en kolorimeter eller spektrofotometer. På detta sätt bestäms bilirubinhalten i blodserum..
I pappersindustrin
Sulfanilsyra gör det möjligt att syntetisera en papperspolering, det vill säga en förening som ger den en optisk glans eller ett vitt utseende, eftersom den neutraliserar den gula färgen på naturligt eller obehandlat papper..

Den har fördelen jämfört med andra föreningar genom att den kan användas i relativt höga koncentrationer för att behandla pappersmassa under lågt pH-förhållande, utan att öka pappersgulheten..
Resultatet är uppenbart när papperet observeras med UV (ultraviolett) ljus, under vilket det fluorescerar mycket mer än när andra föreningar används, och med synligt ljus observeras att graden av gulhet är mycket låg.
Det är mycket lösligt i vatten, vilket gör att det kan användas i mer koncentrerade lösningar. Kan användas på alla typer av papper, inklusive papper som framställts av slipad vedmassa, sulfitmassa eller någon annan process.
I tryck, gravyrer eller litografier
Sulfanilic syra fungerar som en surgörare i koncentrerade lösningar för litografi, utan att presentera problemen med andra syror såsom fosforsyra, är mindre giftig och mindre förorenande än den senare..
I byggmaterial
Sulfanilsyramodifierade vattenhaltiga melamin-formaldehydhartslösningar har testats i betong (betong), murbruk eller cementpasta. Syftet har varit att minska vatteninnehållet och förhindra en minskning av blandningens flytbarhet över tiden utan att minska inställningstiden..
Betong eller murbruk framställd med dessa lösningar är mycket effektiv på sommaren, då minskningen av fluiditet över tid är ett problem..
Med dessa lösningar kan cementkompositionen lätt hällas i formar eller liknande, eftersom murbruk eller betong framställs och av vilken anledning som helst måste lämnas vilande, eftersom den inte har tappat flytbarhet över tiden..

Referenser
- Windholz, M. et al. (redaktörer) (1983). Merck Index. En encyklopedi av kemikalier, läkemedel och biologiska ämnen. Tionde upplagan. Merck & CO., Inc..
- Kirk-Othmer (1994). Encyclopedia of Chemical Technology. Volym 2. Fjärde upplagan. John Wiley & Sons.
- National Library of Medicine. (2019). Sulfanilic syra. Återställd från: pubchem.ncbi.nlm.nih.gov
- Urist, H. och Martin, G.J. (1950). Sulfanil-syraderivat. US patent nr 2 504 471. Tilldelare till National Drug Company. 18 april 1950.
- Villaume, Frederick G. (1964). Ljusmedelkomposition för papper härrörande från metanil- och sulfanilsyra. US patent nr 3 132 106. 5 maj 1964.
- Martin, Tellis A. och Comer, William T. (1979). Bensoesyraderivat och bensensulfonsyra mukolytisk process. US patent nr 4,132,802. 2 januari 1979.
- Druker, L.J. och Kincaid, R.B. (1979). Litografisk fontänkoncentrat. US patent nr 4 150 996. 24 april 1979.
- Shull, Bruce C. (1983). Bilirubin-analys. US patent nr 4,404,286. 13 september 1983.
- Uchida, J. et al. (2001). Förfarande för framställning av en vattenlösning av sulfanilsyramodifierat melamin-formaldehydharts och en cementkomposition. US patent nr 6,214,965 B1. 10 april 2001.
- Corradini, M.G. (2019). Volym 1. I Encyclopedia of Food Chemistry. Återställd från sciencedirect.com.



Ingen har kommenterat den här artikeln än.