
Kalciumfluorid (CaF2) struktur, egenskaper, användningsområden
De kalciumfluorid Det är ett oorganiskt fast ämne bildat av en kalciumatom (Ca) och två fluoratomer (F). Dess kemiska formel är CaFtvå och det är ett kristallint gråvitt fast ämne.
I naturen finns den i mineralet fluorit eller fluorspar. Det finns naturligt i ben och tänder. Mineralet fluorit är den viktigaste källan som används för att erhålla andra fluorföreningar.

Dessutom har CaFtvå Det används för att förhindra håligheter i tänderna, så det läggs till material som används av tandläkare för att bota dem. I själva verket tillsätts kalciumfluorid också till dricksvatten (vatten som kan drickas) så att befolkningen drar nytta av att inta det och borsta tänderna..
CaFtvå Den används i form av stora kristaller i optisk utrustning och kameror. Det används också i små enheter som används för att upptäcka hur mycket en person har utsatts för radioaktivitet.
Artikelindex
- 1 Struktur
- 2 Nomenklatur
- 3 fastigheter
- 3.1 Fysiskt tillstånd
- 3.2 Molekylvikt
- 3.3 Smältpunkt
- 3.4 Kokpunkt
- 3.5 Densitet
- 3.6 Brytningsindex
- 3.7 Löslighet
- 3.8 Kemiska egenskaper
- 4 Närvaro i naturen
- 5 användningsområden
- 5.1 - Vid erhållande av fluorföreningar
- 5.2 - Under vård av tänder
- 5.3 - I linser för optisk utrustning
- 5.4 - Inom metallindustrin
- 5.5 - I detektorer av radioaktivitet eller farlig strålning
- 5.6 - Andra användningsområden
- 6 Referenser
Strukturera
CaF kalciumfluoridtvå är en jonförening bildad av en kalciumkatjon Catvå+ och två fluoranjoner F-. Vissa informationskällor indikerar dock att deras länkar har en viss kovalent karaktär.
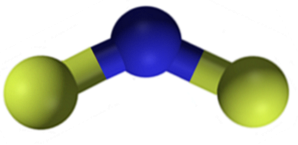
Nomenklatur
Kalciumfluorid
Egenskaper
Fysiskt tillstånd
Färglös till gråvit fast substans med kubisk kristallstruktur.
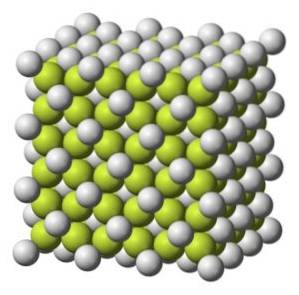
Molekylvikt
78,07 g / mol
Smältpunkt
1418 ºC
Kokpunkt
2533 ºC
Densitet
3,18 g / cm3 vid 20 ° C.
Brytningsindex
1.4328
Löslighet
Det är olösligt i vatten vid 20 ° C. Nästan olöslig vid 25 ° C: 0,002 g / 100 ml vatten. Lätt löslig i syror.
Kemiska egenskaper
Dess oxiderande eller reducerande egenskaper är mycket svaga, men dessa reaktioner kan uppstå. Även i allmänhet i mycket få fall.
Det är inert mot organiska kemikalier och många syror, inklusive fluorvätesyra. Lösas långsamt i salpetersyra HNO3.
Det är inte brandfarligt. Reagerar inte snabbt med luft eller vatten.
På grund av dess låga affinitet för vatten påverkar den inte ens i upp till en månad vid normal rumstemperatur, även om den utsätts för en hög andel fuktighet..
I närvaro av fuktighet löses kristallväggarna långsamt upp vid temperaturer över 600 ° C. I torra miljöer kan den användas upp till cirka 1000 ° C utan att påverkas märkbart.
Närvaro i naturen
CaF kalciumfluoridtvå finns naturligt i mineralet fluorit eller fluorspar.
Även om CaFtvå rent är färglöst mineral fluorit, det färgas ofta av närvaron av elektroner som fångats i "hålen" i den kristallina strukturen.
Detta mineral är högt uppskattat för sin glasiga glans och olika färger (lila, blå, grön, gul, färglös, brun, rosa, svart och rödorange). Det sägs vara "världens mest färgade mineral".





Kalciumfluorid finns också i benen i mängder mellan 0,2 och 0,65%, och även i emalj av tänderna i 0,33-0,59%.
Applikationer
- Vid erhållande av fluorföreningar
Mineralet fluorit CaFtvå Det är den grundläggande eller majoritetskällan för fluor över hela världen. Det är råmaterialet att framställa nästan alla fluorföreningar.
Den viktigaste av dessa är fluorvätesyra HF, från vilken de andra fluorerade föreningarna framställs. Fluoridjonen F- frigörs från mineralet genom att reagera det med koncentrerad svavelsyra HtvåSW4:
CaFtvå (fast) + HtvåSW4 (flytande) → CaSO4 (fast) + 2 HF (gas)
- Under vård av tänder
CaF kalciumfluoridtvå det är ett medel för att förhindra håligheter. Det används för att fluoridera dricksvatten (vatten som kan drickas) för detta ändamål.
Vidare är de låga koncentrationerna av fluor F- (i storleksordningen 0,1 delar per miljon) som används i tandkrämer och munvatten har visat sig ha en mycket positiv effekt på hålrums förebyggande tandvård.

CaF nanopartiklartvå mer effektivt
Även om fluorider används i tandkrämer och sköljningar, innebär den låga koncentrationen av kalcium (Ca) i saliv att CaF-avlagringar inte bildas.två på tänderna så effektivt som möjligt.
Det är därför som ett sätt att erhålla CaF-pulver har utformats.två som nanopartiklar.
För detta används en spraytork (från engelska spraytork) där två lösningar (en av kalciumhydroxid Ca (OH)två och en av ammoniumfluorid NH4F) blandas medan de sprutas i en kammare med varmluftflöde.
Därefter inträffar följande reaktion:
Ca (OH)två + NH4F → CaFtvå (fast) + NH4Åh
NH4OH förångas som NH3 och HtvåEller och CaF-nanopartiklarna finns kvartvå.
Dessa har hög reaktivitet och större löslighet, vilket gör dem mer effektiva för remineralisering av tänder och som antikroppar.
- I linser för optisk utrustning
Kalciumfluorid används för att bygga optiska element såsom prismor och fönster i infraröda och ultravioletta (UV) ljusspektrofotometrar..
Dessa enheter gör att vi kan mäta mängden ljus som absorberas av ett material när det passerar genom det.
CaFtvå den är transparent i dessa delar av ljusspektret, har ett extremt lågt brytningsindex och möjliggör en mer effektiv upplösning än NaCl i intervallet 1500-4000 cm.-1.
Tack vare sin kemiska stabilitet tål den ogynnsamma förhållanden, varför CaF optiska elementtvå de attackeras inte. Det har också en hög hårdhet.
I kameror
Vissa kameratillverkare använder CaF-objektivtvå artificiellt kristalliserad för att reducera ljusspridning och uppnå utmärkt färgförvrängningskorrigering.

- Inom metallindustrin
CaFtvå Det används som ett flussmedel i metallindustrin, eftersom det är en källa till kalcium som är olöslig i vatten och därför effektiv i applikationer som är känsliga för syre..
Det används för att smälta och bearbeta järn och stål i flytande form. Detta baseras på det faktum att det har en smältpunkt som liknar järnens och att den kan lösa upp oxider och metaller..
- I detektorer av radioaktivitet eller farlig strålning
CaFtvå det är ett termoluminescerande material. Detta innebär att den kan absorbera strålning i elektronerna i dess kristallstruktur och senare, när den värms upp, släppa den i form av ljus..
Detta utsända ljus kan mätas med en elektrisk signal. Denna signal är proportionell mot mängden strålning materialet mottaget. Det betyder att ju större mängd mottagen strålning, desto större mängd ljus som den kommer att avge efter uppvärmning..
Av denna anledning CaFtvå Den används i så kallade personliga dosimetrar, som används av människor som utsätts för farlig strålning och vill veta hur mycket strålning de har fått under en tidsperiod.
- Andra användningsområden
- Det används som en katalysator vid dehydrering och dehydrogenering kemiska reaktioner för syntes av organiska föreningar.
- Den används i alkaliska svetselektroder. En starkare svets erhålls än med syraelektroder. Dessa elektroder är användbara vid tillverkning av fartyg och högtrycksstålkärl..
- Som kosttillskott i extremt låga mängder (ppm eller delar per miljon).

Referenser
- Pirmoradian, M. och Hooshmand, T. (2019). Remineralisering och antibakteriella förmåga hos hartsbaserade dental nanokompositer. Syntes och karakterisering av kalciumfluorid (CaFtvå). In Applications of Nanocomposite Materials in Dentistry. Återställd från sciencedirect.com.
- USA National Library of Medicine. (2019). Kalciumfluorid. Återställd från pubchem.ncbi.nlm.nih.gov.
- Weman, K. (2012). Manuell metallbågsvetsning (MMA) med belagda elektroder. I Welding Processes Handbook (andra upplagan). Återställd från sciencedirect.com.
- Hanning, M. och Hanning, C. (2013). Nanobiomaterial i förebyggande tandvård. Nanoserat kalciumfluorid. I nanobiomaterial i klinisk tandvård. Återställd från sciencedirect.com.
- Ropp, R.C. (2013). Grupp 17 (H, F, Cl, Br, I) Alkaliska jordföreningar. Kalciumfluorid. I Encyclopedia of the Alkaline Earth Compounds. Återställd från sciencedirect.com.
- Cotton, F. Albert och Wilkinson, Geoffrey. (1980). Avancerad oorganisk kemi. Fjärde upplagan. John Wiley & Sons.
- Valkovic, V. (2000). Mätningar av radioaktivitet. I radioaktivitet i miljön. Termoluminescerande detektorer (TLD). Återställd från sciencedirect.com.


Ingen har kommenterat den här artikeln än.