
Metalloids egenskaper, egenskaper och användningsområden
De metalloider eller halvmetaller är en grupp kemiska element med mellanliggande fysiska och kemiska egenskaper mellan metaller och icke-metaller. De flesta kemiska forskare accepterar följande kemiska element som metalloider: bor, kisel, arsenik, germanium, antimon och tellur (grön i bilden nedan).
En mindre grupp forskare lägger dock till polonium, astat (blå färg) och selen (rosa färg) till metalloider..
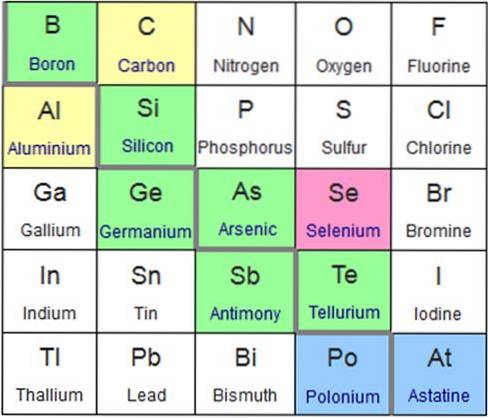
Även baserat på vissa egenskaper föreslår de att de kemiska grundämnena kol och aluminium (gul i färg) också bör betraktas som metalloider..
Artikelindex
- 1 Huvudegenskaper hos metalloider
- 1.1 Situationen i det periodiska systemet
- 1.2 De bildar legeringar med metaller
- 1.3 Elektriska halvledare
- 1.4 Grunden för elektronikindustrin
- 1.5 Allotropiska tillstånd
- 2 Fysikaliska och kemiska egenskaper
- 2.1 Fysiska egenskaper
- 2.2 Kemiska egenskaper
- 3 användningsområden
- 3.1 Om levande varelser
- 3.2 I glas och emalj
- 3.3 Vid tillverkning av material av högre kvalitet
- 3.4 Inom elektronik och dator
- 3.5 Skyddande åtgärder av metalloider
- 3.6 Andra
- 4 De 8 metalloidelementen
- 5 Referenser
Huvudegenskaper hos metalloider
Situationen på det periodiska systemet
Metalloider är placerade på det periodiska systemet på en nedåtgående diagonal mellan kolumnerna 13, 14, 15, 16 och 17, som börjar med bor uppe till vänster och slutar med astatin längst ner till höger..
Metaller är till vänster om metalloider och icke-metaller till höger; därför representerar de gränsen mellan båda typerna av materia.
De bildar legeringar med metaller
Metalloider bildar legeringar med metaller och reagerar med icke-metaller, till exempel med syre, svavel och halogener..
Elektriska halvledare
För det mesta betraktas de som elektriska halvledare, deras konduktans är temperaturberoende. Vid låga temperaturer är den elektriska konduktansen låg, så de fungerar som elektriska isolatorer, men när de värms upp ökar deras förmåga att leda elektricitet..
Elektronikindustrins bas
Halvledare är grunden för utvecklingen av elektronikindustrin, såväl som databehandling och informatik. På samma sätt har applikationen som har gjorts av kisel varit mycket användbar inom detta område.
Allotropiska tillstånd
Metalloider har olika allotropa tillstånd (olika kristallina former); sålunda har till exempel arsenik svarta, gula eller gråa kristaller.
I naturen finns de vanligtvis inte som rena kemiska element utan snarare associerade eller bildande aggregat i mineraler tillsammans med bly, svavel, järn etc..
Fysiska och kemiska egenskaper

Fysikaliska egenskaper
De verkar som glänsande fasta ämnen. I detta avseende liknar de metaller. De är spröda och inte särskilt elastiska, så de kan inte sträckas i form av en tråd, det vill säga de är inte särskilt duktila. Dessutom är dess omvandling till ark svår, så metalloiderna är inte särskilt smidiga..
De kan leda elektricitet och temperatur, men i mindre grad än metaller. Inom metalloiderna finns kemiska element som, baserat på deras bandstrukturer, klassificeras som halvledare.
Denna grupp består av bor, kisel, germanium och antimon. Arsenik och tellur klassificeras som halvmetaller.
Fusionspunkter
Bor 2076 ° C; Kisel 1 414 ° C; Germanium 938,25 ° C; Arsenik 817 ° C; Antimon 630,13 ° C; Tellurium 449,51 ° C och Polonium 254 ° C.
Kokpunkter
Bor 3 927 ° C; Kisel 3 265 ° C; Germanium 2,833 ° C; Arsenik 614 ° C; Antimon 1587 ° C; Tellurium 988 ° C och Polonium 962 ° C.
Densiteter
Bor 2,34 g / cm3: Kisel 2,33 g / cm3; Germanium 5,323 g / cm3; Arsenik 5,727; Antimon 6 677 g / cm3; Tellurium 6,24 g / cm3 och Polonium 9,32 g / cm3.
Kemiska egenskaper
De beter sig på liknande sätt som icke-metaller, de bildar oxacider som SiOtvå och de har ett amfotiskt beteende. Metalloider kan bete sig som en syra eller en bas beroende på mediumets pH..
Applikationer
Om levande varelser
-Arsen används i jordbruket som insektsmedel och herbicid. Dessutom används det för att placera det som ett pulver eller i flytande lösning på boskap för att eliminera insekter och parasiter från djuret. Kalciumarsenat används för att döda bomullsbiffen.
-Arsenik används som ett träskyddsmedel på grund av dess toxicitet för insekter och svampar.
-Arsenik används för att behandla akut promyelocytisk leukemi, en typ av blodcancer. Det används vid beredning av Fowlers lösning för användning vid behandling av psoriasis. En radioaktiv isotop av arsenik (74As) används vid lokalisering av cancertumörer som finns i människokroppen.
-Arsenik är en del av Melarsoprol, ett läkemedel som används vid behandling av human afrikansk trypanosomiasis. Parasitisk sjukdom överförd av tsetseflugan.
-Telluriumoxid har använts vid behandling av seborrheisk dermatit. Likaså används andra tellurföreningar som antimikrobiella medel..
-Bor, i form av borsyra, används som ett milt antiseptiskt medel i ögon, näsa och hals.
I glas och emalj
-Tellurium används vid tillverkning av blå, bruna och röda glasögon. Metalloid kan elektrolytiskt deponeras på silver och ger en svartaktig yta.
-Antimon används för att ge glasögon och emaljer en gul nyans. Bor används vid tillverkning av glas och keramik. I synnerhet är borosilikatglas resistent mot temperaturförändringar, varför det används i laboratorier vid kemiska reaktioner och destillationer..
-Hemma kan maten bakas med borosilikatglas utan att bryta redskapen som används..
-Kisel är den viktigaste basen för glasindustrin, involverad i tillverkningen av nästan alla glasföremål.
-Germaniumoxid används vid tillverkning av kameralinser och mikroskoplinser. Dessutom används den vid tillverkning av kärnan av optiska fibrer för många applikationer..
Vid produktion av material av högre kvalitet
-Arsenik bildar legeringar med bly och orsakar en minskning av smältpunkten. Detta orsakar en högre hårdhet i legeringen som används vid produktion av skott.
-Tillsättningen av en mängd tellur mellan 0,1% och 0,6% av en blyad legering ökar dess motståndskraft mot korrosion och mot dragkraft med ökad flexibilitet. Tellurium tillsätts ofta i gjutjärn för att härda ytskiktet på härdade delar..
-Antimon används i legeringar för att producera lager, ackumulatorplattor och tryckmaterial.
-Kisel används vid tillverkning av legeringar med högre motståndskraft mot syror. Så är fallet med Duriron, som innehåller 14% kisel.
Legeringen av kisel, järn och aluminium används för att utarbeta bitar med stor hårdhet, som används i fordonsindustrin.
-Arsenik bildar legeringar med platina och koppar för att öka korrosionsbeständigheten. Dessutom tillsätts arsenik till alfamässing för att öka zinkens styrka. Denna typ av mässing används vid tillverkning av tillbehörsmaterial för VVS.
Inom elektronik och dator
-Metalloider används som halvledare inom elektronik- och datorindustrin. I denna mening är kisel ledande inom handeln med halvledare som utgör grunden för modern elektronik och dator. Kisel och dess derivat används i datorer, transitorer, solceller och LCD-skärmar..
-Tellurium är en halvledare som har applikationer inom elektroptik och elektronik.
-Germanium är en halvledarmetalloid som används tillsammans med kisel i höghastighetsintegrerade kretsar för att förbättra deras prestanda. Även om germanium har något förskjutet kisel i sin halvledarfunktion har dess användning vid tillverkning av miniatyriserade marker förbättrats.
-Germanium används vid tillverkning av solpaneler. Även utforska robotar på planeten Mars innehåller germanium i sina solceller. Dessutom används germanium vid tillverkning av radar.
Skyddande åtgärder av metalloider
Bor och dess besläktade föreningar ger stor beständighet mot de material som den ingår i. Detta möjliggör dess användning i skapandet av rumsliga strukturer. Dessutom används de vid tillverkning av golfklubbor och fiskespön..
Borskarbids skyddande verkan används som kontrollbarriärer i kärnreaktorer, vilket begränsar läckaget av radioaktivt material. Dessutom används borcarbid i skottsäkra västar och i krigstankarnas rustning..
Kiseldioxid och kiseldioxid, i form av lera eller sand, är viktiga komponenter i tegel, betong och cement, som används i olika former av konstruktion.
Andra
-Antimensulfid används i fyrverkerier och blixtlampor.
-Bor är en del av neodymidiummagneter.
-Silikon, en polymer härrörande från kisel, används vid tillverkning av oljor och vaxer, bröstimplantat, kontaktlinser, sprängämnen och inom pyroteknik.
-Germanium används vid tillverkning av lysrör och vissa lysdioder. Dessutom används germanium i elgitarrer för att producera en karakteristisk distorsionston..
-Germanium används i termisk bildapplikation för militär användning och brandbekämpning.
-Antimon används vid tillverkning av tändstickor och spår- och lokaliseringsgranater samt i grundfärger för patroner.
-Natriumborat används som brandskyddsmedel i plast och gummi.
De 8 metalloidelementen
Denna grupp av kemiska element består av bor, kisel, antimon, tellur, germanium, arsenik, polonium och astat. Men det största antalet forskare inom kemi utesluter polonium och astat som metalloider..
Därför skulle den mest allmänt accepterade gruppen metalloider bestå av bor, kisel, antimon, tellur, germanium och arsenik..
Polonium har noterats vara distinkt metalliskt, eftersom dess två allotropa former är metalliska ledare. Å andra sidan klassificerades astatin 2013 som en metall, även om den tidigare 1950 betecknades som en halogen, en reaktiv icke-metallisk.
Gränsen mellan grupperna av element som betraktas som metaller, metalloider eller icke-metaller är oklar. Av denna anledning föreslår vissa forskare, baserade på någon egenskap, att detta eller det här elementet bör betraktas som metalloid. Det har till exempel påpekats att kol, aluminium eller selen bör klassificeras som metalloider.
Ett försök har gjorts att fastställa urvalskriterier som gör det möjligt att klassificera ett kemiskt element som metall, metalloider eller icke-metalliska. Andra urvalskriterier inkluderar joniseringsenergi, elektronegativitet och packningseffektivitet hos de olika kemiska elementen..
Referenser
- Eden Francis. (2002). Elementens klassificering. Hämtad från: dl.clackamas.edu
- Metaller, metalloider och icke-metaller. Hämtad från: angelo.edu
- Element. Metalloider. Hämtad från: elements.org.es
- Exempel av. (2013). Metalloider. Hämtad från: examplede.com
- Wikipedia. (2018). Metalloid. Hämtad från: en.wikipedia.org
- Kemi snabbt. (2011). Metalloider (halvmetaller). Hämtad från: chemistry.patent-invent.com
- Redaktörerna för Encyclopaedia Britannica. (2016, 18 oktober). Metalloid. Hämtad från: britannica.com



Ingen har kommenterat den här artikeln än.