
Rasemisk blandning av kiralitet, exempel

A racemisk blandning eller racemat är en sammansatt av två enantiomerer i lika delar och som därför är optiskt inaktiv. Denna optiska aktivitet avser förmågan hos dess lösningar att rotera, medurs eller moturs, en stråle av polariserat ljus som färdas genom dem i en riktning..
En enantiomer har förmågan att rotera polariserat ljus, till exempel till vänster (vänsterhänt), så dess rena lösning kommer att vara optiskt aktiv. Men om enantiomeren som roterar ljuset åt höger (dextrorotatory) börjar läggas till den kommer dess optiska aktivitet att minska tills den inaktiveras..

När detta händer sägs att det finns lika stora mängder av vänster och höger enantiomer; Om en molekyl roterar det polariserade ljuset åt vänster kommer dess effekt att omedelbart avbrytas när den "snubblar" med en annan molekyl som roterar den till höger. Och så vidare. Därför kommer vi att ha en racemisk blandning.
Den första synen av enantiomerism gjordes av den franska kemisten Louis Pasteur 1848, som studerade en blandning av enantiomera kristaller av vinsyra (vid den tiden kallad raceminsyra). Eftersom denna syra kom från druvorna som användes för att tillverka vin, applicerades denna blandning på ett allmänt sätt för alla molekyler.
Artikelindex
- 1 Skor och chiralitet
- 2 Exempel
- 2.1 Vinsyra
- 2.2 Kinin
- 2.3 Talidomid
- 2,4 1,2-epoxipropan
- 2,5 1-fenyletylamin
- 2.6 Slutlig kommentar
- 3 Referenser
Skor och chiralitet
Först och främst måste det finnas två enantiomerer (vanligtvis) för att det ska finnas en racemisk blandning, vilket innebär att båda molekylerna är kirala och att deras spegelbilder inte är överlagbara. Ett par skor illustrerar detta perfekt: oavsett hur hårt du försöker lägga den vänstra skon till höger kommer de aldrig att kunna passa..
Den högra skon, för att säga, avböjer det polariserade ljuset till vänster; medan den vänstra skon gör det till höger. I en hypotetisk lösning där skorna är molekylerna, om det bara finns raka, kirala skor, kommer detta att vara optiskt aktivt. Detsamma kommer att hända om det bara finns kvar skor i lösning.
Men om det finns tusen vänsterskor blandat med tusen högerskor, har vi en racemisk blandning, som också är optiskt inaktiv, eftersom avvikelserna från ljuset inuti tar bort varandra..
Om det istället för skor var kulor, föremål som är achirala, skulle det vara omöjligt för racemiska blandningar av dessa att existera, eftersom de inte ens skulle kunna existera som par av enantiomerer.
Exempel
Vinsyra
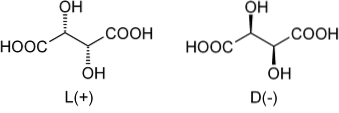
Återvänder till vinsyra var dess racemiska blandning den första som var känd. I den övre bilden visas dess två enantiomerer, var och en som kan bilda kristaller med morfologiska "vänster" eller "höger" ansikten. Pasteur lyckades med hjälp av ett mikroskop och en sträng ansträngning att separera dessa enantiomera kristaller från varandra..
Kristallerna av L (+) - och D (-) - enantiomererna visar separat optisk aktivitet genom att avböja polariserat ljus åt höger respektive vänster. Om båda kristallerna i lika molära proportioner löser sig i vatten kommer en optiskt inaktiv racemisk blandning att erhållas..
Observera att båda enantiomererna har två kirala kol (med fyra olika substituenter). I L (+) ligger OH: erna bakom planet bildat av kolskelettet och COOH-grupperna; medan i D (-) ligger dessa OH över nämnda plan.
De som syntetiserar vinsyra kommer att få en racemisk blandning. För att separera L (+) enantiomeren från D (-) är en kiral upplösning nödvändig, i vilken denna blandning reageras med en kiral bas för att producera diastereoisomera salter, som kan separeras senare genom fraktionerad kristallisation..
Kinin

I exemplet ovan, för att hänvisa till en racemisk blandning av vinsyra, är det vanligtvis skrivet som (±) -vinsyra. Således, när det gäller kinin (övre bild) kommer det att vara (±) -kinin.
Kinomerns isomerism är komplex: den har fyra kirala kol, vilket ger upphov till sexton diastereoisomerer. Intressant är att två av dess enantiomerer (en med OH ovanför planet och den andra under den), faktiskt är diastereoisomerer, eftersom de skiljer sig åt i konfigurationerna för sina andra kirala kolatomer (de av bicyclo med N-atomen).
Det är dock svårt att avgöra vilken av stereoisomererna av kinin som kommer att avböja polariserat ljus åt höger eller vänster..
Talidomid
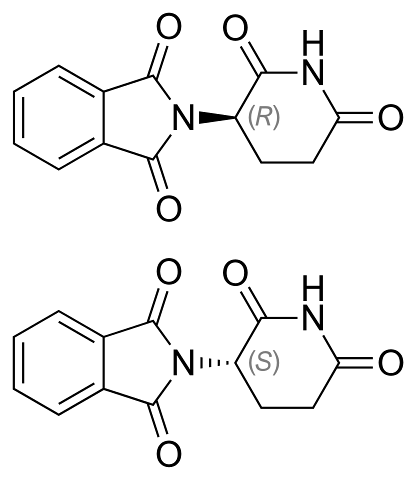
Talidomidens enantiomerer visas ovan. Det har bara ett kiralt kol: det som är kopplat till kvävet som förenar båda ringarna (en av ftalimid och den andra av gluteramid).
I R-enantiomeren (med lugnande egenskaper) är ftalimidringen (den till vänster) orienterad ovanför planet; medan i S enantiomeren (med mutagena egenskaper), nedan.
Det är inte känt för ögat procent vilken av de två som avböjer ljuset till vänster eller höger. Vad som är känt är att en 1: 1 eller 50% blandning av båda enantiomererna bildar den racemiska blandningen (±) -talidomid.
Om du bara vill marknadsföra talidomid som ett hypnotiskt lugnande medel, är det obligatoriskt att utsätta dess racemiska blandning för den redan nämnda kirala upplösningen, på ett sådant sätt att den rena R-enantiomeren erhålls..
1,2-epoxipropan
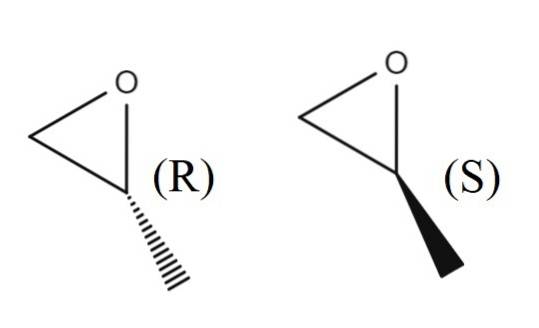
I den övre bilden har du enantiomerparet 1,2-epoxipropan. R-enantiomeren avböjer polariserat ljus till höger, medan S-enantiomeren avböjer det till vänster; den första är (R) - (+) - 1,2-epoxipropan, och den andra är (S) - (-) - 1,2-epoxipropan.
Den racemiska blandningen av de två blir återigen i förhållandet 1: 1 eller 50% (±) -1,2-epoxipropan.
1-fenyletylamin
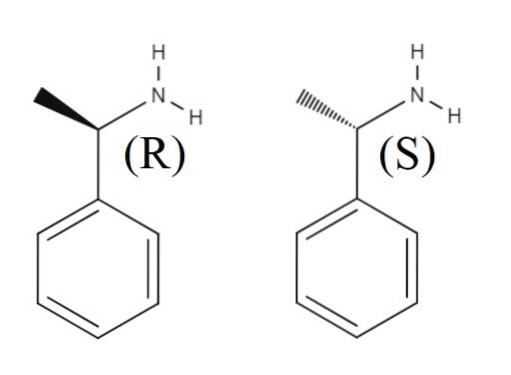
Ovan är en annan racemisk blandning bildad av de två enantiomererna av 1-fenyletylamin. R-enantiomeren är (R) - (+) - 1-fenyletylamin och S-enantiomeren är (S) - (-) - 1-fenyletylamin; en har metylgruppen, CH3, pekar ut ur den aromatiska ringens plan och den andra pekar under den.
Observera att när konfigurationen är R, sammanfaller den ibland med det faktum att enantiomeren roterar det polariserade ljuset åt höger; det gäller dock inte alltid och kan inte tas som en allmän regel.
Slutlig kommentar
Viktigare än förekomsten eller inte av racemiska blandningar är deras kirala upplösning. Detta gäller särskilt föreningar med farmakologiska effekter som är beroende av nämnda stereoisomerism; det vill säga en enantiomer kan vara till nytta för patienten, medan den andra kan påverka den.
Det är därför dessa kirala upplösningar används för att separera de racemiska blandningarna i deras komponenter och därmed kunna marknadsföra dem som rena läkemedel utan skadliga föroreningar..
Referenser
- Morrison, R. T. och Boyd, R, N. (1987). Organisk kemi. 5: e upplagan. Ledare Addison-Wesley Interamericana.
- Carey F. (2008). Organisk kemi. (Sjätte upplagan). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kemi. Aminer. (10: e upplagan.). Wiley plus.
- Steven A. Hardinger. (2017). Illustrerad ordlista för organisk kemi: rasemisk blandning. Institutionen för kemi och biokemi, UCLA. Återställd från: chem.ucla.edu
- Nancy Devino. (2019). Racemic Mixture: Definition & Exempel. Studie. Återställd från: study.com
- James Ashenhurst. (2019). Stereokemi och kiralitet: Vad är en racemisk blandning? Återställd från: masterorganicchemistry.com
- John C. Leffingwell. (2003). Kiralitet och bioaktivitet I.: Farmakologi. [PDF]. Återställd från: leffingwell.com



Ingen har kommenterat den här artikeln än.