
Syncytiotrofoblastegenskaper, funktion, placentapoptos
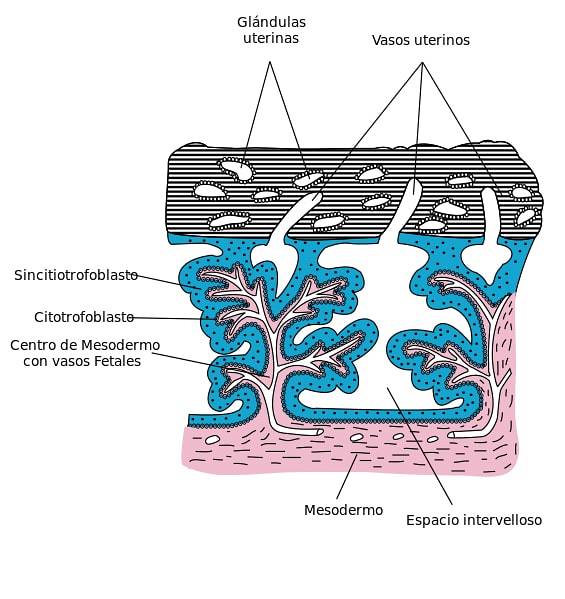
De syncytiotrofoblast Det är en flerkärnig cytoplasmisk massa som bildar det yttre skiktet av trofoblasten och kommer i kontakt med moderns vävnad. Detta cellskikt hittas invaderar epiteliet och stroma i endometrium under embryonal utveckling av däggdjur. Cellerna som utgör syncytiotrofoblasten smälter samman och förlorar sina cellmembran.
Detta cellskikt härstammar från celldifferentiering av cytotrofoblasten och ansvarar för utbytet av gaser och näringsämnen mellan modern och fostret. Dessutom kan den producera hormoner och peptider i blastocystens implantationsfas till endometrium och bildandet av moderkakan..
Artikelindex
- 1 Funktioner
- 2 Roll i embryonal utveckling
- 2.1 Nidering eller implantation
- 2.2 Utero-placenta cirkulation
- 3 Placental apoptos
- 3.1 Apoptos och preeklampsi
- 3.2 Bevis på sambandet mellan apoptos och preeklampsi
- 4 Referenser
Egenskaper
Som namnet antyder har syncytiotrofoblastceller tappat sina membran och smält, vilket ger detta cellskikt ett flerkärnigt syncytialiknande utseende..
Dessa celler täcker kontinuerligt den korioniska villösa ytan, decidua basalis och korionplattan och utgör en del av placentabarriären som är ansvarig för att separera moderns och fostrets blod.
Syncytiotrofoblasten härrör från spridning och fusion av cytotrofoblastceller. Cellerna i detta skikt har inte proliferativ kapacitet, det vill säga de genomgår inte mitos, så expansion och underhåll av detta cellskikt beror bara på kontinuerlig införlivande av celler från cytotrofoblasten, vilket säkerställer dess funktionalitet..
Dessa celler har Golgi-komplex och rikligt med jämn och grov endoplasmatisk retikulum, liksom ett stort antal mitokondrier och lipidinkluderingar..
Detta cellskikt har också en sekretorisk funktion och frigör progesteron, östrogen, humant koriongonadotropin (hCG) och laktogener. När cellmaterial åldras, är det insvept i ett skyddande membran och kastas genom moderns cirkulation..
Roll i embryonal utveckling
Nidation eller implantation
Blastocysten ansluter sig till endometrium och initierar ett stadium av snabb cellproliferation, med differentiering av trofoblasten till cytotrofoblast och syncytiotrofoblast. Det senare sträcker sig genom endometriumepitelet tills det når sitt stroma, där cellerna fylls med lipider och glykogen och blir lövceller..
Dessa lövceller genomgår degenerativa processer som gör att de kan ge näringsämnen till det utvecklande embryot..
När blastocysten är implanterad i endometrium genom implantation eller häckningsprocess, ger fusionen av de yttersta cellerna i trofoblasten upphov till den primitiva syncytiotrofoblasten.
Senare bildas laguner, ockuperade av glandulära sekretioner av endometrium, som senare kommer att ersättas av moderblod, genom att försvaga kapillärkärlen och endometriumvenulerna..
Dessa intracellulära luckor fyllda med moderblod definierar lakunar- eller trabekulär fas och sträcker sig tills de når motsatt sida av implantationspunkten..
Gapet i syncytiotrofoblasten kallas trabeculae. Embryogenes, som består av förändringar i embryoblasten inuti blastocysten, sker också i detta skede..
Utero-placenta cirkulation
En av de grundläggande funktionerna för syncytiotrofoblasten är det metaboliska utbytet mellan modern och fostret, vilket visar en hög endokrin aktivitet och deltar i homeostasen för embryonal utveckling..
Utseendet på intracellulära eller trofoblastiska luckor i syncytiotrofoblasten initierar utvecklingen av den utero-placenta cirkulationen. Sinusoider som härrör från kapillärerna i moderkretsen av moderkakan strömmar in i dessa laguner..
Ett riktningsflöde bildas av differenstrycket mellan cirkulationskärlen och de trofoblastiska lagunerna. Detta flöde går från artärerna till venerna och bildar den primitiva livmodercirkulationen..
Det finns en överföring av näringsämnen från moderkärlen till embryot, vilket är uppenbart när man observerar de rikliga pinocytiska blåsorna i syncytiotrofoblasten..
Det syncytiala cellskiktet leder till placentas flytande villi. Dessa villi kommer i kontakt med moderblodet när livmodercirkulationen upprättas, vilket reglerar transporten av syre och näringsämnen..
Placental apoptos
Apoptos eller programmerad celldöd visar sig vara en viktig komponent i embryonal utveckling, varför eliminering av utvalda celler sker, för att förhindra den urskiljande förlusten av celler. Syncytial fusion av cytotrofoblastceller är den initiala fasen av den apoptotiska kaskaden.
I det inledande skedet av apoptos sprids cytotrofoblastceller och smälter samman för att bilda det syncytiala skiktet eller syncytiotrofoblasten..
Under exekveringsfasen av apoptos har cytotrofoblastens cytoplasmiska och nukleära material passerat in i det syncytiala skiktet, så cellerna i det sista lagret är utrustade med det nödvändiga materialet för att den apoptotiska kaskaden ska kunna starta..
Den apoptotiska processen utgör en tillfällig paus på grund av verkan av antiapoptotiska enzymer, men caspase 3-enzymet återaktiverar denna process, eftersom det i sin tur aktiverar komponenter som bryter ned proteiner och nukleinsyror i celler. Andra enzymer som ansvarar för nedbrytning av cellulära mikrofilament aktiveras.
Efter nedbrytningen av cellkomponenterna förpackas avfallet i syncytiotrofoblastens apikala membran, med ursprung i syncytiala eller apoptotiska noder, som slutligen släpps ut i moderns blodomlopp..
Apoptos och preeklampsi
Preeklampsi är en patologi som presenteras under graviditeten. Viss forskning har visat att denna patologi orsakas av en förändring i differentieringen av trofoblasten på grund av ett överskott av apoptotiska processer på denna nivå.
Utsläppet av apoptotiskt avfall i moderns blodomlopp framkallar inte inflammatoriska reaktioner hos modern eftersom dessa avfall skyddas av ett membran som förhindrar dem från att komma i kontakt med moderns strukturer. Skrotbeläggningsprocessen tar några veckor.
I preeklampsi finns det ett överskott av proliferation och fusion av cytotrofoblastceller, vilket orsakar en ökning av cellulär nedbrytning i syncytiotrofoblasten. Denna ökning orsakar en ansamling av cellulärt skräp och en fördröjning i bildandet av deras skyddande membran..
Detta medför att delvis nedbrytade skräp och mikrofragment, inklusive syncytiotrofoblastenzymer, kommer in i moderns blodomlopp och orsakar vävnadsskador. Förutom preeklampsi har hypoxiska tillstånd i moderkakan associerats med en ökning av cellapoptos.
Bevis för förhållandet mellan apoptos och preeklampsi
Betydande cytoplasmiska koncentrationer av mikrofragment av syncytiotrofoblast har hittats hos patienter med preeklampsi. Dessa mikrofragment kan förändra makrofagbeteende, vilket orsakar både ökad neutrofilaktivering och minskad endotelavslappning..
Dessa förändringar i maternella blodkroppar förklarar systemisk skada och manifestation av preeklampsi, som orsakar epitelskador och ett inflammatoriskt svar. Förutom att orsaka skada på moderkakan på grund av en ökning av fibrinoidavlagringar på villi.
Referenser
- Flores, A. M., Montoya, J. B., Aguilar, A. O., & Ortega, F. V. (2006). Utveckling och validering av en in vitro-odlingsmodell för studier av differentiering av mänsklig trofoblast. Gynekologi och obstetrik i Mexiko, 74 (12), 657-665.
- Hernández-Valencial, M., Valencia-Ortega, J., Ríos-Castillo, B., Cruz-Cruz, P. D. R., & Vélez-Sánchez, D. (2014). Element av implantation och placering: kliniska och melekulära aspekter. Mexikansk tidskrift för reproduktiv medicin, 6 (2), 102-116.
- Reece, E. A., & Hobbins, J. C. (2010). Klinisk obstetrik / Klinisk obstetrik. Panamerican Medical Ed..
- Rodríguez, M., Couve, C., Egaña, G., & Chamy, V. (2011). Placental apoptos: molekylära mekanismer i preeklampsi. Chilensk tidskrift för obstetrik och gynekologi, 76 (6), 431-438.
- Ross, M. H., & Pawlina, W. (2007). Histologi. Panamerican Medical Ed..
- Roura, L. C. (2007). Obstetrics and Maternal-Fetal Medicine. Panamerican Medical Ed..


Ingen har kommenterat den här artikeln än.