
Progressivt sublimeringskoncept, process och exempel

De progressiv sublimering Det är en termodynamisk process där en endoterm tillståndsförändring sker direkt från ett fast ämne till en gas utan föregående bildning av vätskan. Fastämnets beteende under normala förhållanden är att värma upp och smälta; det vill säga att slå samman. Under tiden, i sublimering börjar det fasta ämnet att röka direkt, utan att föregående droppar visar att det smälter..
Det som beskrivs i avsnittet ovan visas i bilden ovan. Anta en fast orange blandning (vänster) som börjar värmas upp. Blandningen består av två komponenter eller fasta ämnen: en gul och en röd, vars kombination resulterar i orange färg..
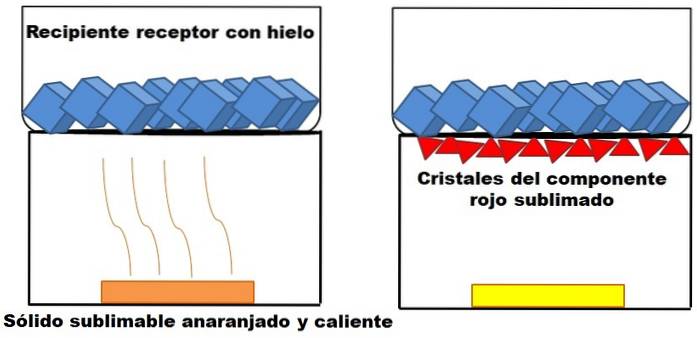
Den röda fasta substansen sublimerar, eftersom en vätska inte bildas av den utan hamnar avsatt (röda trianglar) vid basen av den övre behållaren; den som innehåller isbitar och därför erbjuder en kall yta. Under tiden förblir det gula fasta ämnet oförändrat av värme (gul rektangel).
De röda trianglarna eller kristallerna avsätts tack vare den kalla ytan på den mottagande behållaren (till höger) som absorberar deras temperatur; Och även om den inte visas ska storleken på dina isbitar minska på grund av värmeabsorptionen. Det gula fasta ämnet är inte sublimerbart, och om du fortsätter att värma det smälter det förr eller senare.
Artikelindex
- 1 Progressivt sublimeringskoncept
- 1.1 Process
- 1.2 Från fast struktur till gasstörning
- 1.3 Fasdiagram och trippelpunkt
- 1.4 Villkor
- 2 Exempel
- 2.1 Rening av fasta ämnen
- 2.2 Kristalsyntes
- 3 Referenser
Progressivt sublimeringskoncept
Bearbeta
Det har redan sagts att sublimering är en endotermisk tillståndsförändring, för att det måste ske måste det finnas värmeabsorption. Om det fasta ämnet absorberar värme kommer dess energi att öka, så dess partiklar kommer också att vibrera vid högre frekvenser..
När dessa vibrationer blir mycket starka påverkar de intermolekylära interaktioner (inte kovalenta bindningar); och följaktligen kommer partiklarna förr eller senare att ta större avstånd från varandra tills de lyckas flyta och röra sig mer fritt genom rymdens regioner.
I vissa fasta ämnen är vibrationerna så starka att vissa partiklar "skjuter" ut ur strukturen istället för att agglomera i rörliga kluster som definierar en droppe. Dessa partiklar flyr och bildar den första "bubblan", som hellre bildar de första ångorna från det sublimerade fasta ämnet..
Vi talar då inte om en smältpunkt utan om en sublimeringspunkt. Även om båda är beroende av trycket på det fasta ämnet, är sublimeringspunkten mer; därför varierar temperaturen anmärkningsvärt med tryckförändringar (liksom kokpunkten).
Från solid struktur till gasstörning
I sublimering sägs det också att det ökar systemets entropi. Partiklernas energitillstånd går från att vara begränsade av deras fasta positioner i den fasta strukturen, till att homogenisera i deras nyckfulla och kaotiska riktningar i gasformigt tillstånd, mer enhetlig, där de äntligen får en genomsnittlig kinetisk energi..
Fasdiagram och trippelpunkt
Sublimeringspunkten beror på trycket; för annars skulle de fasta partiklarna absorbera värme för att inte skjuta ut i rymden utanför det fasta materialet utan för att bilda droppar. Det sublimerar inte, men det smälter eller smälter, vilket är det vanligaste.
Ju större yttre tryck, desto mindre troligt är sublimering, eftersom det fasta materialet tvingas smälta.
Men vilka fasta ämnen är sublimerbara och vilka inte? Svaret ligger i dina P vs T-fasdiagram, som den som visas nedan:
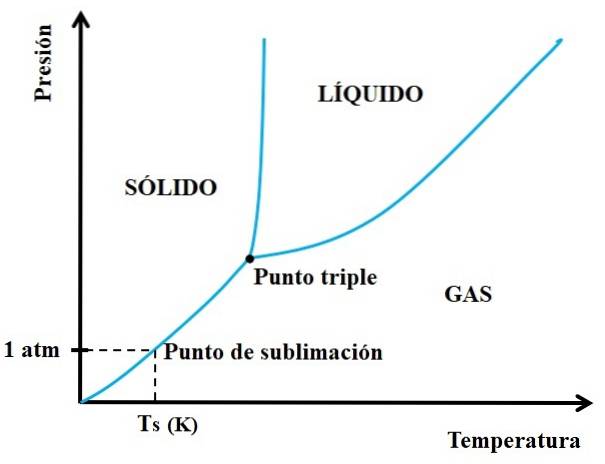
Vi måste först titta på den tredubbla punkten och gå igenom den nedre delen: den som skiljer de fasta och gasformiga tillstånden. Observera att i det fasta området måste det finnas ett tryckfall för att sublimering ska kunna inträffa (inte nödvändigtvis vid 1 atm, vårt atmosfärstryck). Vid 1 atm kommer den hypotetiska substansen att sublimera vid en temperatur Ts uttryckt i K.
Ju längre och horisontellt snittet eller kurvan under den tredubbla punkten, desto större är fastämnets förmåga att sublimera vid olika temperaturer; men om det är långt under 1 atm kommer höga dammsugare att behövas för att uppnå sublimering, på ett sådant sätt att trycket sänks (till exempel 0,0001 atm).
Villkor
Om den tredubbla punkten är tusentals gånger lägre än atmosfärstrycket, kommer det fasta ämnet aldrig att sublimera även när det appliceras ultravakuum (för att inte tala om dess känslighet för sönderdelning genom värmeverkan).
Om detta inte är fallet utförs sublimering genom att värmas måttligt och utsätta det fasta ämnet för ett vakuum så att dess partiklar lättare flyter utan att de behöver absorbera så mycket värme..
Sublimering blir mycket viktigt när det gäller särskilt fasta ämnen med högt ångtryck; det vill säga trycket inuti, en reflektion av effektiviteten i deras interaktioner. Ju högre ångtryck, desto mer doftande är det och desto mer sublimerbart är det..
Exempel
Rening av fasta ämnen
Bilden av det orange fasta ämnet och dess sublimerbara rödaktiga komponent är ett exempel på vad sublimering representerar när det gäller rening av fasta ämnen. Röda trianglar kan sublimeras vid behov tills hög renhet garanteras.
Denna teknik används mestadels med doftande fasta ämnen. Till exempel: kamfer, koffein, bensin och mentol.
Bland andra fasta ämnen som kan vara sublimering har vi: jod, is (i höga höjder), teobromin (från choklad), sackarin, morfin och andra läkemedel, kvävebaser och antracen.
Kristalsyntes
Återgå till de röda trianglarna, sublimering erbjuder ett alternativ till konventionell kristallisation; Kristaller kommer inte längre att syntetiseras från en lösning utan genom den mest kontrollerade möjliga avsättningen av ångor på en kall yta, där det bekvämt kan finnas kristallina frön för att gynna en specifik morfologi.
Säg, om du har röda rutor kommer kristalltillväxten att behålla denna geometri och de borde inte bli triangulära. De röda rutorna kommer gradvis att växa när sublimeringen äger rum. Det är dock ett operativt och molekylärt komplext komplex där många variabler är inblandade..
Exempel på kristaller syntetiserade via sublimering är: kiselkarbid (SiC), grafit, arsenik, selen, fosfor, aluminiumnitrid (AlN), kadmiumsulfid (CdS), zinkselenid (ZnSe), kvicksilverjodid (HgI).två), grafen, bland andra.
Observera att dessa verkligen är två sammanflätade fenomen: progressiv sublimering och deposition (eller invers sublimering); ångan migrerar från det fasta till kallare områden eller ytor och slutligen sätter sig i form av kristaller.
Referenser
- Whitten, Davis, Peck & Stanley. (2008). Kemi. (8: e upplagan). CENGAGE Learning.
- Wikipedia. (2019). Sublimering (fasövergång). Återställd från: en.wikipedia.org
- Jones, Andrew Zimmerman. (27 januari 2019). Sublimering. Återställd från: thoughtco.com
- Sheila Morrissey. (2019). Vad är sublimering i kemi? - Definition, process och exempel. Studie. Återställd från: study.com
- Elsevier B.V. (2019). Sublimeringsmetod. ScienceDirect. Återställd från: sciencedirect.com



Ingen har kommenterat den här artikeln än.