
Acinetobacter baumannii egenskaper, morfologi, symtom
Acinetobacter baumannii Det är en gramnegativ bakterie som tillhör ordningen Pseudomonas. Under hela sin taxonomiska historia har den lokaliserats i släktena Micrococcus, Moraxella, Alcaligenes, Mirococcuscalco-aceticus, Herellea Y Achromobacter, tills den placerades i sin nuvarande genre 1968.
TILL. baumannii det är en patogen bakterie, som anses vara den art som oftast är inblandad i infektioner inom sitt släkte. Det har identifierats som involverat i olika typer av infektioner såsom septikemi, lunginflammation och hjärnhinneinflammation.
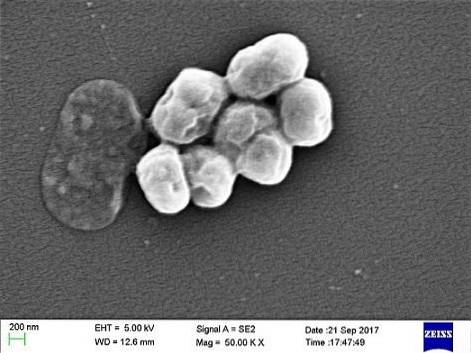
Det är en opportunistisk parasit som har en betydande förekomst i sjukhus eller nosokomiala sjukdomar. Överföring med mekanisk ventilation har identifierats som en viktig orsak till smitta, särskilt i intensivvårdsavdelningar.
Trots att det betraktas som en patogen av låg kvalitet, har den förmågan att öka sin virulens i stammar som är involverade i frekventa infektioner. Den har en stor förmåga att utveckla resistens och multiresistens mot antibiotika.
På sjukhus överförs det främst genom kontakt av personal, genom användning av förorenat sjukhusmaterial och även genom luften över korta avstånd..
Världshälsoorganisationen inkluderar A. baumannii på en lista över resistenta patogener för vilka det krävs akut nya antibiotika, med tilldelning av kategori 1 med kritisk prioritet.
Artikelindex
- 1 Egenskaper för Acinetobacter baumannii
- 2 Morfologi
- 3 Metabolism
- 4 Motståndskraft mot antibiotika
- 5 patologier
- 6 symtom
- 7 Behandling
- 8 Referenser
Kännetecken för Acinetobacter baumannii
Alla arter av släktet Acinetobacter har en bred fördelning i olika naturliga nischer. A. baumannii det kan naturligt bo i huden hos friska människor och kunna kolonisera slemhinnor, vilket utgör en viktig epidemiologisk behållare. Emellertid livsmiljön för A. baumannii är nästan exklusivt för sjukhusinställningar.
Dessa bakterier saknar flageller eller strukturer som används för rörelse. De uppnår emellertid rörelse genom strukturer som gör det möjligt för dem att sträcka sig och dra tillbaka, och genom kemiska mekanismer såsom utsöndring av en film med en högmolekylär exopolysackarid bakom bakterierna..
A. baumannii kan kolonisera ett stort antal levande eller inerta miljöer och har en stor förmåga att överleva på konstgjorda ytor under en längre tid.
Denna förmåga beror möjligen på deras förmåga att motstå uttorkning, att använda olika kolkällor genom olika metaboliska vägar och på grund av förmågan att bilda biofilmer. Av denna anledning är det vanligt att hitta det i sjukhusmaterial, såsom katetrar och mekaniska ventilationsanordningar..
Morfologi
A. baumannii är en coccobacillus, med en mellanliggande form mellan cocci och stavar. De mäter 1,5 till 2,5 gånger 1 till 1,5 mikron när populationer befinner sig i en logaritmisk tillväxtfas. De är mer sfäriska när de når den stationära fasen.
Ämnesomsättning
Bakterierna A. baumannii det är inte en glukosjäser; det är strikt aerobt, det vill säga det kräver syre för dess ämnesomsättning.
Arten av släktet Acinetobacter de är de enda i Moraxellaceae-familjen som saknar cytokrom c-oxidaser, för vilka de ger negativa resultat i oxidastester.
A. baumannii växer vid temperaturer som varierar mellan 20 och 44 ° C, eftersom den är den bästa temperaturen mellan 30 och 35 ° C.
Antibiotikaresistens
Den konstanta genereringen av resistens mot antibiotika hindrar inte bara behandlingen och kontrollen av infektioner orsakade av A. baumannii, det främjar också valet av endemiska och epidemiska multiresistenta stammar.
Några inneboende mekanismer för A. baumannii, som främjar antibiotikaresistens:
- Närvaron av β-laktamaser ger resistens mot b-laktamer.
- Framställningen av specifika enzymer såsom ammoniglukosid-3'-fosfotransferas VI inaktiverar amikacin.
- Närvaron av oxacillinas OXA-51 hydrolyserar penicilliner och karbapenemer.
- Närvaron och överuttrycket av återflödespumpar, som är pumpar som driver ut små molekyler ur cellen som lyckas tränga in i cytoplasman, vilket minskar deras känslighet för antibiotika.
De biofilmer som genereras av A. baumannii förändra metabolismen av mikroorganismer, minska deras känslighet för antibiotika, förutom att ge en fysisk barriär mot stora molekyler och förhindra uttorkning av bakterier.
Patologier
A. baumannii koloniserar en ny värd genom kontakt med smittade personer eller med förorenad medicinsk utrustning. Först och främst fäster denna bakterie sig på huden och slemhinnorna. För att reproducera måste den överleva antibiotika och hämmare och förhållandena på dessa ytor..
Ökningen av antalet bakterier på slemhinnor, särskilt vid sjukhusvistelser i kontakt med intravaskulära katetrar eller endotrakealtubar, kan öka risken för infektion i luftvägarna och blodomloppet..
Sjukhusförvärvad lunginflammation är den vanligaste av infektioner orsakade av A. baumanii. Vanligtvis kontraherade i intensivvårdsavdelningar, av patienter som får mekaniskt assisterad andning.
A. baumanii det har också orsakat stora infektionsproblem hos militärpersonal med efterkrigstrauma, särskilt i Irak och Afghanistan. Specifikt på grund av osteomyelit och mjukvävnadsinfektioner, vilket kan orsaka nekros och cellulit.
Det finns också risker för hjärnhinneinflammation från A. baumanii hos patienter som återhämtar sig från neurokirurgi.
Individer som är mottagliga för infektioner av A. baumanii inkluderar de som tidigare har utsatts för användning av antibiotika, större operationer, brännskador, trauma, immunsuppression eller användning av invasiva medicintekniska produkter, huvudsakligen mekanisk ventilation, i intensivvårdsenheter.
Symtom
Det finns ingen specifik symptom på infektioner av A. baumanii. Var och en av de olika infektioner som produceras av denna bakterie har sina egna karakteristiska symptom..
I allmänhet symtomen på infektioner som kan innebära A. baumanii eller andra opportunistiska bakterier såsom Klebsiella pneumoniae Y Streptococcus pneumoniae, kan inkludera feber, frossa, utslag, smärtsam urinering, akut behov av att urinera ofta, förvirring eller förändrade mentala tillstånd, illamående, muskelsmärta, bröstsmärta och hosta.
Behandling
Antibiotika för att behandla infektioner genom A. baumannii de är extremt begränsade på grund av deras stora förmåga att skaffa motstånd och multiresistorer. Av denna anledning är det viktigt att bestämma känsligheten för varje stam för olika antibiotika för att garantera effektiviteten för varje behandling..
Med tanke på motståndet mot karbapenemer har man använt polymyxiner, speciellt kolistin, trots att det har ett relativt lågt resistensindex och dess biverkningar på njurarna..
Kolistinresistenta stammar har emellertid redan upptäckts. Som ett alternativ till resistens mot dessa antibiotika har kombinationsbehandling använts.
Referenser
- Bergogne-Bérézin, E. & Towner, K.J. Acinetobacter spp. som nosokomiala patogener: mikrobiologiska, kliniska och epidemiologiska egenskaper. Clin Microbiol Rev, 9 (1996), sid. 148-165.
- Fournier, P.E., Richet, H. (2006). Epidemiologi och kontroll av Acinetobacter baumanii i vårdinrättningar. Kliniska infektionssjukdomar, 42: 692-9.
- Hernández Torres, A., García Vázquez, E., Yagüe, G. &, Gómez Gómez, J. (2010) Acinetobacter baumanii Multiresistent: nuvarande klinisk situation och nya perspektiv Revista Española de Quimioterapia, 23 (1): 12-19.
- Maragakis LL, Perl TM. Acinetobacter baumanii: Epidemiologi, antimikrobiell resistens och behandlingsalternativ. Clin Infec Dis 2008; 46: 1254-63.
- McConnell, M.j., Actis, L. & Pachón, J. (2013) Acinetobacter baumannii: mänskliga infektioner, faktorer som bidrar till patogenes och djurmodeller. FEMS Microbiology Reviews, 37: 130-155.
- Peleg, A.Y., Seifert, H. & Paterson, D.L. (2008). Acinetobacter baumannii: framväxten av en framgångsrik patogen. Kliniska mikrobiologiska recensioner, 21 (3): 538-82.
- Vanegas-Múnera, J.M., Roncancio-Villamil, G. & Jiménez-Quiceno, J.N. (2014). Acinetobacter baumannii: klinisk betydelse, resistensmekanismer och diagnos. CES Medicine Magazine, 28 (2): 233-246.


Ingen har kommenterat den här artikeln än.