
Förgrenade alkaner strukturer, egenskaper och exempel
De grenade alkaner de är mättade kolväten vars strukturer inte består av en rak kedja. Raka kedjealkaner skiljer sig från sina grenade isomerer genom att lägga till en bokstav n före namnet. Således betyder n-hexan att strukturen består av sex kolatomer inriktade i en kedja.
Grenarna på ett kalt trädtak (lägre bild) kunde jämföras med grenarna på grenade alkaner; Emellertid har tjockleken på dess kedjor, vare sig de är huvud-, sekundära eller tertiära, alla har samma dimensioner. Varför? Eftersom det finns enkla C-C-bindningar i dem alla.

Träd tenderar att förgrena sig när de växer; så gör alkaner. Håll en konstant kedja med vissa metylenenheter (-CHtvå-) innebär en serie energiska förhållanden. Ju mer energi alkanerna har, desto större är tendensen att förgrena sig.
Både linjära och grenade isomerer har samma kemiska egenskaper, men med små skillnader i kokning, smältning och andra fysikaliska egenskaper. Ett exempel på en grenad alkan är 2-metyl-propan, det enklaste av allt.
Artikelindex
- 1 Kemiska strukturer
- 2 Kemiska och fysikaliska egenskaper
- 2.1 Kok- och smältpunkter
- 2.2 Densitet
- 3 Nomenklatur och exempel
- 4 Referenser
Kemiska strukturer
Grenade och linjära alkaner har samma allmänna kemiska formel: CnH2n + 2. Det vill säga att båda för ett givet antal kolatomer har samma antal väten. Därför är de två typerna av föreningar isomerer: de har samma formel men olika kemiska strukturer..
Vad observeras först i en linjär kedja? Ett begränsat antal metylengrupper, -CHtvå-. Således kan ch3CHtvåCHtvåCHtvåCHtvåCHtvåCH3 är en rak kedjealkan som kallas n-heptan.
Notera de fem på varandra följande metylengrupperna. Det bör också noteras att dessa grupper utgör alla kedjor och därför har samma tjocklek men med varierande längder. Vad mer kan man säga om dem? Vilket är 2º kol, det vill säga kol kopplat till två andra.
För att nämnda n-heptan ska förgrenas är det nödvändigt att omorganisera dess kol och väten. Hur? Mekanismerna kan vara mycket komplexa och involvera migrering av atomer och bildandet av positiva arter som kallas karbocations (-C+).
På papper räcker det dock att ordna strukturen på ett sådant sätt att det finns tredje och fjärde kol; med andra ord kol som är bundna till tre eller fyra andra. Denna nya beställning är mer stabil än de långa grupperingarna av CH-gruppertvå. Varför? Eftersom det tredje och fjärde kolet är energiskt mer stabilt.
Kemiska och fysikaliska egenskaper
Grenade och linjära alkaner med samma atomer bibehåller samma kemiska egenskaper. Deras bindningar förblir enkla, C-H och C-C, och med liten skillnad i elektronegativiteter, så deras molekyler är apolära. Skillnaden, som nämnts ovan, ligger i det tredje och fjärde kolet (CHR3 och CR4).
Men när kedjan förgrenas till isomererna ändras hur molekylerna interagerar med varandra..
Exempelvis är sättet att förena två linjära grenar av ett träd inte detsamma som att sätta två högt grenade på varandra. I den första situationen är det mycket ytkontakt, medan i det andra "mellanrummen" mellan grenarna dominerar. Vissa grenar interagerar mer med andra än med huvudgrenen.
Allt detta resulterar i liknande värden, men inte detsamma i många av de fysiska egenskaperna.
Kok- och smältpunkter
De flytande och fasta faserna av alkaner utsätts för intermolekylära krafter under specifika betingelser för tryck och temperatur. Eftersom molekylerna i de grenade och linjära alkanerna inte interagerar på samma sätt kommer inte deras vätskor eller fasta ämnen att vara desamma..
Smält- och kokpunkter ökar med antalet kol. För linjära alkaner är dessa proportionella mot n. Men för grenade alkaner beror situationen på hur grenad huvudkedjan är och vad substituenten eller alkylgrupperna är (R).
Om linjära kedjor betraktas som rader med sicksack, kommer de att passa perfekt varandra ovanpå varandra; men med de grenade kedjorna interagerar knappast huvudkedjorna eftersom substituenterna håller dem ifrån varandra.
Som ett resultat har grenade alkaner en mindre molekylär kontaktyta och därför tenderar deras smält- och kokpunkter att vara något lägre. Ju mer grenad strukturen desto lägre kommer dessa värden att vara.
Till exempel n-pentan (CH3CHtvåCHtvåCHtvåCH3) har en Peb på 36,1 ° C, medan 2-metyl-butan (CH3CHtvå(CH3) CHtvåCH32,2-dimetylpropan (C (CH3)4) på 27,8 och 9,5 ° C.
Densitet
Med samma resonemang är grenade alkaner något mindre täta på grund av att de upptar en större volym på grund av minskningen av ytkontakten mellan huvudkedjorna. Liksom linjära alkaner är de oblandbara med vatten och flyter ovanför det; de är mindre täta.
Nomenklatur och exempel
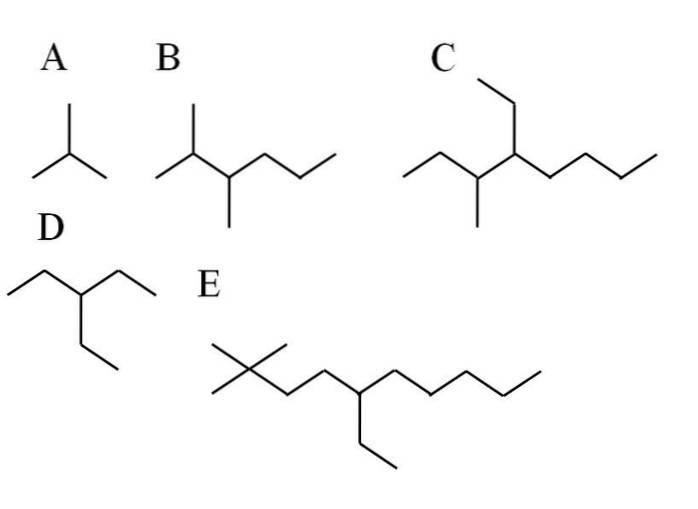
Fem exempel på grenade alkaner visas i bilden ovan. Observera att grenarna kännetecknas av att de har tredje eller fjärde kol. Men vad är huvudkedjan? Den med flest kolatomer.
-I A spelar det ingen roll, eftersom oavsett vilken kedja som väljs har de båda 3 C. Så deras namn är 2-metyl-propan. Det är en isomer av butan, C4H10.
-Alkane B har vid första anblicken två substituenter och en lång kedja. Till -CH-grupper3 de är numrerade på ett sådant sätt att de har minst antal; därför börjar kolet räknas från vänster sida. Således kallas B 2,3-dimetyl-hexan.
-För C gäller samma sak som för B. Huvudkedjan har 8 C, och de två substituenterna, en CH3 och en CHtvåCH3 de är mer till vänster. Dess namn är därför: 4-etyl-3-metyloktan. Observera att -etylsubstituenten nämns före -metylen i sin alfabetiska ordning.
-När det gäller D, spelar det ingen roll var huvudkedjans kol räknas. Dess namn är: 3-etyl-propan.
-Och slutligen för E, en lite mer komplex grenad alkan, har huvudkedjan 10 C och den börjar räkna från någon av CH-grupperna3 till vänster. Gör det så här är namnet: 5-etyl-2,2-dimetyl-dekan.
Referenser
- Carey, F. A. (2006). Organic Chemistry Sixth Edition. Ledare Mc Graw Hill, sidorna 74-81.
- John T. Moore, Chris Hren, Peter J. Mikulecky. Hur man namnge grenade alkaner i kemi. Återställd från: dummies.com
- Dr. Ian Hunt. (2014). Enkla grenade alkaner. Hämtad från: chem.ucalgary.ca
- Helmenstine, Anne Marie, Ph.D. (8 januari 2018). Grenad kedjedefinition. Återställd från: thoughtco.com
- Kemi LibreTexts. Filialkedjor. Hämtad från: chem.libretexts.org
- Alkaner: struktur och egenskaper. Hämtad från: uam.es
- Nomenklatur: alkaner. [PDF]. Hämtad från: quimica.udea.edu.co


Ingen har kommenterat den här artikeln än.