
Latent värme

Vad är latent värme?
Latent värme är mängden värme som ett ämne behöver absorbera eller släppa ut för att ändra sitt fysiska tillstånd eller fas och hålla temperaturen konstant under denna process. Värmen som tillförs eller släpps manifesterar sig inte, den "känns" inte som vanligt i en temperaturvariation; därav termen latent värme.
Det latenta ordet kommer från det latinska ordet "latens" vilket betyder dold, så latent värme beter sig som om det inte fanns när temperaturen hölls konstant. Men det existerar: vad som händer är att det konsumeras totalt i fasförändringen eller det fysiska tillståndet.
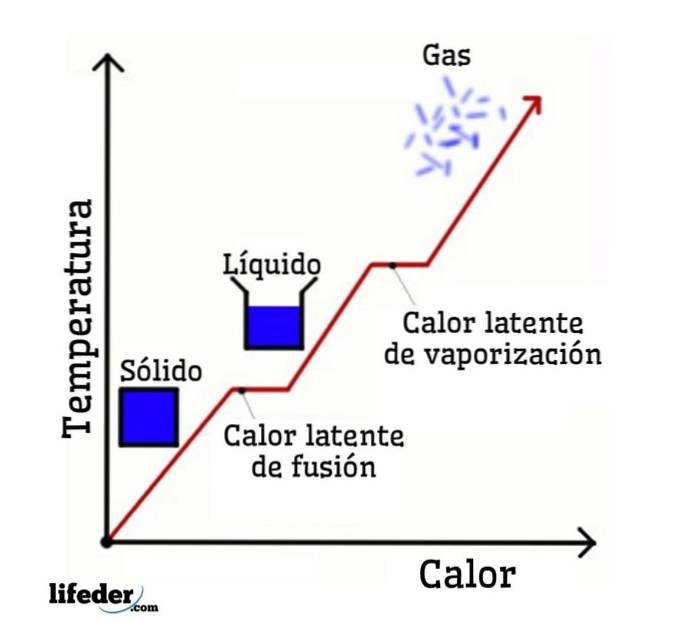
Med vatten som ett exempel är fasförändringarna följande: is (fast) smälter i flytande vatten (flytande) i en process som kallas smältning; och flytande vatten förångas i sin tur för att omvandlas till vattenånga (gas) i en process som kallas förångning.
Å andra sidan kyls vattenånga till flytande vatten i en process som kallas kondens; och flytande vatten förvandlas tillbaka till is i en process som kallas stelning.
Var och en av dessa fasförändringar är associerad med en latent värme, som kan vara positiv (absorption) eller negativ (frisättning)..
Latent fusionsvärme

Det är mängden värme som måste tillföras till en viss mängd fast ämne för att ändra dess fysiska tillstånd från fast till flytande. Under fusion sker ingen temperaturförändring, så medan fastämnet smälter eller smälter har vätskan som genereras från den samma temperatur som hela fastämnet.
I allmänhet bestäms denna värme vid den normala smältpunkten, vilket är den temperatur vid vilken fastämnet börjar smälta under atmosfärstryck. Vid denna temperatur finns en jämvikt eller samtidig närvaro av fast tillstånd och flytande tillstånd samtidigt..
Fast tillstånd kännetecknas av närvaron av en kompakt struktur på grund av förekomsten av högenergiska kemiska bindningar, vilket ger den strukturell styvhet. För omvandlingen av ett fast ämne till vätska måste dessa interaktioner brytas, så energi förbrukas (absorberas) för det ändamålet.
Ett typiskt exempel är när en glass konsumeras, bestående av vatten, socker och andra ämnen. Det är vanligt att observera att glass, om den inte konsumeras snabbt, börjar smälta, det vill säga smälta. Detta inträffar när glassens temperatur når isens smältpunkt..
Exempel
Några exempel på latenta värme av fusion uttryckt i J / g kommer att listas; det vill säga den energi som ett gram fast ämne måste absorbera för att smälta vid smältpunkten:
-Ice 334.0
-Aluminium 380.0
-Svavel 38,1
-Koppar 134.0
-Etanol 104,0
-Kvicksilver 11.8
-Guld 64,5
-Silver 80.3
-Bly 24.5
-Volfram 184
Is absorberar mycket värme inte för att dess interaktioner är starkare, utan för att det kan sprida värme exceptionellt mellan kristallerna..
Latent förångningsvärme
Det är mängden värme som en viss mängd ämne absorberar för att växla från flytande tillstånd till gasform vid den normala kokpunkten. Det vill säga det är värmen som vätskan absorberar när den kokar och förvandlas till gas utan en temperaturökning..
Inom vätskan kan ämnens molekyler interagera genom bildandet av vätebindningar och genom attraktionskrafter mellan molekylerna. För att överföra ett ämne från flytande tillstånd till gasform måste dessa krafter övervinnas, så värme måste tillföras.
Känslig värme är vad vätskan absorberar bara för att öka temperaturen, vilket beror på dess specifika värme. Under tiden används den latenta förångningsvärmen för att omvandla den direkt till ånga, en process som är mycket lättare vid kokpunkten..
Exempel
Nedan listas exempel på vissa vätskor med deras respektive latenta förångningsvärme återigen uttryckta i J / g:
-Ättiksyra 402
-Aceton 518
-Vatten 2256
-Etylalkohol 846
-Svavel 1510
-Bensen 390
-Koldioxid 574
-Klor 293
-Ether 377
-Glycerin 974
-Kvicksilver 295
-Syre 214
Observera den enorma latenta värmen av flytande vatten: 1 g flytande vatten (cirka 1 ml) behöver absorbera 2256 J för att förångas. Flytande vatten släpper ut värmen det får ännu bättre jämfört med is.
Latent stelningsvärme
Det är värmen som en viss mängd ämne måste avge för att gå från dess flytande tillstånd till sitt fasta tillstånd vid stelning eller frysning. Återigen, tills vätskan har stelnat helt, kommer temperaturen att förbli konstant..
Stelningsprocessen är det motsatta av fusionsprocessen, så värdena för den latenta stelningsvärmen och de för den latenta fusionsvärmen är desamma, men med motsatta tecken..
Molekylerna i ett ämne i flytande tillstånd rör sig med en viss frihet på grund av den energi de besitter. För att passera till den fasta fasen måste därför molekylerna frigöra energi i form av värme, vilket möjliggör större interaktion mellan ämnets molekyler..
Interaktionen mellan molekylerna gynnar bildandet av de kemiska bindningarna i den fasta fasen. Ett exempel på detta inträffar när flytande vatten placeras i de isbildande behållarna i kylen. Frysen extraherar värme från det flytande vattnet och den stelnar och blir is.
Exempel
Några exempel på latenta stelningar (i J / g) för vissa vätskor listas nedan:
-Vatten (-334)
-Aluminium (-380)
-Svavel (-38)
-Koppar (-134)
-Etanol (-104)
Latent kondensvärme
Det är mängden värme som måste avges eller frigöras från en viss mängd substans för att gå från gasformigt tillstånd till flytande tillstånd. Gasen som kondenserar och vätskan som bildas bibehåller samma temperatur under kondens.
Kondens är motsatsen till förångning. Den latenta kondensvärmen har samma värde som den latenta förångningsvärmen, men med motsatt tecken och vid kokpunkten. Ett exempel på detta är när matlagning och ånga kondenserar på insidan av krukorna..
Gasformiga molekyler rör sig fritt drivna av den energi de besitter. Därför måste de frigöra energi för att möjliggöra intermolekylära interaktioner mellan flytande tillstånd mellan ämnets molekyler..
I naturen finns det många andra exempel på fenomenet vattenkondensation. Vattenånga stiger i atmosfären och kondenserar i molnen i form av vattendroppar.
Förekomsten av vattendroppar i bilfönster observeras också som ett resultat av kondensering av vatten på grund av en temperaturfall som inträffar tidigt på morgonen, vilket utgör den så kallade daggen.
Exempel
Slutligen, för vissa ångor kommer deras respektive latenta kondensvärme, återigen, i J / g att listas:
-Ättiksyra (-402)
-Aceton (-518)
-Vatten (-2256)
-Etylalkohol (-846)
-Svavel (-1510)
-Bensen (-390)
Referenser
- Whitten, Davis, Peck & Stanley. (2008). Kemi. (8: e upplagan). CENGAGE Learning.
- Walter J. Moore. (1963). Fysisk kemi. Inom kemisk kinetik. Fjärde upplagan, Longmans.
- Wikipedia. (2020). Latent värme. Återställd från: en.wikipedia.org
- Redaktörerna för Encyclopaedia Britannica. (2020). Latent värme. Återställd från: britannica.com
- Verktygslåda för teknik. (2003). Vätskor: Latent avdunstningsvärme. Återställd från: engineeringtoolbox.com
- Lumen inlärning. (s.f.). Fasförändring och latent värme. Återställd från: courses.lumenlearning.com


Ingen har kommenterat den här artikeln än.