
Fosfatidyletanolaminstruktur, biosyntes och funktioner
De fosfatidyletanolamin (PE) är en glycerofosfolipid riklig i plasmamembranen hos prokaryota organismer. Tvärtom, i eukaryota cellmembran är detta den näst vanligaste glycerofosfolipiden på insidan av plasmamembranet efter fosfatidylkolin..
Trots överflödet av fosfatidyletanolamin beror dess överflöd inte bara på celltypen utan också på facket och ögonblicket för den specifika celllivscykel som övervägs..
Biologiska membran är barriärer som definierar cellulära organismer. Inte bara har de skydds- och isoleringsfunktioner, men de är också nyckeln till att skapa proteiner som kräver en hydrofob miljö för att de ska fungera optimalt..
Både eukaryoter och prokaryoter har membran som huvudsakligen består av glycerofosfolipider och i mindre utsträckning sfingolipider och steroler..
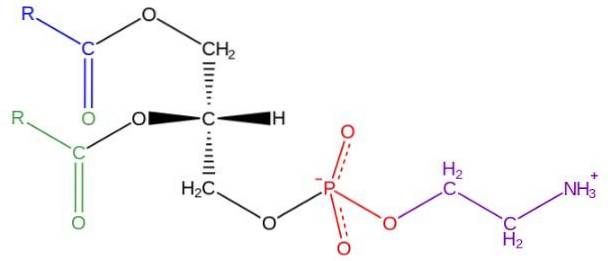
Glycerofosfolipider är amfipatiska molekyler strukturerade på en L-glycerolkedja som förestras vid sn-1 och sn-2-positionerna av två fettsyror med varierande längd och mättnadsgrad. I hydroxylen i sn-3-positionen förestras den av en fosfatgrupp, till vilken i sin tur olika typer av molekyler kan fästas som ger upphov till olika klasser av glycerofosfolipider.
I den cellulära världen finns det en mängd olika glycerofosfolipider, men de vanligaste är fosfatidylkolin (PC), fosfatidyletanolamin (PE), fosfatidylserin (PS), fosfatidylinositol (PI), fosfatidinsyra (PA), fosfatidylglycerol (PG) och kardiolipin (CL).
Artikelindex
- 1 Struktur
- 2 Biosyntes
- 2.1 Kennedy-rutten
- 2.2 PSD-sökväg
- 3 funktioner
- 4 Referenser
Strukturera
Strukturen av fosfatidyletanolamin upptäcktes av Baer et al. 1952. Som har fastställts experimentellt för alla glycerofosfolipider, bildas fosfatidyletanolamin av en glycerolmolekyl förestrad i sn-1 och sn-2-positionerna med syrakedjor som är feta med mellan 16 och 20 kolatomer.
Fettsyrorna förestrade i sn-1-hydroxylen är vanligtvis mättade (utan dubbelbindningar) med maximala längder av 18 kolatomer, medan kedjorna kopplade i sn-2-positionen är längre och med en eller flera omättningar (dubbelbindningar).
Graden av mättnad av dessa kedjor bidrar till membranets elasticitet, vilket har stor inverkan på insättning och sekvestrering av proteiner i dubbelskiktet..
Fosfatidyletanolamin anses vara en icke-lamellär glycerofosfolipid, eftersom den har en konisk geometrisk form. Denna form ges av den lilla storleken på dess polära grupp eller "huvud", i förhållande till den hos fettsyrakedjorna som innefattar de hydrofoba "svansarna".
"Huvudet" eller den polära gruppen av fosfatidyletanolamin har en zwitterjonisk karaktär, det vill säga den har grupper som kan laddas positivt och negativt under vissa pH-betingelser..
Denna egenskap gör det möjligt att vätebindas med ett stort antal aminosyrarester och dess laddningsfördelning är en väsentlig faktor för domäntopologin för många integrerade membranproteiner..
Biosyntes
I eukaryota celler är syntesen av strukturella lipider geografiskt begränsad, den huvudsakliga biosyntesplatsen är endoplasmatisk retikulum (ER) och i mindre utsträckning Golgi-apparaten..
Det finns fyra oberoende biosyntetiska vägar för produktion av fosfatidyletanolamin: (1) CDP-etanolaminvägen, även känd som Kennedy-vägen; (2) PSD-vägen för fosfatidylserin (PS) dekarboxylering; (3) acylering av lyso-PE och (4) basförändringsreaktioner hos den polära gruppen av andra glycerofosfolipider.
Kennedy Route
Fosfatidyletanolaminbiosyntes genom denna väg är begränsad till ER och det har visat sig att det i hamsterleverceller är den huvudsakliga produktionsvägen. Den består av tre på varandra följande enzymatiska steg katalyserade av tre olika enzymer.
I det första steget produceras fosfoetanolamin och ADP tack vare verkan av etanolaminkinas, som katalyserar den ATP-beroende fosforyleringen av etanolamin..
Till skillnad från växter kan varken däggdjur eller jäst producera detta substrat, så det måste konsumeras i kosten eller erhållas från nedbrytning av befintliga fosfatidyletanolamin- eller sfingosinmolekyler..
Fosfoetanolamin används av CTP: fosfoetanolamincytidyltransferas (ET) för att bilda högenergiföreningen CDP: etanolamin och ett oorganiskt fosfat.
1,2-diacylglyceroletanolaminfosfotransferas (ETP) använder energin i CDP-etanolaminbindningen för att kovalent binda etanolamin till en membraninsatt diacylglycerolmolekyl, vilket ger upphov till fosfatidyletanolamin..
Rutt PSD
Denna rutt fungerar både i prokaryoter och i jäst och däggdjur. Hos bakterier förekommer det i plasmamembranet, men i eukaryoter förekommer det i ett område av det endoplasmiska retikulum som är nära besläktat med mitokondriellt membran.
I däggdjur katalyseras vägen av ett enda enzym, fosfatidylserindekarboxylas (PSD1p), som är inbäddat i mitokondriellt membran, vars gen kodas av kärnan. Reaktionen innefattar dekarboxylering av PS till fosfatidyletanolamin.
De återstående två vägarna (PE-lyso-acylering och polargruppberoende kalciumutbyte) förekommer i det endoplasmiska retikulumet, men bidrar inte signifikant till total fosfatidyletanolaminproduktion i eukaryota celler..
Funktioner
Glycerofosfolipider har tre huvudfunktioner i cellen, bland vilka strukturfunktionerna, energilagring och cellsignalering sticker ut..
Fosfatidyletanolamin är förknippat med förankring, stabilisering och vikning av flera membranproteiner, liksom de anpassningsförändringar som är nödvändiga för att många enzymer ska fungera..
Det finns experimentella bevis som föreslår fosfatidyletanolamin som en avgörande glycerofosfolipid i det sena stadiet av telofas, under bildandet av den sammandragna ringen och upprättandet av fragmoplasten som möjliggör uppdelningen av membranet hos de två dottercellerna..
Det har också en viktig roll i alla processer av fusion och fission (förening och separation) av membranen i både det endoplasmiska retikulumet och Golgi-apparaten..
I E. coli har det visat sig att fosfatidyletanolamin är nödvändig för korrekt vikning och funktion av enzymet laktospermeas, varför det har föreslagits att det spelar en roll som en molekylär "chaperone".
Fosfatidyletanolamin är den huvudsakliga givaren av etanolaminmolekylen som är nödvändig för post-translationell modifiering av många proteiner, såsom GPI-ankare.
Denna glycerofosfolipid är föregångaren till många molekyler med enzymatisk aktivitet. Dessutom kan molekyler härledda från dess ämnesomsättning, liksom diacylglycerol, fosfatidinsyra och vissa fettsyror, fungera som andra budbärare. Dessutom är det ett viktigt substrat för produktion av fosfatidylkolin..
Referenser
- Brouwers, J. F. H. M., Vernooij, E. A. A. M., Tielens, A. G. M., & van Golde, L. M. G. (1999). Snabb separation och identifiering av fosfatidyletanolaminmolekylära arter. Journal of Lipid Research, 40 (1), 164-169. Återställd från jlr.org
- Calzada, E., McCaffery, J. M., & Claypool, S. M. (2018). Fosfatidyletanolamin som produceras i det inre mitokondriella membranet är viktigt för jästcytokrom bc1-komplexfunktion 3. BioRxiv, 1, 46.
- Calzada, E., Onguka, O., & Claypool, S. M. (2016). Fosfatidyletanolaminmetabolism i hälsa och sjukdom. International Review of Cell and Molecular Biology (Vol. 321). Elsevier Inc..
- Gibellini, F., & Smith, T. K. (2010). Kennedy pathway-de novo-syntesen av fosfatidyletanolamin och fosfatidylkolin. IUBMB Life, 62 (6), 414-428.
- Harayama, T., & Riezman, H. (2018). Förstå mångfalden av membran lipidkomposition. Nature Reviews Molecular Cell Biology, 19 (5), 281-296.
- Luckey, M. (2008). Membranstrukturbiologi: med biokemiska och biofysiska fundament. Cambrudge University Press. Återställd från cambrudge.org
- Seddon, J. M., Cevc, G., Kaye, R. D., & Marsh, D. (1984). Röntgendiffraktionsstudie av polymorfism av hydrerade diacyl- och dialkylfosfatidyletanolaminer. Biokemi, 23 (12), 2634-2644.
- Sendecki, A. M., Poyton, M. F., Baxter, A. J., Yang, T., & Cremer, P. S. (2017). Stödda lipidskikt med fosfatidyletanolamin som huvudkomponent. Langmuir, 33 (46), 13423-13429.
- van Meer, G., Voelker, D. R., & Feignenson, G. W. (2008). Membranlipider: var de är och hur de beter sig. Nature Reviews, 9, 112-124.
- Vance, J. E. (2003). Molekylär och cellbiologi av fosfatidylserin och fosfatidyletanolaminmetabolism. I K. Moldave (red.), Progress Nucleic Acid Research and Molecular Biology (s. 69-111). Academic Press.
- Vance, J. E. (2008). Fosfatidylserin och fosfatidyletanolamin i däggdjursceller: två metaboliskt relaterade aminofosfolipider. Journal of Lipid Research, 49 (7), 1377-1387.
- Vance, J. E., & Tasseva, G. (2013). Bildning och funktion av fosfatidylserin och fosfatidyletanolamin i däggdjursceller. Biochimica et Biophysica Acta - Molecular and Cell Biology of Lipids, 1831 (3), 543-554.
- Watkins, S. M., Zhu, X., & Zeisel, S. H. (2003). Fosfatidyletanolamin-N-metyltransferasaktivitet och kostkolin reglerar lipidflöde i lever-plasma och essentiell fettsyrametabolism hos möss. Journal of Nutrition, 133 (11), 3386-3391.


Ingen har kommenterat den här artikeln än.