
Isomeri
Vad är isomerism?
Isomerism är ett kemiskt fenomen som kännetecknas av att molekyler med samma antal atomer har olika kemiska eller fysiska egenskaper. Således förekommer det i isomerer, som i sin tur är molekyler vars kemiska formler är desamma, men deras strukturer eller rumsliga arrangemang skiljer sig väsentligt från varandra..
Vi har konstitutionell eller strukturell isomerism och rumslig isomerism, som koncentrerar mycket uppmärksamhet på stereokemi. Flödesschemat i bilden nedan visar att isomerer huvudsakligen är indelade i de två just nämnda typerna av isomerism: konstitutionella och stereoisomerer..
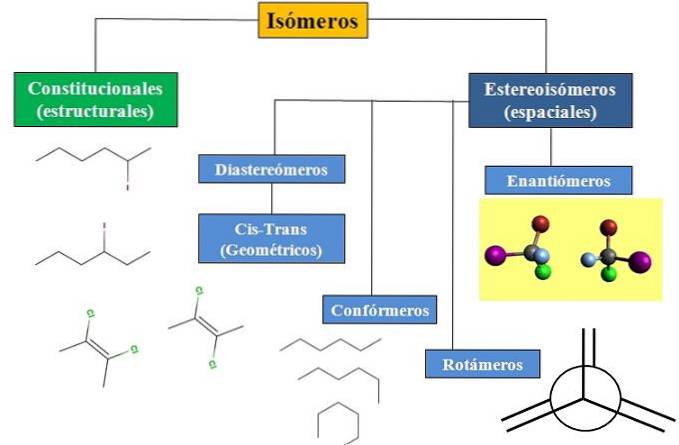
Alla isomerer, för en viss förening, har samma kemiska formel. Men strukturerna som dessa atomer kan bygga och deras proportioner är unika för varje molekyl eller isomer. Även om själva strukturen är densamma kan atomerna eller grupperna uppta olika rumsliga positioner..
Flödesschemat visar några exempel på isomerer som kommer att diskuteras i nästa avsnitt..
Typer av isomerer
Konstitutionell
Konstitutionella eller strukturella isomerer är de som skiljer sig åt i ordningen av den molekylära ryggraden. Det vill säga att deras atomer inte är länkade på samma sätt, så strukturen eller funktionella grupper i fråga kan bli väldigt olika..
Till exempel för samma kemiska formel C7H10Eller så kan det finnas flera molekyler som möter det antalet atomer; de kommer alla att ha en enda syreatom, men de andra atomernas strukturella arrangemang kommer att vara unikt för varje isomer.
Och därav kemiska och fysikaliska egenskaper hos alla konstitutionella isomerer för formel C7H10Eller så skiljer de sig också mycket från varandra.
Å andra sidan kan konstitutionella isomerer vara väldigt enkla och varierar endast i den relativa positionen för en enda atom eller grupp. I nästa avsnitt kommer du att se ett exempel på detta och ovanstående sagt.
Stereoisomerer
Stereoisomerer är de som har samma strukturella ordning, men skiljer sig åt i deras atomer eller gruppers positioner och rumsliga orienteringar..
För att deras existens ska vara möjlig måste molekyler innehålla stereogena centra, de mest kända inom organisk kemi är asymmetriska eller kirala kolatomer; det vill säga med fyra olika substituenter.
Förutom asymmetriska kol måste den betraktade molekylen sakna element av symmetri. Annars är det omöjligt för den rumsliga ordningen att bli stereoisomerism..
Enantiomerer
Enantiomerer är stereoisomerer som består av icke-överlappande spegelbilder. Till exempel överlappar inte högra och vänstra händer, liksom skor eller handskar. I nästa avsnitt behandlas det klassiska exemplet på enantiomerism: bromklordometan: CBrClI.
Diastereomerer
Diastereomerer, å andra sidan, är också stereoisomerer men de är inte spegelbilder. Det vill säga att det som placeras framför varandra är inte en reflektion av sig själva. Av de mest kända diastereomererna har vi cis-trans-isomerismen, även kallad geometrisk isomerism, speciellt när den appliceras på alkener.
Överensstämmande
Även om konformare är inom stereoisomerismens spektrum är de egentligen inte isomerer. De är rumsliga konfigurationer som en molekyl, vid ett visst ögonblick eller energitillstånd, förvärvar genom rotation av flera av dess bindningar. Vi kommer att se i nästa avsnitt exemplet på överensstämmelsen med n-hexan.
Rotamerar
Slutligen har vi rotamerer, som liknar konformare i den meningen att de är beroende av rotationen av kovalenta bindningar..
Emellertid tas en enda bindning mellan två kolatomer som referens, och de relativa positionerna, oavsett om de är förmörkade eller alternerade, för substituenterna för båda kolerna jämförs. Senare kommer vi att se exemplet med propylenrotamerer.
Exempel på isomerer
Hexanjod
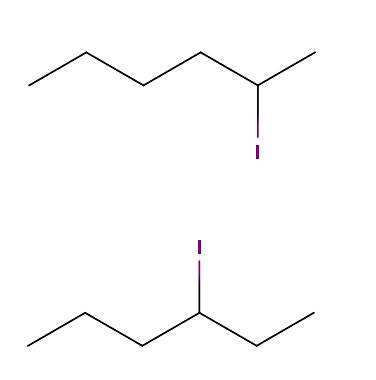
Ovan har vi två molekyler vars kemiska formler är C6H13I. I den första har vi 2-jodhexan, medan den andra har 3-jodhexan. De är konstitutionella isomerer av positionstyp, eftersom skelettet är detsamma, med skillnaden att jodatomens position varierar från ett kol till ett annat..
C3H8ELLER
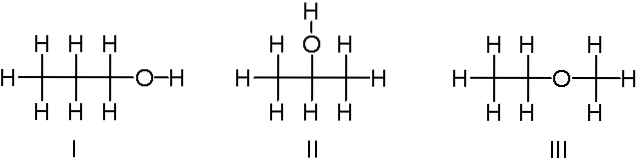
Ovan har vi ett annat exempel på konstitutionella isomerer för den kemiska formeln C3H8O. Molekylerna I och II är 1-propanol respektive 2-propanol. De är båda alkoholer. I stället handlar molekyl III om etylmetyleter.
Därför talar vi om en annan funktionell grupp. Observera att de tre molekylerna har samma antal atomer, men deras strukturer är olika..
2,3-diklor-2-buten
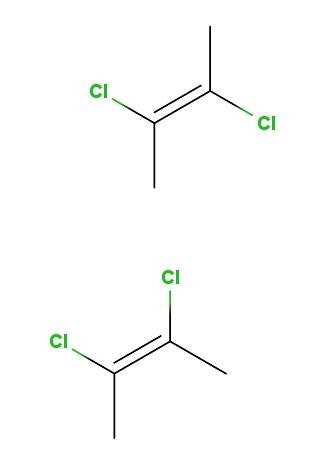
Ovan har vi trans-2,3-diklor-2-buten-isomeren och nedan har vi cis-2,3-diklor-2-buten-isomeren. I den första är kloratomerna i motsatta positioner med avseende på dubbelbindningen, medan de i den andra ligger på samma sida av dubbelbindningen..
Ryggraden för båda molekylerna är densamma, men de skiljer sig åt i kloratomernas rumsliga positioner; därför är de stereoisomerer, och eftersom de inte är spegelbilder, blir de diastereomerer.
3-fluor-2-metylcyklohexan
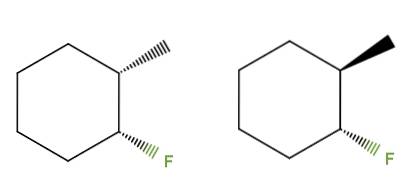
Denna gång, istället för en dubbelbindning, har vi en cyklohexanring för föreningen 3-fluoro-2-metylcyklohexan. I den vänstra isomeren grupperar CH3 och F är under ringen; medan i den till höger, CH3 är upp och F är nere.
Därför skulle den till vänster motsvara cis-isomeren, och den till höger skulle vara trans-isomeren. De är därför diastereomerer, för igen är de inte spegelbilder.
Uppföljare av n-hexan
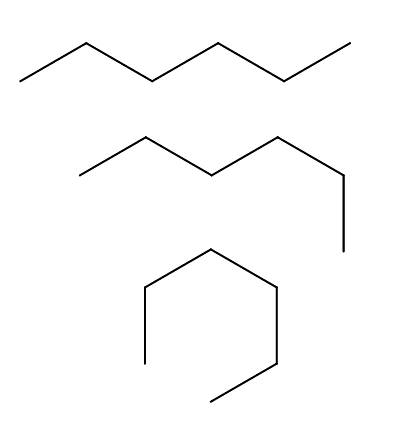
Vi har över tre överensstämmelser med n-hexan, som härrör från kol-kedjans rotationer och "böjningar" i olika riktningar. De motsvarar alla samma molekyl av n-hexan med olika vikningsnivåer, vilket beror på miljön och den inre energin i varje molekyl.
3-brom-2-pentanol
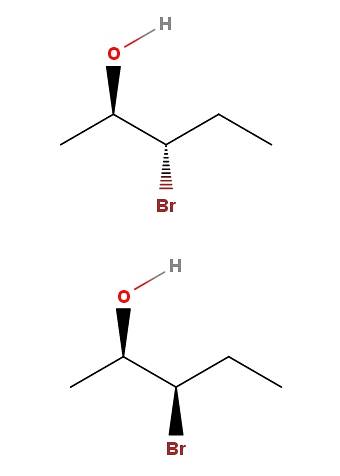
I 3-bromo-2-pentanol har vi ett annat exempel på ett par diastereomerer. Observera att återigen, i isomeren ovan har vi OH och Br som pekar i motsatta riktningar av skelettplanet; medan i den nedre isomeren pekar båda grupperna mot läsarens riktning.
1-brom-3-klor-5-etylcyklohexan
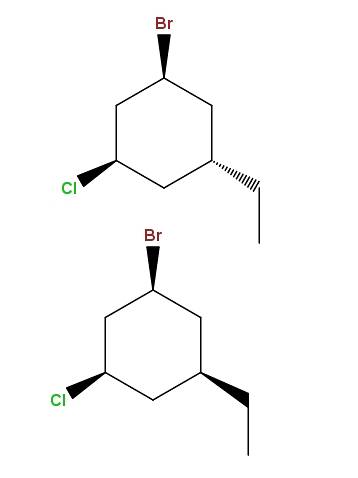
Och återigen har vi ytterligare ett par diastereomerer, med skillnaden att nu ligger skillnaden i en enskild grupps rumsliga position: etylen, -CHtvåCH3.
Denna typ av isomerer har ett mycket specifikt namn: epimerer, som är diastereomerer vars variation endast observeras i den rumsliga konfigurationen av ett enda asymmetriskt kol; i detta fall den som är bunden till -CHtvåCH3.
Bromkloroyodometan
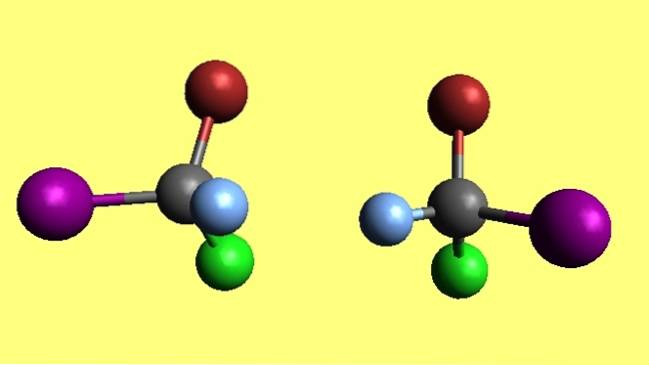
Observera att de två bromklorojodmetanmolekylerna, CBrClI, är enantiomerer eftersom den ena är den icke-överlagrade reflektionen av den andra. Oavsett hur hårt du försöker, dess fyra atomer kommer aldrig att matcha. De sägs ha motsatta rumsliga konfigurationer.
2-brom-4-etylcyklohexan
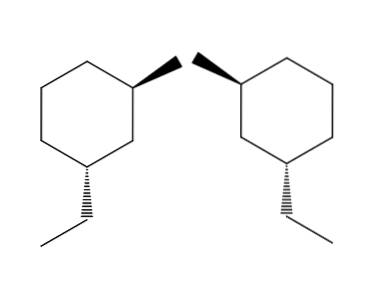
I exemplet med 2-brom-4-etylcyklohexanparet av molekyler är enantiomerismen ännu tydligare. Om vi försöker vända molekylen till höger ser vi att -CH-gruppentvåCH3 den kommer inte att finnas under ringen utan ovanför.
På samma sätt har CH3 Det kommer inte att peka upp ringen utan under den. Rumskonfigurationer är omvända, de är motsatta. Detta är en annan av de viktigaste egenskaperna hos enatiomerism..
Propylen rotamerer
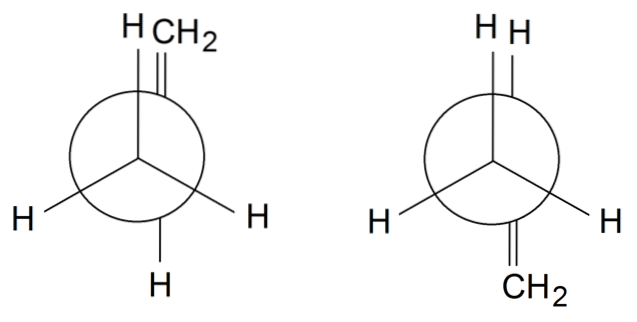
I propylen-rotamerer, för att avsluta, roterar vi enkelbindningen mellan C1 och Ctvå: H3C-CH = CHtvå. Gruppen = CHtvå är i en förmörkad position med en av H-grupperna i CH-gruppen3 fram på rotametern till vänster. Under tiden är = CHtvå och H är i alternativa positioner på höger rotamer.
Beroende på gruppens förmörkelse eller inte kommer vi att ha steriskt hinder, vilket kommer att destabilisera rotameren. Därför är rotameren till höger mer stabil än den till vänster..
Referenser
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kemi. (10th utgåva.). Wiley plus.
- Carey F. (2008). Organisk kemi. (Sjätte upplagan). Mc Graw Hill.
- Morrison och Boyd. (1987). Organisk kemi. (Femte upplagan). Addison-Wesley Iberoamericana.
- Dr. S. Gevorg. (2020). Enantiomerer, diastereomerer, identiska eller konstitutionella isomerer. Steg för kemi. Återställd från: chemistrysteps.com
- Wikipedia. (2020). Isomer. Återställd från: en.wikipedia.org
- Allison Soult. (13 augusti 2020). Isomerer. Kemi LibreTexts. Återställd från: chem.libretexts.org
- James Ashenhurst. (2020). Stereokemi och kiralitet. Återställd från: masterorganicchemistry.com


Ingen har kommenterat den här artikeln än.