
Subatomära partiklar och deras egenskaper

De subatomära partiklar De är mindre än atomen och finns i naturen, nästan alla utgör en del av den. Vi känner väl till de viktigaste och mest stabila, som är elektronen, protonen och neutronen..
All materia består av dessa partiklar, även om det finns andra, även om deras existens ignorerades under lång tid. De första atommodellerna, som dateras från några århundraden före Kristus, antog att atomerna var odelbara, något som kulor som när de kombinerades på ett visst sätt gav upphov till de olika elementen.
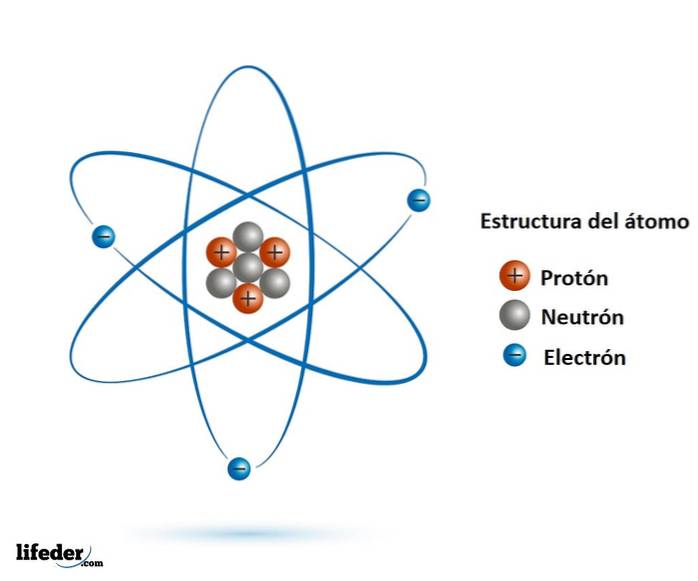
När det blev känt att detta inte var fallet, tack vare upptäckten av elektronen på 1800-talet och atomkärnan i början av 1900-talet, undrade forskare om dessa partiklar hade en inre struktur.
Det visade sig att ja, både protonen och neutronen är partiklar som består av ännu mindre, som inte har någon inre struktur: de är elementära partiklar.
Det är därför subatomära partiklar är uppdelade i:
- Förenade partiklar.
- Elementpartiklar.
De elementära partiklarna är kvarker, gluoner och leptoner. Kvarkerna och gluonerna utgör protonerna och neutronerna, medan elektronen, en elementär partikel, är en lepton.
Artikelindex
- 1 Upptäckt av subatomära partiklar
- 1.1 Atomkärnan: protoner och neutroner
- 2 De viktigaste subatomära partiklarna
- 2.1 Elektron
- 2.2 Proton
- 2.3 Neutron
- 2.4 Kvark
- 3 Andra partiklar
- 4 Referenser
Upptäckt av subatomära partiklar
Upptäckten av subatomära partiklar började på 1800-talet och den första som hittades var elektronen.
År 1890 var fysiker mycket upptagna med att studera strålning och överföring av elektromagnetiska vågor. J. J. Thomson var en av dem och han utförde ett flertal experiment med ett rör som hade fått bort luften och ett par elektroder fäst..

När en spänning applicerades producerades mystiska strålar, kallade katodstrålar, vars natur var okänd, tills J. J. Thomson (1856-1940) upptäckte att de bestod av en ström av negativt laddade partiklar.
Thomson erhöll kvoten mellan laddningen och massan av dessa partiklar: 1,76 x 108 C / g, där C betyder coulomb, enheten för elektrisk laddning i det internationella systemet för enheter och g är gram.
Och han fann två mycket viktiga saker, det första att partiklarnas massa var extremt liten och för det andra att detta värde var detsamma för dem alla, oavsett vad elektroderna var gjorda av..
Värdet på laddningen hittades strax efter, i början av 1900-talet, av den amerikanska fysikern Robert Millikan (1868-1953) och hans medarbetare, tack vare experimentet med droppen olja.
Atomkärnan: protoner och neutroner
I slutet av 1800-talet hade Henri Becquerel (1852-1908) upptäckt fenomenet naturlig radioaktivitet, som fascinerade andra fysiker som Marie och Pierre Curie, liksom Nya Zeelandern Ernest Rutherford..
Den senare hittade tre olika typer av strålning från uranprover, ett känt radioaktivt element. Han namngav dem med de tre första bokstäverna i det grekiska alfabetet: α, β och γ.
Rutherford spridningsexperiment

Med hjälp av de mycket energiska, positivt laddade α-partiklarna bombade Rutherford tunna guldfolier och fann att, som förväntat, de flesta av α-partiklarna passerade genom folierna utan problem.
Men konstigt nog avböjdes en liten del av partiklarna och några studsade till och med i motsatt riktning. Det senare var ofattbart, för som Rutherford hävdade, det var som att skjuta ett gevär mot en tunn näsduk och se kulorna återvända..
Anledningen till att α-partiklarna avböjs är att det finns något inuti arket som stöter bort dem och därför måste det vara positivt laddat. Det är atomkärnan, liten i storlek, men innehåller nästan hela atomens massa.
Upptäckten av neutronen

Neutronen tog lite längre tid att hitta och berodde på den engelska fysikern James Chadwick (1891-1974), en student vid Rutherford. Rutherford själv hade föreslagit förekomsten av en oladdad partikel i kärnan, för att förklara varför den inte sönderfaller på grund av elektrostatisk avstötning.
Chadwicks experiment avslöjade 1932 förekomsten av en masspartikel som mycket liknar protonens, men utan laddning. Det är därför de kallade det en neutron och tillsammans med protonen är de de väsentliga komponenterna i atomkärnan.
De viktigaste subatomära partiklarna
I allmänhet kännetecknas subatomära partiklar av att de har:
- Massa.
- Elektrisk laddning.
- Snurra.
Snurr är en kvalitet som är analog med rotation runt axeln, men helt kvant i sin natur. Och å andra sidan finns det partiklar med laddning och massa 0, som foton.
Elektron
Elektronen är en stabil subatomär partikel, negativt laddad och tillhör gruppen leptoner, den som har den lägsta massan. Det är en väsentlig del av atomen, men den kan existera isolerad från den, i form av fria elektroner.
I själva verket är det den minsta elektriska laddningen som finns i naturen, så vilken annan laddning som helst är en multipel av elektronens, enligt principen om laddningskvantisering..
Dess huvudsakliga egenskaper är:
- Massa: 9,1 x 10-31 kg
- Belastning: e = -1,6 x 10-19 C
- Snurr: ± ½
- Antipartikel: positron.
Elektronen är ansvarig för bildandet av kemiska bindningar, liksom för elektrisk och termisk ledning. Och tack vare kvantmekanik vet vi att elektronen har ett dubbelt beteende: våg och partikel samtidigt.
Proton
Det är en elektriskt laddad partikel vars laddning har samma storlek som elektronens, men med motsatt tecken..
Protonen är inte en elementär partikel som elektronen, men består av tre kvarkar som förenas av gluoner och det är mycket mer massivt än elektronen.
Till skillnad från detta är protonen begränsad till atomkärnan, och dess kvantitet avgör vilket element det är, liksom dess egenskaper..
- Massa: 1672 x 10-27 kg
- Laddning: e = +1,6 x 10-19 C
- Snurr: ½
- Antipartikel: antiproton.
Neutron
Neutronen tillsammans med protonen utgör atomkärnan och den består också av tre kvarkar: två av typen ner och en i slag upp.
- Massa: 1675 x 10-27 kg
- Ingen nettoladdning.
- Snurr: ½.
Det är en stabil partikel i atomkärnan, men som en fri partikel sönderfaller den med en halveringstid på cirka 10,3 minuter. Dess massa är något större än protonens och som vi har sagt har den ingen nettoladdning..
Antalet neutroner i en atom är viktigt, för även om det inte bestämmer elementets natur, som protonen gör, bestämmer det dock isotopklassen..
Elementets isotoper är varianter av det och deras beteende kan skilja sig mycket från varandra. Det finns stabila och instabila sådana, till exempel har väte deuterium och tritium som isotoper.
Genom att bombardera atomerna i vissa uran- och plutoniumföreningar med neutroner klyvs kärnan och sönderdelas i partiklar. Den kärnkedjereaktion som inträffar kan avge en stor mängd energi.
Quarks
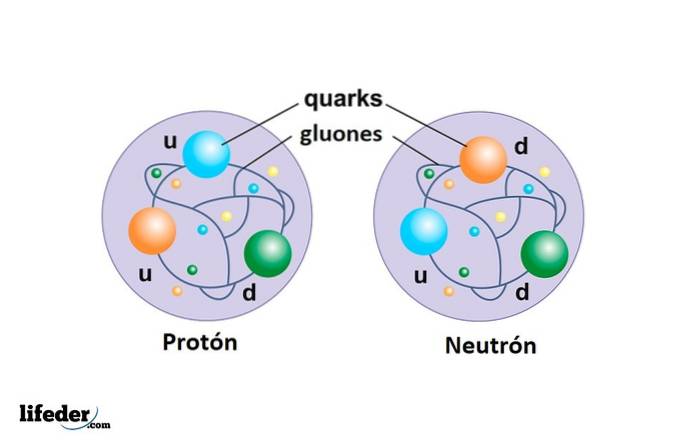
De är beståndsdelarna i protoner och neutroner. Hittills har 6 typer av kvarkar hittats, men ingen som en fri partikel, utan snarare associerad till att bilda andra sammansatta partiklar.
Bevisen för dess existens erhölls genom experiment som utförts sedan 1960-talet, med Stanford linjäraccelerator och senare vid CERN.
- Laddning: + 2 / 3e, -1 / 3e
- Snurr: ½
- Antipartikel: antikvark.
Andra partiklar
Från och med 1930 följde upptäckterna av nya partiklar, många förutsagda av teorin. Standardmodellen för partiklar tar hänsyn till förekomsten av 17 typer av grundläggande partiklar, bland kvarker, leptoner, bosoner och Higgs-bosonen..
De har också sina respektive antipartiklar, som, när de interagerar, förintar och genererar nya partiklar. Här är några av dem:
-Positron, identisk med elektronen men positivt laddad.
-Neutrino, utan kostnad.
-meson.
-Bosons, som är bärare av grundläggande interaktioner, utom gravitation.
-Higgs-bosonen, ansvarig för massan.
-Graviton, är en partikel som föreslås för att förklara gravitationen, men det finns fortfarande inga bevis för att den existerar.
Referenser
- Chang, R. 2013. Kemi. 11: e. Utgåva. Mc Graw Hill utbildning.
- Cobian, J. Standardmodellen för partiklar. Återställd från: sne.es.
- Fernández de Sala, P. Elementära partiklar, kompositpartiklar och virtuella partiklar. Återställd från: ific.uv.es.
- Giambattista, A. 2010. Fysik. 2: a. Ed McGraw Hill.
- Olmo, M. Protoner och neutroner. Återställd från: hyperphysics.phy-astr.gsu.edu.



Ingen har kommenterat den här artikeln än.