
Endotermisk och exoterm reaktion

A endoterm reaktion kräver ström medan a exoterm reaktion frigör energi. Denna klassificering av kemiska reaktioner tar hänsyn till deltagandet av energi antingen som en reaktant eller som en produkt..
Energi är förmågan att utföra arbete eller att producera värme. Kom ihåg att kemiska reaktioner innebär en omorganisation av atomer mellan ämnen med brott eller bildning av kemiska bindningar. I allmänhet åtföljs denna bildning eller brytning av kemiska bindningar av förändringar i systemets energi..
| Endoterm reaktion | Exoterm reaktion | |
|---|---|---|
| Definition | Kemisk reaktion där energi absorberas. | Kemisk reaktion där energi släpps ut i form av värme. |
| Energins ursprung | Av miljön | Av systemet |
| Potentiell energi | Lägre i reaktanter än i produkter. | Större reaktanter än i produkter. |
| Produktion | Inte spontant | Spontan |
| Intern energiförändring | AE> 0; intern energi förändring större än noll. | AE<0; cambio de energía interna menor que cero. |
| Temperatur | Minskar | Ökar |
| Exempel | Reaktioner i fotosyntes och syntes i allmänhet. | En brinnande tändsticka, förbränningsreaktioner. |
Vad är en endoterm reaktion?
En kemisk reaktion är endoterm när absorberar energi från miljön. I detta fall överförs värmen från utsidan till systemets insida. När vi placerar en termometer medan den endotermiska reaktionen pågår, sjunker temperaturen.
Ordet "endoterm" kommer från grekiska endon vilket betyder "inuti" och term vilket betyder "värme". Endotermiska reaktioner fortsätter inte spontant.
Varifrån kommer energin i endotermiska reaktioner?
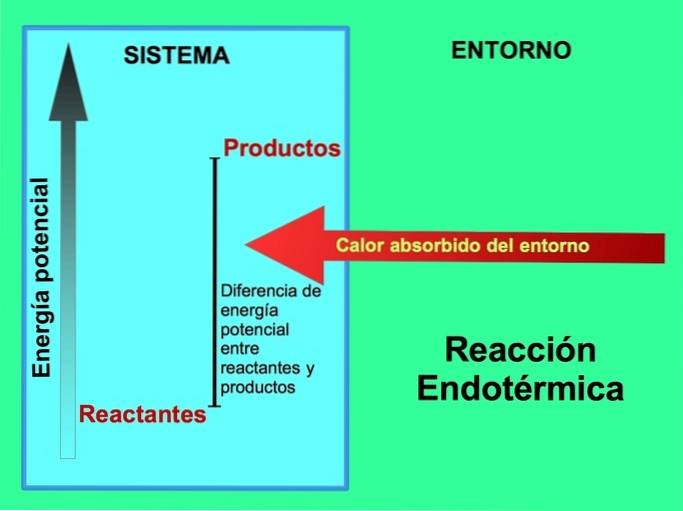
I endotermiska reaktioner kommer energin från omgivningen utanför systemet. Mängden potentiell energi för produkterna är större än den potentiella energin för reaktanterna. Därför är det nödvändigt att lägga till energi till reaktanterna för att reaktionen ska fortsätta. Denna energi kommer från miljövärmen.
Till exempel, fotosyntes är en endoterm process, där växter fångar solenergi för att producera glukos från koldioxid och syre:

Produkterna från fotosyntesreaktionen, glukos och syre, har en större mängd potentiell energi med avseende på reaktanter, koldioxid och vatten. Andra exempel på endotermiska kemiska reaktioner med mängden energi som används:

Exempel på endoterm reaktion
Det är inte bara i kemilaboratoriet som reaktioner uppstår. Dagligen hittar vi också situationer där endotermiska reaktioner uppträder.
Lagar mat
Även om det kanske inte verkar som det, är processen att laga mat endoterm. För att konsumera vissa livsmedel måste vi ge värme.
Omedelbar kallpåse
Kallförpackningar som används för att behandla stötar eller stukningar är fyllda med vatten, men när de skakas eller slås, bryts en kapsel innehållande ammoniumnitrat inuti. Blandning av ammoniumnitrat med vatten är en endoterm reaktion som får påsen att svalna.
Vad är en exoterm reaktion?
A exoterm reaktion är en där energi flyter ut ur systemet. Denna energi frigörs i form av värme, så att placera en termometer i reaktionssystemet ökar temperaturen.
Ordet "exoterm" bildas av exo vilket betyder "utåt" och termar, vilket betyder "värme". Exoterma reaktioner kan uppstå spontant och i vissa fall vara explosiva, såsom kombinationen av alkalimetaller och vatten.
Varifrån kommer energin i exoterma reaktioner?
I en kemisk reaktion är reaktanter de föreningar som transformerar och ger upphov till produkter. Till exempel, när natrium Na reagerar med klor Cl, är dessa reaktanterna och produkten är natriumklorid NaCl:
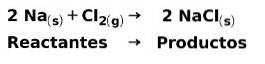
Både reaktanter och produkter har lagrad potentiell energi. Vi vet från lenergibesparing ey att energi varken går förlorad eller har vunnits, så reaktanternas energi måste vara lika med den för produkterna.
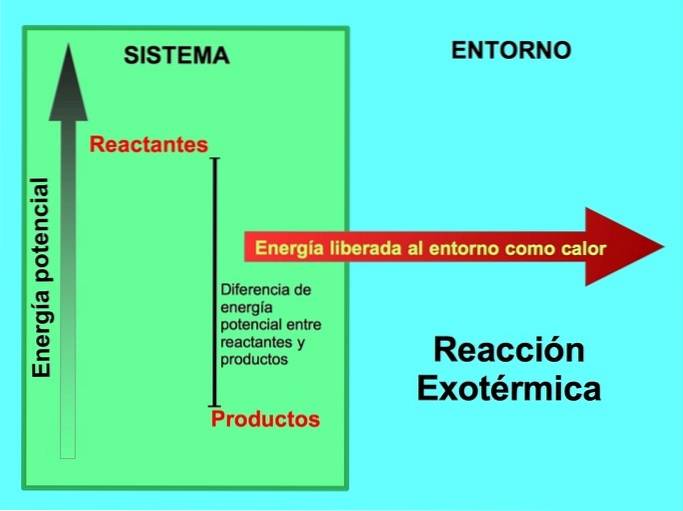
I en exoterm reaktion, lreaktanter har mer potentiell energi jämfört med produkter, så överflödig energi frigörs som värme. I detta fall anses energi också som en del av produkterna:

I varje exotermisk process omvandlas en del av den potentiella energi som lagras i kemiska bindningar till värmeenergi genom värme..
Exempel på exoterm reaktion
Tvättmedel
När vi löser upp lite tvättpulver med vatten i händerna kan vi känna en lätt uppvärmning.
Inhemsk gasförbränning
Förbränningen av gaser för hushållsbruk, såsom metan eller butan, involverar den kemiska reaktionen med syre med bildandet av koldioxid och vatten och frigöring av energi. Detta är en typisk exoterm reaktion i daglig användning:
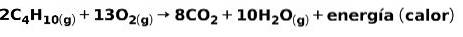
Energin som frigörs vid förbränningsprocessen används för att laga mat.
Du kan också vara intresserad av att veta vad som är öppet system, slutet system och isolerat system.



Ingen har kommenterat den här artikeln än.