
Ytspänningsorsaker, exempel, applikationer och experiment
De ytspänning Det är en fysisk egenskap som alla vätskor finns och kännetecknas av motståndet som deras ytor motsätter sig en ökning av deras område. Detta är detsamma som att säga att ytan kommer att leta efter minsta möjliga yta. Detta fenomen sammanflätar flera kemiska begrepp, såsom sammanhållning, vidhäftning och intermolekylära krafter..
Ytspänning är ansvarig för bildandet av ytskurvningar av vätskor i rörbehållare (graderade cylindrar, kolonner, provrör etc.). Dessa kan vara konkava (böjda i form av en dal) eller konvexa (böjda i en kupolform). Många fysiska fenomen kan förklaras genom att överväga de förändringar som en vätskes ytspänning genomgår..

Ett av dessa fenomen är tendensen hos flytande molekyler att agglomerera i form av droppar när de vilar på ytor som stöter bort dem. Till exempel kan vattendropparna som vi ser ovanpå bladen inte fukta det på grund av dess vaxartade, hydrofoba yta..
Men det kommer en tid då tyngdkraften spelar sin roll och droppen sprids ut som en vattenpelare. Liknande fenomen förekommer i sfäriska droppar av kvicksilver när de spills från en termometer.
Å andra sidan är vattens ytspänning det viktigaste av allt eftersom det bidrar till och organiserar tillståndet hos mikroskopiska kroppar i vattenmedier, såsom celler och deras lipidmembran. Dessutom är denna spänning ansvarig för det faktum att vattnet avdunstar långsamt och vissa kroppar tätare än det kan flyta på ytan..
Artikelindex
- 1 Orsaker till ytspänning
- 2 enheter
- 3 Ytspänning av vatten
- 4 Andra exempel
- 4.1 Kondenserade gaser
- 4.2 Icke-polära vätskor
- 4.3 Polära vätskor
- 5 applikationer
- 5.1 Tvättmedel
- 5.2 Emulsioner
- 6 enkla experiment
- 6.1 Klippexperiment
- 6.2 Pappersbåt
- 7 Referenser
Orsaker till ytspänning
Förklaringen till fenomenet ytspänning ligger på molekylär nivå. Vätskans molekyler interagerar med varandra på ett sådant sätt att de är sammanhängande i sina oregelbundna rörelser. En molekyl interagerar med sina grannar bredvid den och med dem ovanför eller under den.
Detta händer dock inte samma sak med molekylerna på vätskans yta, som är i kontakt med luft (eller någon annan gas) eller med ett fast ämne. Molekyler på ytan kan inte sammanhållas med de i den yttre miljön.
Som ett resultat upplever de inga krafter som drar dem uppåt; bara nedåt, från sina grannar i det flytande mediet. För att motverka denna obalans "kläms" ytmolekylerna, för bara på detta sätt kan de övervinna kraften som trycker ner dem.
En yta skapas där molekylerna är i ett mer spänt arrangemang. Om en partikel vill tränga igenom vätskan måste den först korsa denna molekylära barriär proportionell mot ytspänningen för vätskan. Detsamma gäller en partikel som vill fly till den yttre miljön från vätskans djup..
Därför beter sig dess yta som om det vore en elastisk film som visar motstånd mot deformation..
Enheter
Ytspänning representeras vanligtvis av symbolen γ och uttrycks i enheterna N / m, kraft gånger längd. Men för det mesta är dess enhet dyn / cm. Man kan konverteras till den andra med följande omvandlingsfaktor:
1 dyn / cm = 0,001 N / m
Ytspänning av vatten
Vatten är den sällsynta och mest fantastiska av alla vätskor. Dess ytspänning, liksom flera av dess egenskaper, är ovanligt hög: 72 dyn / cm vid rumstemperatur. Detta värde kan öka till 75,64 dyn / cm, vid en temperatur av 0 ºC; eller minska till 58,85 ºC, vid en temperatur på 100 ºC.
Dessa observationer är vettiga när man tänker på att den molekylära barriären stramar åt ännu mer vid temperaturer nära frysning, eller om den "lossnar" lite mer runt kokpunkten..
Vatten har en hög ytspänning på grund av dess vätebindningar. Om dessa i sig är märkbara i vätskan är de ännu mer på ytan. Vattenmolekyler är starkt intrasslade och bildar interaktioner mellan dipol och dipol av H-typ.tvåOH OH.

Sådan är effektiviteten i deras interaktioner att den vattenhaltiga molekylära barriären till och med kan stödja vissa kroppar innan de sjunker. I applikations- och experimentavsnitten kommer denna punkt att återtas.
Andra exempel
Alla vätskor uppvisar ytspänningar, antingen i mindre eller större grad än vatten, eller om de är rena ämnen eller lösningar. Hur starka och spända de molekylära barriärerna på dess ytor är beror direkt på deras intermolekylära interaktioner, såväl som strukturella och energiska faktorer..
Kondenserade gaser
Till exempel interagerar gasmolekyler i flytande tillstånd bara med varandra genom Londons dispersiva krafter. Detta överensstämmer med att deras ytspänningar har låga värden:
-Flytande helium, 0,37 dyn / cm vid -273 ºC
-Flytande kväve, 8,85 dyn / cm vid -196 ºC
-Flytande syre, 13,2 dyn / cm vid -182 ºC
Ytspänningen för flytande syre är högre än för helium eftersom dess molekyler har en större massa..
Apolära vätskor
Icke-polära och organiska vätskor förväntas ha högre ytspänningar än dessa kondenserade gaser. Bland några av dem har vi följande:
-Dietyleter, 17 dyn / cm vid 20 ° C
-n-Hexan, 18,40 dyn / cm vid 20 ° C
-n-Oktan, 21,80 dyn / cm vid 20 ° C
-Toluen, 27,73 dyn / cm vid 25 ºC
En liknande trend observeras för dessa vätskor: ytspänningen ökar när deras molekylmassor ökar. Men n-Oktan bör enligt detta ha den högsta ytspänningen och inte toluen. Här spelar molekylära strukturer och geometrier in.
Toluenmolekyler, platta och ringa, har effektivare interaktioner än de av n-oktan. Därför är toluenens yta "tätare" än ytan på n-oktan.
Polära vätskor
Eftersom det finns starkare dipol-dipolinteraktioner mellan molekylerna i en polär vätska är deras tendens att visa högre ytspänningar. Men så är inte alltid fallet. Bland några exempel har vi:
-Ättiksyra, 27,60 dyn / cm vid 20 ° C
-Aceton, 23,70 dyn / cm vid 20 ° C
-Blod, 55,89 dyn / cm vid 22 ° C
-Etanol, 22,27 dyn / cm vid 20 ° C
-Glycerol, 63 dyn / cm vid 20 ° C
-Smält natriumklorid, 163 dyn / cm vid 650 ° C
-6 M NaCl-lösning, 82,55 dyn / cm vid 20 ° C
Smält natriumklorid förväntas ha enorm ytspänning: det är en viskös, jonisk vätska..
Å andra sidan är kvicksilver en av vätskorna med den högsta ytspänningen: 487 dyn / cm. I den består dess yta av starkt sammanhängande kvicksilveratomer, mycket mer än vattenmolekyler kan vara..
Applikationer

Enbart ytspänningen har inga applikationer. Detta betyder dock inte att det inte är involverat i olika dagliga fenomen, som om de inte fanns, inte skulle uppstå..
Till exempel kan myggor och andra insekter gå genom vatten. Detta beror på att deras hydrofoba ben stöter bort vatten, medan deras låga massa gör att de kan hålla sig flytande på den molekylära barriären utan att falla till botten av floden, sjön, dammen etc..
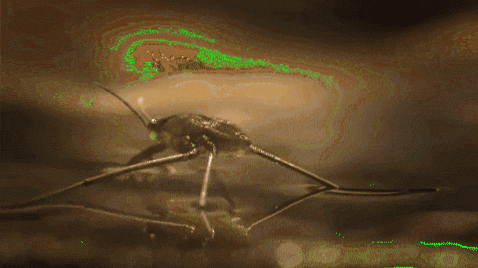
Ytspänningen spelar också en roll i vätskans vätbarhet. Ju högre ytspänning desto mindre tenderar den att sippra genom porer eller sprickor i ett material. Utöver detta är de inte särskilt användbara vätskor för att rengöra ytor.
Tvättmedel
Det är här rengöringsmedel verkar, vilket minskar vattens ytspänning och hjälper det att täcka större ytor; samtidigt som den förbättrar dess avfettningsverkan. Genom att minska ytspänningen ger det plats för luftmolekyler, med vilka det bildar bubblor..
Emulsioner
Å andra sidan är låga högre spänningar kopplade till stabiliseringen av emulsionerna, vilket är mycket viktigt vid formuleringen av ett annat produktutbud..
Enkla experiment

Slutligen kommer några experiment som kan utföras i vilket som helst inhemskt utrymme att citeras..
Klippsexperiment
En metallklämma placeras på ytan i ett glas kallt vatten. Som framgår av bilden ovan kommer klämman att hålla sig flytande tack vare vattens ytspänning. Men om du lägger till lite lergodslava i glaset kommer ytspänningen att sjunka dramatiskt och gemet plötsligt sjunker..
Pappersbåt
Om vi har en pappersbåt eller en träpall på ytan, och om diskmaskinen eller tvättmedlet läggs till en svabbs huvud, kommer ett intressant fenomen att inträffa: det kommer att finnas en avstötning som sprider dem mot kanterna på glas. Pappersbåten och träpallen kommer att flytta bort från tvättpinnen med tvättmedel.

Ett annat liknande och mer grafiskt experiment består i att upprepa samma operation, men i en hink med vatten beströs med svartpeppar. De svarta pepparpartiklarna kommer att glida bort och ytan kommer att ändras från peppar täckt till kristallklart, med peppar på kanterna.
Referenser
- Whitten, Davis, Peck & Stanley. (2008). Kemi. (8: e upplagan). CENGAGE Learning.
- Wikipedia. (2020). Ytspänning. Återställd från: en.wikipedia.org
- USGS. (s.f.). Ytspänning och vatten. Återställd från: usgs.gov
- Jones, Andrew Zimmerman. (12 februari 2020). Ytspänning - Definition och experiment. Återställd från: thoughtco.com
- Susanna Laurén. (2017, 15 november). Varför är ytspänningen viktig? Biolin Scientific. Återställd från: blog.biolinscientific.com
- Rookie Parenting Science. (07 november 2019). Vad är ytspänning | Cool vetenskapsexperiment. Återställd från: rookieparenting.com
- Jessica Munk. (2020). Ytspänningsexperiment. Studie. Återställd från: study.com
- Barnet borde se det här. (2020). Sju ytspänningsexperiment - Physics Girl. Återställd från: thekidshouldseethis.com


Ingen har kommenterat den här artikeln än.