
Uracil struktur, funktioner, egenskaper, syntes
De uracil Det är en kvävebas av pyrimidintyp, som finns i ribonukleinsyra (RNA). Detta är en av egenskaperna som skiljer RNA från deoxiribonukleinsyra (DNA), eftersom den senare har tymin istället för uracil. Båda substanserna, uracil och tymin, skiljer sig bara genom att den andra har en metylgrupp.
Ur en evolutionär synvinkel har det föreslagits att RNA var den första molekylen som lagrade genetisk information och fungerade som en katalysator i celler före DNA och enzymer. På grund av detta anses uracil ha spelat en nyckelroll i livets utveckling.
I levande saker finns uracil inte i fri form utan bildar ofta nukleotider monofosfat (UMP), difosfat (UDP) och trifosfat (UTP). Dessa uracil-nukleotider har olika funktioner, såsom RNA- och glykogenbiosyntes, isomer interkonvertering av sockerarter och reglering av glutaminsyntas..
Artikelindex
- 1 Struktur och egenskaper
- 2 Biosyntes
- 2.1 Reglering av biosyntes
- 3 Roll i RNA-biosyntes
- 4 Roll i biosyntes av socker
- 5 Roll i den isomera omvandlingen av sockerarter
- 6 Roll i glykoproteinbiosyntes
- 7 Roll i regleringen av glutaminsyntas
- 8 Roll i RNA-redigering
- 9 Biosyntes av UDP-glukos
- 10 Uracil DNA-glykosylas
- 11 Referenser
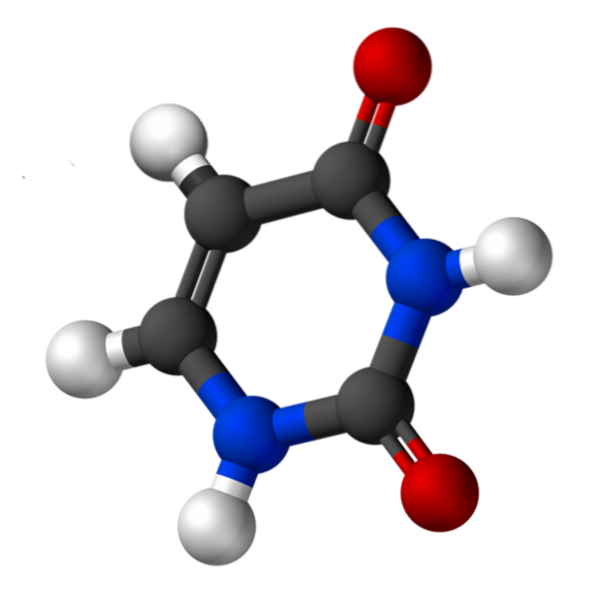
Struktur och egenskaper
Uracil, kallad 2,4-dioxypyridin, har den empiriska formeln C4H4NtvåELLERtvå, vars molekylvikt är 112,09 g / mol och renas som ett vitt pulver.
Uridins struktur är en heterocyklisk ring med fyra kolatomer och två kväveatomer, med alternerande dubbelbindningar. Är plan.
Den har en löslighet på 50 mg / ml vid 25 ° C i 1 M natriumhydroxid och en pKa mellan 7,9 och 8,2. Våglängden där dess maximala absorbans uppträder (ʎmax) är mellan 258 och 260 nm.
Biosyntes
Det finns en gemensam väg för pyrimidinnukleotidbiosyntes (uracil och cytokin). Det första steget är biosyntesen av karbamoylfosfat från COtvå och NH4+, som katalyseras av karbamoylfosfatsyntetas.
Pyrimidin är byggt av karboylfosfat och aspartat. Båda ämnena reagerar och bildar N-karbamoylaspartat, en reaktion katalyserad av aspartattranskabamoylas (ATCas). Förslutningen av pyrimidinringen orsakas av uttorkning katalyserad av dihydrootas och producerar L-dihydrorotat..
L-dihydrorotat oxideras och omvandlas till orotat; elektronacceptorn är NAD+. Det är en reaktion katalyserad av dihydroorotatdehydrogenas. Nästa steg är överföringen av fosforibosylgruppen, från fosforibosylpyrofosfat (PRPP), till orotat. Bildar orotidylat (OMP) och oorganiskt pyrofosfat (PPi), katalyserat av orotatfosforibosyltransferas.
Det sista steget består av dekarboxylering av pyrimidinringen i orotidylatet (OMP). Bildar uridylat (uridin-5'-monofosfat, UMP), som katalyseras av ett dekarboxylas.
Sedan, genom deltagande av ett kinas, överförs en fosfatgrupp från ATP till UMP och bildar UDP (uridin-5'-difosfat). Det senare upprepas och bildar UTP (uridin-5'-trifosfat).
Reglering av biosyntes
Hos bakterier sker reglering av pyrimidinbiosyntes genom negativ återkoppling, på nivån av aspartattranskabamoylas (ATCas).
Detta enzym inhiberas av CTP (cytidin-5'-trifosfat), som är slutprodukten av pyrimidinbiosyntetiska vägen. ATCase har reglerande underenheter som binder till den allosteriska regulatorn CTP.
Hos djur sker reglering av pyrimidinbiosyntes genom negativ återkoppling, på nivån av två enzymer: 1) karbamoylfosfatsyntas II, som inhiberas av UTP och aktiveras av ATP och PRPP; och 2) OMP-dekarboxylas, som inhiberas av produkten av reaktionen som den katalyserar, UMP. Graden av biosyntes av OMP varierar med tillgängligheten av PRPP.
Roll i RNA-biosyntes
Uracil finns i alla typer av RNA, såsom budbärar-RNA (mRNA), överförings-RNA (tRNA) och ribosomalt RNA (rRNA). Biosyntesen av dessa molekyler sker genom en process som kallas transkription..
Under transkription kopieras informationen i DNA till RNA med ett RNA-polymeras. Den omvända processen, där informationen i RNA kopieras till DNA, sker i vissa virus och växter genom omvänd transkriptas..
RNA-biosyntes kräver nukleosidtrifosfat (NTP), nämligen uridintrifosfat (UTP), cytidintrifosfat (CTP), adenintrifosfat (ATP) och guanintrifosfat (GTP). Reaktionen är:
(RNA)n rester + NTP -> (RNA)n + 1 rest + PPi
Hydrolys av oorganiskt pyrofosfat (PPi) ger energi för RNA-biosyntes.
Roll i biosyntes av socker
Sockerestrar är mycket vanliga i levande organismer. Några av dessa estrar är nukleosidester-difosfater, såsom UDP-sockerarter, som är mycket rikliga i celler. UDP-sockerarter deltar i biosyntesen av disackarider, oligosackarider och polysackarider.
I växter sker sackarosbiosyntes genom två vägar: en primär och en sekundär.
Huvudvägen är överföringen av D-glukos från UDP-D-glukos till D-fruktos för att bilda sackaros och UDP. Den sekundära vägen innehåller två steg: den börjar med UDP-D-glukos och fruktos-6-fosfat och slutar med bildandet av sackaros och fosfat..
I bröstkörtlarna sker laktosbiosyntes från UDP-D-galaktos och glukos.
I växter utförs cellulosabiosyntes genom kontinuerlig kondensation av beta-D-glukosylrester, från UDP-glukos till den icke-reducerande änden av den växande polyglukoskedjan. På liknande sätt kräver amylos- och amylopektinbiosyntes UDP-glukos som ett glukosgivarsubstrat till den växande kedjan..
Hos djur används både UDP-glukos och ADP-glukos för glykogenbiosyntes. På liknande sätt kräver kondroitinsulfatsyntes UDP-xylos, UDP-galaktos och UDP-glukuronat..
Roll i den isomera omvandlingen av sockerarter
Omvandlingen av galaktos till en glykolys-mellanprodukt sker genom Leloir-vägen. Ett av stegen i denna väg katalyseras av enzymet UDP-galaktos-4-epimeras, vilket underlättar omvandlingen av UDP-galaktos till UDP-glukos..
Roll i glykoproteinbiosyntes
Under glykoproteinbiosyntes korsar proteiner cis-, mitt- och transsäckarna i Golgi-apparaten.
Var och en av dessa säckar har en uppsättning enzymer som bearbetar glykoproteiner. Sockermonomerer, såsom glukos och galaktos, tillsätts till proteinoligosackariden från UDP-hexos och andra nukleotider-hexos.
Hexosnukleotiderna transporteras till Golgi-cisternerna med antiport. UDP-galaktos (UDP-Gal) och UDP-N-acetylgalaktosamin (UDP-GalNAc) kommer in i cisternerna från cytosolen genom utbyte mot UMP.
I Golgi-cisternen hydrolyserar en fosfatas en fosfatgrupp på UDP och bildar UMP och Pi. UDP kommer från reaktioner katalyserade av galaktosyltransferas och N-acetylgalaktosamyltransferas. UMP bildat av fosfatas tjänar för nukleotid-hexosbyte.
Roll i regleringen av glutaminsyntas
En regleringsmekanism för glutaminsyntas är kovalent modifiering, som består av adenylering, som inaktiverar det, och dedenylering, som aktiverar det. Denna kovalenta modifiering är reversibel och katalyserad av adenyltransferas..
Adenyltransferasaktivitet moduleras genom bindning av PII-proteinet, vilket regleras genom en kovalent modifiering, uridinylering.
Både uridylering och deuridylering utförs med uridylyltransferas. I detta enzym beror uridyleringsaktiviteten på glutamin och fosfat och aktiveras genom bindning av alfa-ketoglutarat och ATP till PII.
Roll i RNA-redigering
Vissa mRNA redigeras före översättning. I vissa eukaryota organismer, såsom Trypanosoma brucei, det finns RNA-redigering av cytokromoxidas-underenhet II-gentranskript. Detta händer genom införandet av uracilrester, en reaktion katalyserad av det terminala uridyltransferaset..
En guide-RNA, som kompletterar den redigerade produkten, fungerar som en mall för redigeringsprocessen. Basparen bildade mellan det ursprungliga transkriptet och styr-RNA: t innebär G = U-baspar som inte är Watson-Crick och är vanliga i RNA..
UDP-glukosbiosyntes
Under fysiologiska förhållanden är biosyntesen av glykogen från glukos-1-fosfat termodynamiskt omöjlig (AG-positiv). På grund av detta förekommer aktivering av glukos-1-fosfat (G1P) före biosyntes. Denna reaktion kombinerar G1P och UTP för att bilda uridindifosfatglukos (UDP-glukos eller UDPG)..
Reaktionen katalyseras av UDP-glukospyrofosforylas och är som följer:
G1P + UTP -> UDP-glukos + 2Pi.
Variationen i fri energi från Gibbs i detta steg är stor och negativ (-33,5 KJ / mol). Under reaktionen mot syre attackerar G1P alfa-fosforatomen i UTP och bildar UDP-glukos och oorganiskt pyrofosfat (PPi). Därefter hydrolyseras PPi av ett oorganiskt pyrofosfatas, vars hydrolysenergi är det som driver den allmänna reaktionen.
UDP-glukos är en "hög energi" substans. Det gör det möjligt att bilda glykosidbindningarna mellan glukosresten och den växande polysackaridkedjan. Samma energiska princip är tillämplig på reaktioner där UDP-sockerarter deltar, såsom biosyntes av disackarider, oligosackarider och glykoproteiner..
Uracil DNA-glykosylas
Det finns DNA-lesioner som uppträder spontant. En av dessa skador är den spontana deamineringen av cytokin och dess därmed omvandling till uracil. I detta fall sker reparation genom att avlägsna den modifierade DNA-basen med ett enzym som kallas uracil-DNA-glykosylas..
Enzymet uracil DNA-glykosylas avlägsnar det skadade cytokinet (uracil), vilket ger en deoxiribosrest som saknar kvävebasen, kallad AP-platsen (apurin-apyrimidinic site).
Enzymet AP-endonukleas skär sedan fosfodiester-ryggraden i AP-stället och tar bort socker-fosfatresten. DNA-polymeras I återställer den skadade strängen.
Referenser
- Bohinski, R. 1991. Biochemistry. Addison-Wesley Iberoamericana, Wilmington, Delaware.
- Devlin, T.M. 2000. Biokemi. Redaktionellt Reverté, Barcelona.
- Lodish, H., Berk, A., Zipurski, S.L., Matsudaria, P., Baltimore, D., Darnell, J. 2003. Cell- och molekylärbiologi. Ledare Medica Panamericana, Buenos Aires, Bogotá, Caracas, Madrid, Mexiko, Sāo Paulo.
- Nelson, D. L., Cox, M. M. 2008. Lehninger-Principles of biochemistry. W.H. Freeman, New York.
- Voet, D. och Voet, J. 2004. Biochemistry. John Wiley and Sons, USA.



Ingen har kommenterat den här artikeln än.